Geef de vergelijking van de reactie die plaatsvindt wanneer beide oplossingen bij elkaar worden gevoegd.
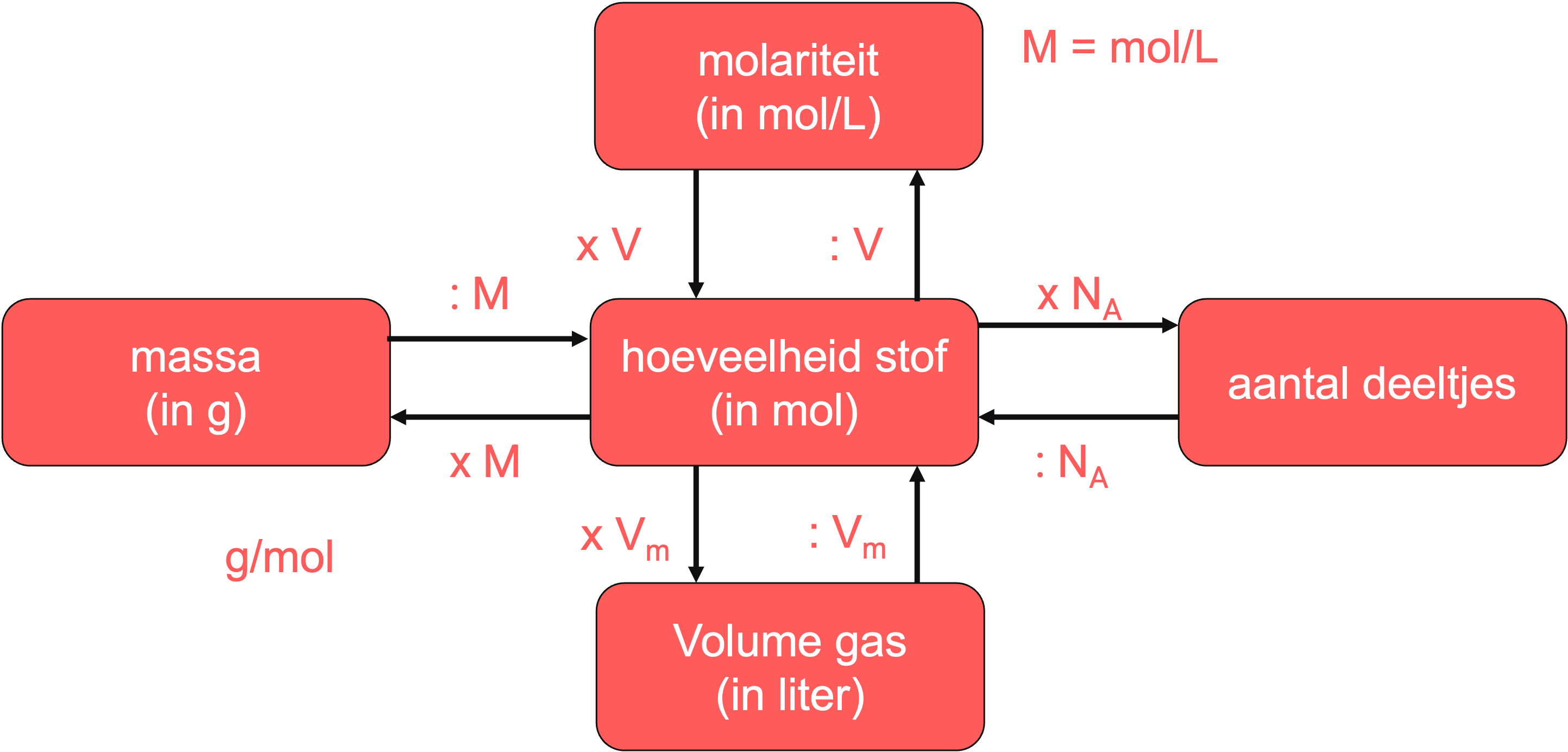
Chemische reacties begrijpen betekent vaak rekenen met hoeveelheden stoffen. Hier komt het molrekenschema van pas. Het startpunt van dit schema is het aantal mol. Vanuit het aantal mol kan je andere hoeveelheden berekenen, zoals grammen of deeltjes.
•Van mol naar gram: Vermenigvuldig het aantal mol met de molaire massa (symbool M, uitgedrukt in gram per mol) om het aantal gram te vinden.
•Van gram naar mol: Deel het aantal gram door de molaire massa (M).
•Van mol naar deeltjes: Vermenigvuldig het aantal mol met het getal van Avogadro (6,02 x 1023) om het aantal deeltjes te vinden.
•Van deeltjes naar mol: Deel het aantal deeltjes door het getal van Avogadro.
Overmaat en ondermaat
Bij een reactie kan er sprake zijn van overmaat en ondermaat. De stof die in ondermaat, dus het minst, aanwezig is, bepaalt hoeveel product er gevormd kan worden. Net zoals een fietsenmaker die afhankelijk is van het aantal beschikbare wielen om fietsen te bouwen, zo bepaalt in een chemische reactie de stof in ondermaat de hoeveelheid product.
Molariteit van ionen in een oplossing
Als we spreken over oplossingen, komt de term molariteit naar voren. Molariteit, uitgedrukt in mol per liter (mol/L), geeft de concentratie van een oplossing aan. Het berekenen van de molariteit is cruciaal om de concentratie ionen na een reactie te kunnen bepalen.
Voorbeeld van berekeningen aan reacties
Mengen van oplossingen
Neem een mengsel van bariumchloride en natriumsulfaat oplossingen. Dit mengen resulteert in de vorming van bariumsulfaat neerslag. Door de oplosbaarheidstabel te raadplegen, bepalen we welke ionen een neerslag vormen en welke in oplossing blijven. Bijvoorbeeld, bariumionen (Ba2+) met sulfaationen (SO42-) vormen een neerslag, omdat ze slecht oplosbaar zijn in water.
Vorming van Neerslag
Stel, je wil weten hoeveel gram bariumsulfaat (BaSO4) neerslag vormt. Eerst bereken je hoeveel mol van elk ion aanwezig is in de oplossingen en vervolgens gebruik je de verhoudingen uit de reactievergelijking om te bepalen welke ion in ondermaat is. De ondermaat bepaalt hoeveel mol BaSO4 kan vormen. Omzetten van mol naar gram doe je door te vermenigvuldigen met de molaire massa van BaSO4.
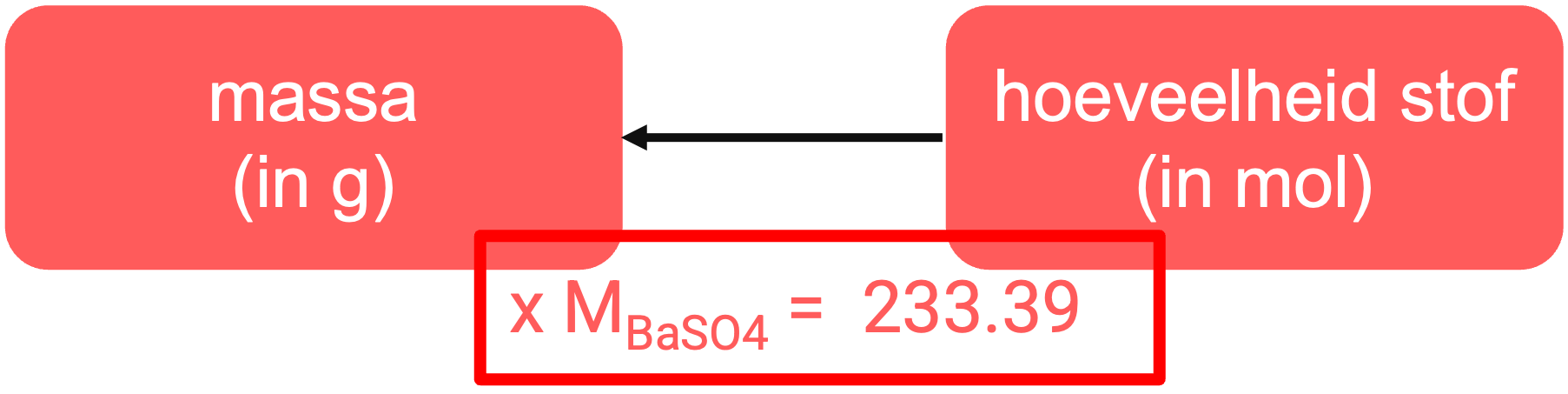
Berekenen van ionconcentraties
Na de reactie is het interessant om de concentraties van de resterende ionen te bepalen. Dit doe je door eerst voor elk ion uit te rekenen hoeveel mol aanwezig is en deze hoeveelheid te delen door het totale volume van de oplossing na de reactie. Vergeet niet dat de molariteit van ionen kan veranderen als een zout zoals Na2SO4 in water oplost.

Door het toepassen van molrekenen en het begrijpen van concepten zoals molariteit en overmaat vs. ondermaat, kun je de uitkomsten van chemische reacties succesvol voorspellen en berekenen. Deze vaardigheden zijn essentieel voor zowel theoretisch inzicht als praktische experimenten in de scheikunde. Succes met oefenen!













