Geef de neerslagvergelijking (als die ontstaat).
Leerdoelen
•Je kunt uitleggen wat een neerslagreactie is.
•Je kunt aan de hand van de oplosbaarheidstabel bepalen of een combinatie van ionen neerslaat.
•Je kunt een kloppende neerslagvergelijking opstellen voor een gegeven reactie.
•Je kunt het concept van een dynamisch evenwicht bij slecht oplosbare zouten beschrijven.
Wat is een neerslagreactie?
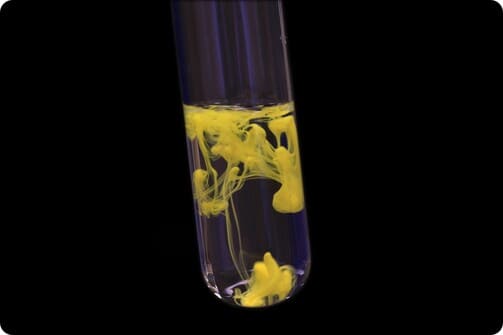
Stel je voor: je voegt twee doorzichtige vloeistoffen samen, en plotseling ontstaat er een prachtige, felgekleurde vaste stof. Hoe kan dat? Dit fenomeen is het resultaat van een neerslagreactie. Een neerslagreactie vindt plaats wanneer twee zoutoplossingen worden samengevoegd en de ionen daarin reageren om een nieuw, onoplosbaar zout te vormen. Dit onoplosbare zout zakt naar de bodem als een vaste stof, die we een neerslag noemen.
Zouten zijn verbindingen die bestaan uit een metaal en een niet-metaal, of uit een metaal en een samengesteld niet-metaal (een polyatomisch ion). In water vallen zouten uiteen in hun afzonderlijke ionen, die dan vrij in de oplossing bewegen.
Ionen in oplossing en de oplosbaarheidstabel (Binastabel 45A)
Om te bepalen of neerslag ontstaat, moeten we eerst weten welke ionen er in de oplossingen aanwezig zijn. Laten we een voorbeeld nemen: een oplossing van kaliumjodide (KI) wordt toegevoegd aan een oplossing van lood(II)nitraat (Pb(NO3)2).
Beide zijn zouten:
•Kaliumjodide (KI): kalium (K) is een metaal, jodide (I) is een niet-metaal. In water splitst dit in K+ en I-.
•Lood(II)nitraat (Pb(NO₃)₂): Lood (Pb) is een metaal, nitraat (NO₃) is een samengesteld niet-metaal. In water splitst dit in Pb²⁺ en NO₃⁻.
Voordat de oplossingen worden samengevoegd, hebben we dus vier verschillende ionen in de twee reageerbuizen: K+, I-, Pb2+ en NO3-.
Om te zien welke combinaties van deze ionen een neerslag vormen, gebruiken we Binastabel 45A, de oplosbaarheidstabel van zouten in water.
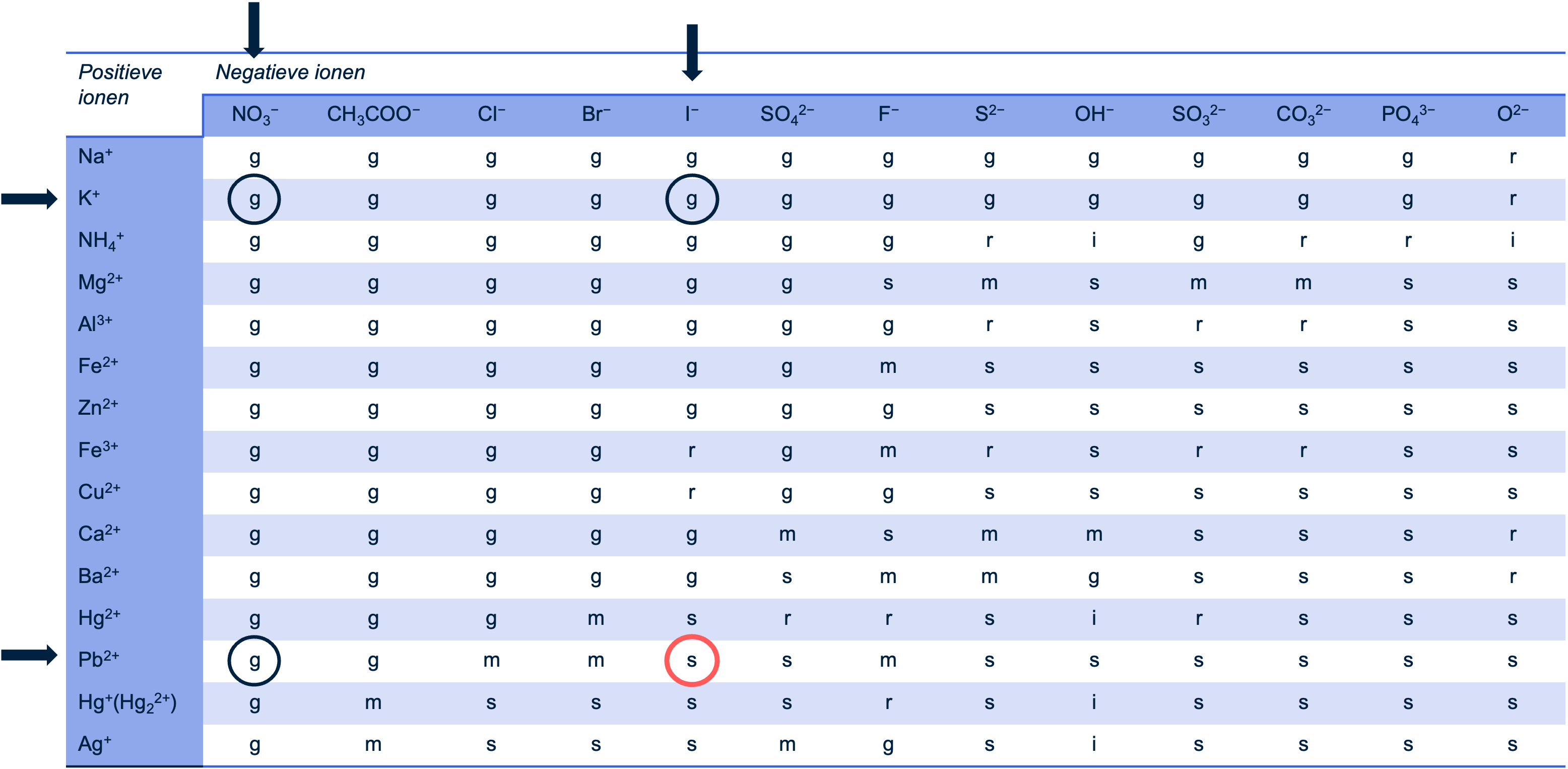
In deze tabel staan verticaal de positieve ionen en horizontaal de negatieve ionen. Op het kruispunt van een positief en een negatief ion vind je een letter die de oplosbaarheid aangeeft:
•G: Goed oplosbaar. De ionen blijven in oplossing.
•M: Matig oplosbaar. Een klein deel lost op, een deel slaat neer.
•S: Slecht oplosbaar. De ionen vormen een vaste stof (neerslag).
•I: Instabiel. De combinatie is niet stabiel.
•R: Reageert met water. De ionen reageren met watermoleculen (bijvoorbeeld het oxide-ion).
Bepalen of een neerslag ontstaat: Voorbeeld 1 (Lood(II)jodide)
We hadden de ionen K+, I-, Pb2+ en NO3-. Nu gaan we alle mogelijke nieuwe combinaties van een positief en een negatief ion bekijken met behulp van Binastabel 45A:
1.K+ en NO3- (kaliumnitraat): Zoek K+ en NO3- op in de tabel. Je zult zien dat dit een G geeft, dus kaliumnitraat is goed oplosbaar.
2.Pb²⁺ en I⁻ (lood(II)jodide): Zoek Pb²⁺ en I⁻ op in de tabel. Hier vind je een S, wat betekent dat lood(II)jodide slecht oplosbaar is. Deze combinatie zal dus een neerslag vormen.
De andere combinaties (K+ met I- en Pb2+ met NO3-) waren de oorspronkelijke zouten en waren al goed oplosbaar. De gele kleur die we zagen ontstaan, is dus de neerslag van lood(II)jodide.
Het opstellen van een neerslagvergelijking
Een neerslagvergelijking beschrijft alleen de ionen die daadwerkelijk een verandering ondergaan, namelijk het vormen van de vaste neerslag. De ionen die in oplossing blijven en niet reageren, noemen we tribune-ionen of spectator-ionen. Deze worden niet in de neerslagvergelijking opgenomen.
Voor het voorbeeld van lood(II)jodide:
•De neerslagvormende ionen zijn Pb²⁺ en I⁻.
•De tribune-ionen zijn K+ en NO3-.
Volg deze stappen om de neerslagvergelijking op te stellen:
Stap 1: Identificeer de neerslagvormende ionen. In ons voorbeeld zijn dit Pb²⁺ en I⁻.
Stap 2: Bepaal de juiste verhouding voor een neutrale ionformule. De lading van het lood(II)ion is 2+ (Pb²⁺). De lading van het jodide-ion is 1- (I-). Om een neutrale verbinding te vormen, hebben we één Pb²⁺-ion en twee I⁻-ionen nodig (). De ionformule van de neerslag is dus PbI₂.
Stap 3: Schrijf de neerslagvergelijking op. De ionen in oplossing krijgen de toestandscode (aq) van 'aqua' (water). De vaste neerslag krijgt de toestandscode (s) van 'solid' (vast). Pb²⁺(aq) + 2I⁻(aq) → PbI₂(s)
Let op: net zoals bij oplosvergelijkingen (bijvoorbeeld NaCl(s) → Na+(aq) + Cl-(aq)), schrijf je geen watermoleculen in de vergelijking, ook al vindt de reactie in water plaats.
Bepalen of een neerslag ontstaat: Voorbeeld 2 (calciumcarbonaat)
Laten we nog een voorbeeld proberen: een oplossing van calciumchloride (CaCl2) wordt toegevoegd aan een oplossing van natriumcarbonaat (Na2CO3).
De aanwezige ionen zijn: Ca²⁺, Cl⁻, Na⁺ en CO₃²⁻.
Weer kijken we naar de mogelijke nieuwe combinaties:
1.Ca²⁺ en CO₃²⁻ (calciumcarbonaat): Zoek Ca²⁺ en CO₃²⁻ op in Binatabel 45A. Je zult een S vinden, wat betekent dat calciumcarbonaat slecht oplosbaar is en een neerslag zal vormen.
2.Na+ en Cl- (natriumchloride): Zoek Na+ en Cl- op. Dit geeft een G, dus natriumchloride is goed oplosbaar en blijft in oplossing.
De tribune-ionen zijn hier Na+ en Cl-. De neerslagvormende ionen zijn Ca²⁺ en CO₃²⁻.
Neerslagvergelijking voor calciumcarbonaat:
•Ionen: Ca²⁺ en CO₃²⁻.
•Ladingen: Ca²⁺ (2+) en CO₃²⁻ (2-). De verhouding is 1:1.
•Ionformule: CaCO₃.
•Vergelijking: Ca²⁺(aq) + CO₃²⁻(aq) → CaCO₃(s)
Dynamisch evenwicht bij slecht en matig oplosbare zouten
Wanneer we zeggen dat een zout "slecht oplosbaar" is, betekent dit niet dat er helemaal niets oplost. Er lost altijd een heel klein beetje zout op. Bij slecht en matig oplosbare zouten ontstaat er een dynamisch evenwicht.
Een dynamisch evenwicht houdt in dat, zelfs nadat de vaste neerslag naar de bodem is gezakt, er nog steeds een constante uitwisseling plaatsvindt tussen de vaste stof en de opgeloste ionen. Per tijdseenheid gaan er evenveel ionen vanuit het neergeslagen zout de oplossing in als dat er ionen vanuit de oplossing weer vast worden en zich bij de neerslag voegen.
De concentraties van de ionen in de oplossing blijven hierdoor constant, ook al is er voortdurend beweging (dynamiek) van ionen.
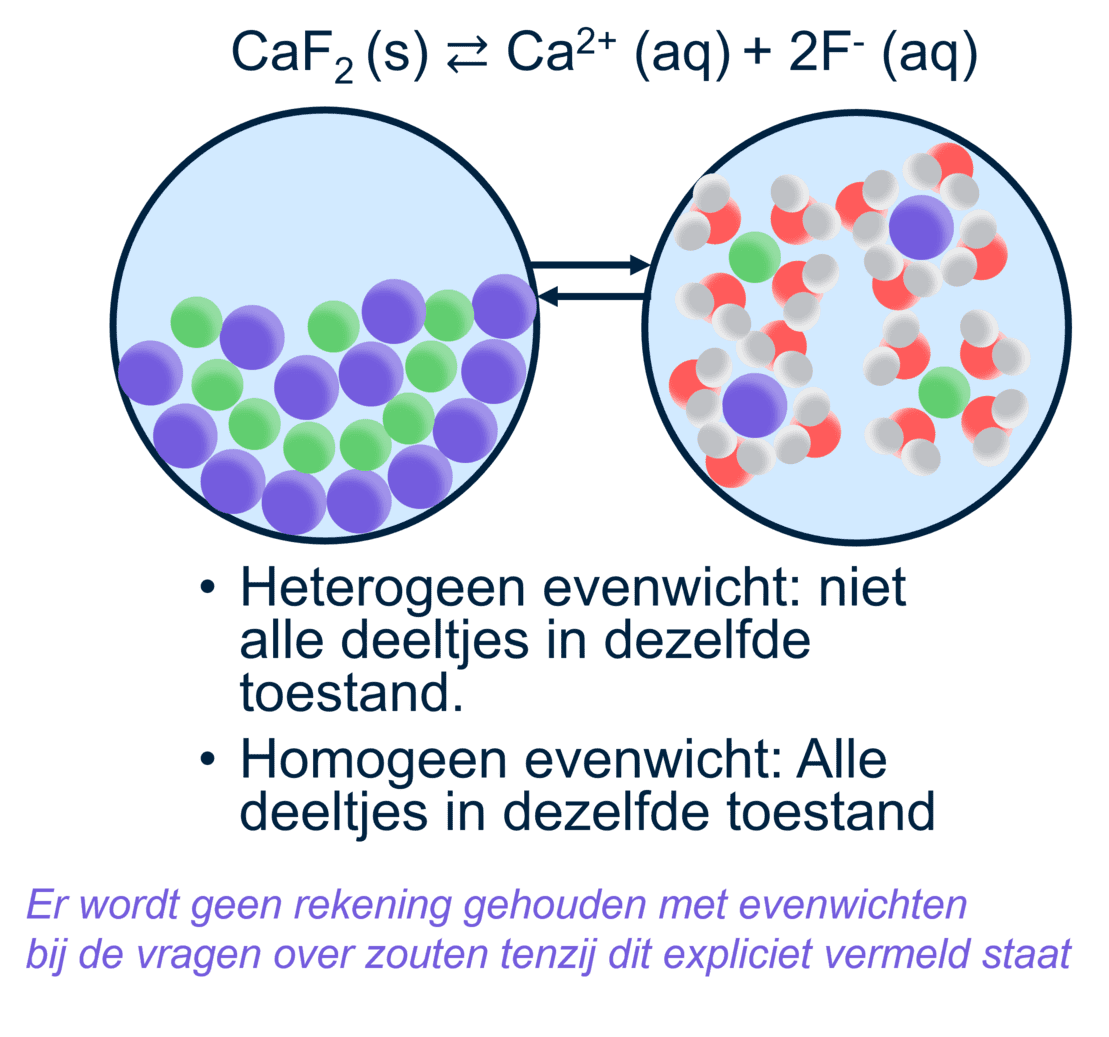
Een voorbeeld hiervan is calciumfluoride (CaF₂): CaF₂(s) ⇌ Ca²⁺(aq) + 2F⁻(aq)
De dubbele pijl (⇌) geeft aan dat het een evenwichtsreactie is, waarbij de reactie in beide richtingen plaatsvindt.
Soorten evenwichten
Er zijn twee hoofdtypen evenwichten:
•Heterogeen evenwicht: dit is het geval wanneer de deeltjes in het evenwicht zich in verschillende aggregatietoestanden bevinden. Bijvoorbeeld, bij een neerslagreactie hebben we een vaste stof (s) en opgeloste ionen (aq). Dit is een heterogeen evenwicht.
•Homogeen evenwicht: hierbij bevinden alle deeltjes in het evenwicht zich in dezelfde aggregatietoestand (bijvoorbeeld allemaal gas, allemaal vloeistof of allemaal opgelost in water).
Voor de meeste scheikundevragen op de middelbare school hoef je geen rekening te houden met het dynamisch evenwicht, tenzij dit expliciet in de vraag wordt vermeld.













