Wat zijn isotopen?
Leerdoelen
•Je kunt uitleggen wat isotopen zijn en hoe ze van elkaar verschillen
•Je kunt beschrijven wat radioactiviteit is en waarom sommige atomen radioactief zijn
•Je kunt uitleggen wat activiteit is en hoe het wordt gemeten
•Je kunt rekenen met halveringstijd en de activiteit van een radioactieve stof na een bepaalde tijd bepalen
Isotopen en radioactiviteit
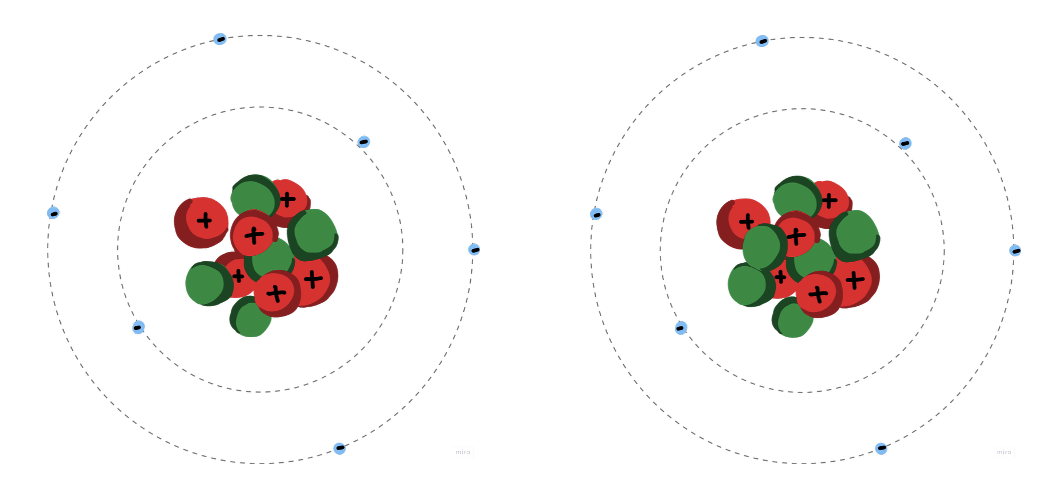
Isotopen zijn varianten van hetzelfde chemische element die hetzelfde aantal protonen, maar een verschillend aantal neutronen in hun kern hebben. Neem bijvoorbeeld koolstof: alle koolstofatomen hebben zes protonen, maar het aantal neutronen kan variëren. Dit verschil in neutronen leidt tot verschillende isotopen van koolstof, zoals koolstof-11 en koolstof-12. Het massagetal van een isotoop is de som van het aantal protonen en neutronen in de kern.
Waarom zijn sommige atomen radioactief?
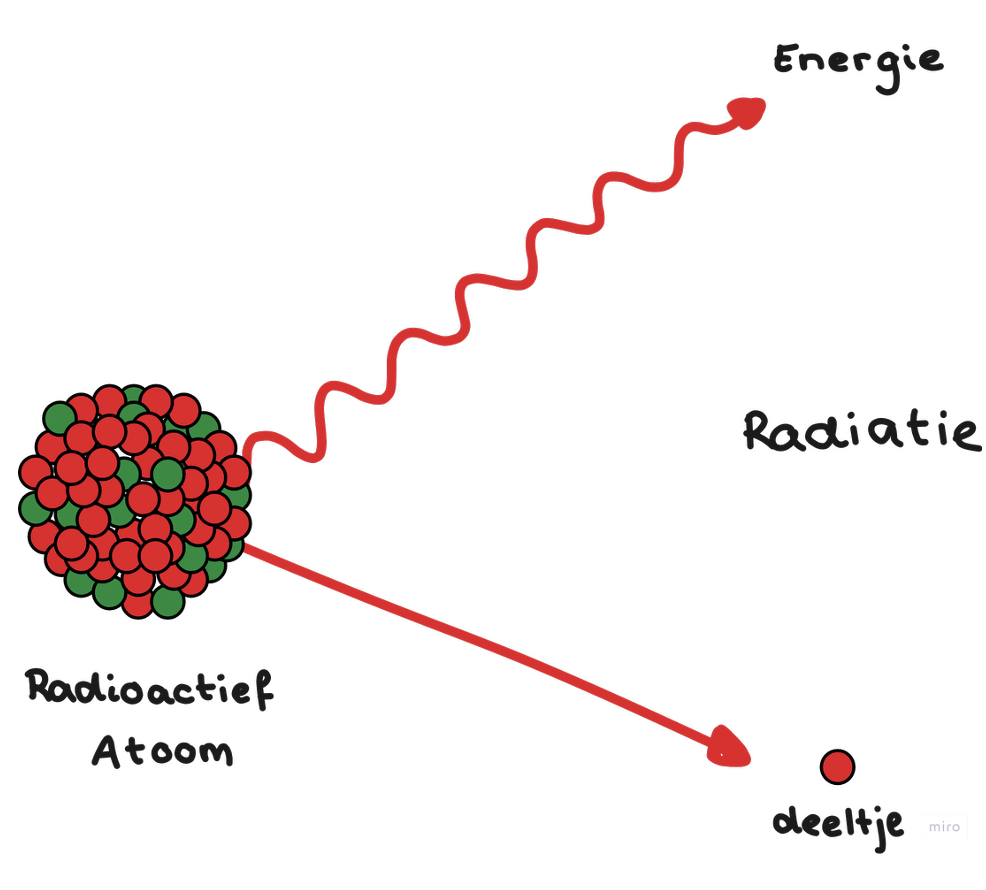
Niet alle isotopen zijn radioactief. Een isotoop is radioactief als de kern instabiel is, wat betekent dat er een onevenwichtige verhouding is tussen protonen en neutronen. Een instabiele kern probeert stabiliteit te bereiken door deeltjes uit te zenden, wat leidt tot radioactief verval. Dit proces gaat gepaard met de vrijgave van energie, die schadelijk kan zijn voor levende wezens en materialen.
Activiteit
De activiteit van een radioactieve stof geeft aan hoeveel atoomkernen er per seconde vervallen. De eenheid van activiteit is de becquerel (Bq), genoemd naar de wetenschapper die het fenomeen ontdekte. Eén becquerel komt overeen met één verval per seconde.
Hoe meet je activiteit?
Een geigerteller is een apparaat dat de activiteit van een radioactieve stof meet. Het telt het aantal deeltjes dat vervalt en geeft dit weer met hoorbare tikjes. Hoe vaker de geigerteller tikt, hoe hoger de activiteit en hoe gevaarlijker de omgeving.
Halveringstijd en berekeningen
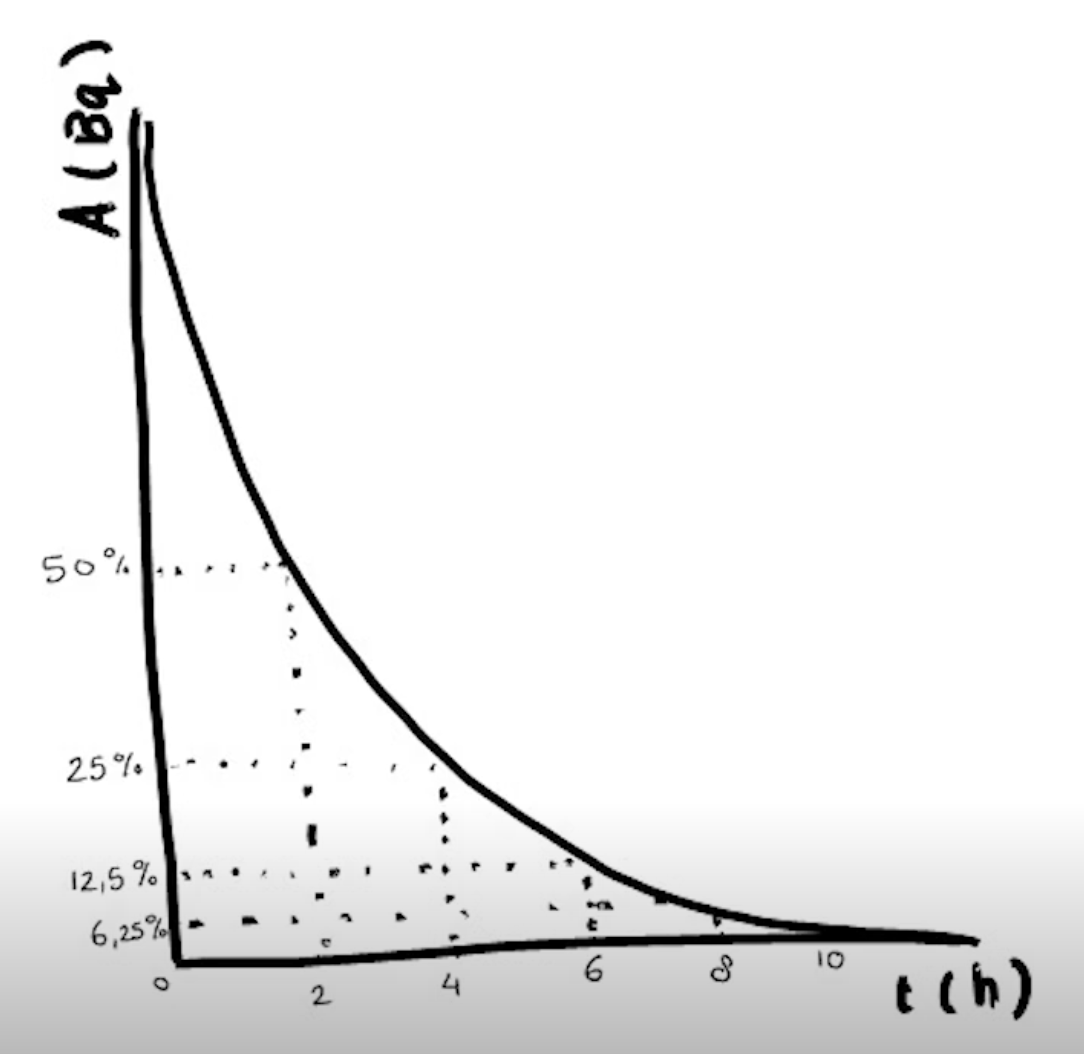
De halveringstijd van een radioactieve stof is de tijd die nodig is om de helft van de oorspronkelijke hoeveelheid radioactieve kernen te laten vervallen. Dit betekent ook dat de activiteit en de straling na één halveringstijd zijn gehalveerd. De halveringstijd is uniek voor elke stof en kan variëren van seconden tot duizenden jaren.
Rekenvoorbeeld: jood-131
Laten we een voorbeeld bekijken met jood-131, dat een halveringstijd van acht dagen heeft. Stel dat de initiële activiteitmegabecquerel is. We willen de activiteit nadagen berekenen.
Gegeven: initiële activiteit=92\operatorname{MBq}=92\operatorname{mMBq}=92\operatorname{mMBqm}=92\operatorname{mMBm}=92\operatorname{mMm}=92\operatorname{mMGm}=92\operatorname{mMG1m}=92\operatorname{mMGm}=92\operatorname{mMm}=92\operatorname{mm}=92m=92=9=92=92M=92MB, halveringstijddagen
Gevraagd: activiteit nadagen
Oplossing: gebruik een tabel om de activiteit na elke halveringstijd te berekenen
Tijd (dagen) | Activiteit\left(\operatorname{MBq}\right)\left(\operatorname{mMBq}\right)\left(\operatorname{mMBqm}\right)\left(\right)\left(\operatorname{mMBqm}\right)\left(\operatorname{mMBqm}\right)\left(\operatorname{mMBm}\right)\left(\operatorname{mMm}\right)\left(\operatorname{mm}\right)\left(m\right)\left(\right)MMB |
|---|---|
11{,}5115 | |
5{,}75575 | |
2{,}8752875 | |
1{,}43751{,}4371{,}431{,}4381438 |
Nadagen is de activiteit van jood-131 gedaald tot ongeveer1{,}438\operatorname{MBq}1{,}438\operatorname{mMBq}1{,}438\operatorname{mMBqm}1{,}438\operatorname{mMBm}1{,}438\operatorname{mMm}1{,}438\operatorname{mm}1{,}438m1{,}43814381.4381.438M1.438MB.
Toepassing: Tsjernobyl
De kernramp in Tsjernobyl in 1986 heeft geleid tot een enorme hoeveelheid radioactieve straling. Hoewel de straling in de loop van de tijd afneemt door het proces van halveringstijd, kan het duizenden jaren duren voordat het gebied volledig veilig is. Dit komt doordat sommige radioactieve stoffen zeer lange halveringstijden hebben en er veel radioactieve stof is vrijgekomen.














