Wat is het verschil tussen indampen en destilleren?
Leerdoelen
•Je kunt uitleggen hoe je een vaste stof uit een oplossing kunt halen door de vloeistof te verdampen.
•Je kunt het verband uitleggen tussen de oplosbaarheid en de temperatuur van zowel een gas als een vaste stof in een vloeistof.
•Je kunt uitleggen hoe je een vloeistofmengsel kunt scheiden in zuivere stoffen door gebruik te maken van het verschil in kookpunt.
Indampen
Indampen is een proces waarbij een vloeistof uit een oplossing wordt verwijderd door verdamping. Dit wordt gedaan om de vaste stof die in de vloeistof is opgelost te verkrijgen. Bijvoorbeeld, als je een oplossing van water met zout hebt, zal het water bijverdampen, terwijl het zout achterblijft.

Voorbeeld van indampen
Een bekend voorbeeld van indampen is het proces dat zich voordoet aan de stranden in Marokko, waar zeewater wordt verdampt om zout te winnen. Dit gebeurt door het zeewater in bakken te laten staan en de zon zijn werk te laten doen. Na enige tijd verdampt al het water en blijft er zout achter op de bodem van de bakken.
Oplosbaarheid
Oplosbaarheid is het maximum aantal gram van een stof dat in een liter oplossing kan worden opgelost. Bijvoorbeeld, de oplosbaarheid van zout in water is een belangrijk concept om te begrijpen. Wanneer je meer zout toevoegt dan de oplosbaarheid toelaat, ontstaat een verzadigde oplossing. Dit betekent dat er zout op de bodem zal liggen, omdat het niet meer kan oplossen.
Oplosbaarheid van vaste stoffen versus gassen
De oplosbaarheid van stoffen wordt beïnvloed door temperatuur. Voor vaste stoffen zoals suiker geldt dat de oplosbaarheid toeneemt met een hogere temperatuur. Dit betekent dat je meer suiker in warm water kunt oplossen dan in koud water.
Omgekeerd geldt voor gassen dat hun oplosbaarheid afneemt bij hogere temperaturen. Dit is bijvoorbeeld te zien bij vissen. In de zomer, wanneer het water verwarmd is, kan er minder zuurstof opgelost zijn, waardoor vissen naar het wateroppervlak komen voor lucht.
Destilleren
Destilleren is een scheidingsmethode die gebruikt wordt om een mengsel van vloeistoffen te scheiden. Hierbij maak je gebruik van het verschil in kookpunten van de stoffen die aanwezig zijn in het mengsel. De stof met het laagste kookpunt verdampt eerst en wordt omgezet in gas.
Proces van destilleren
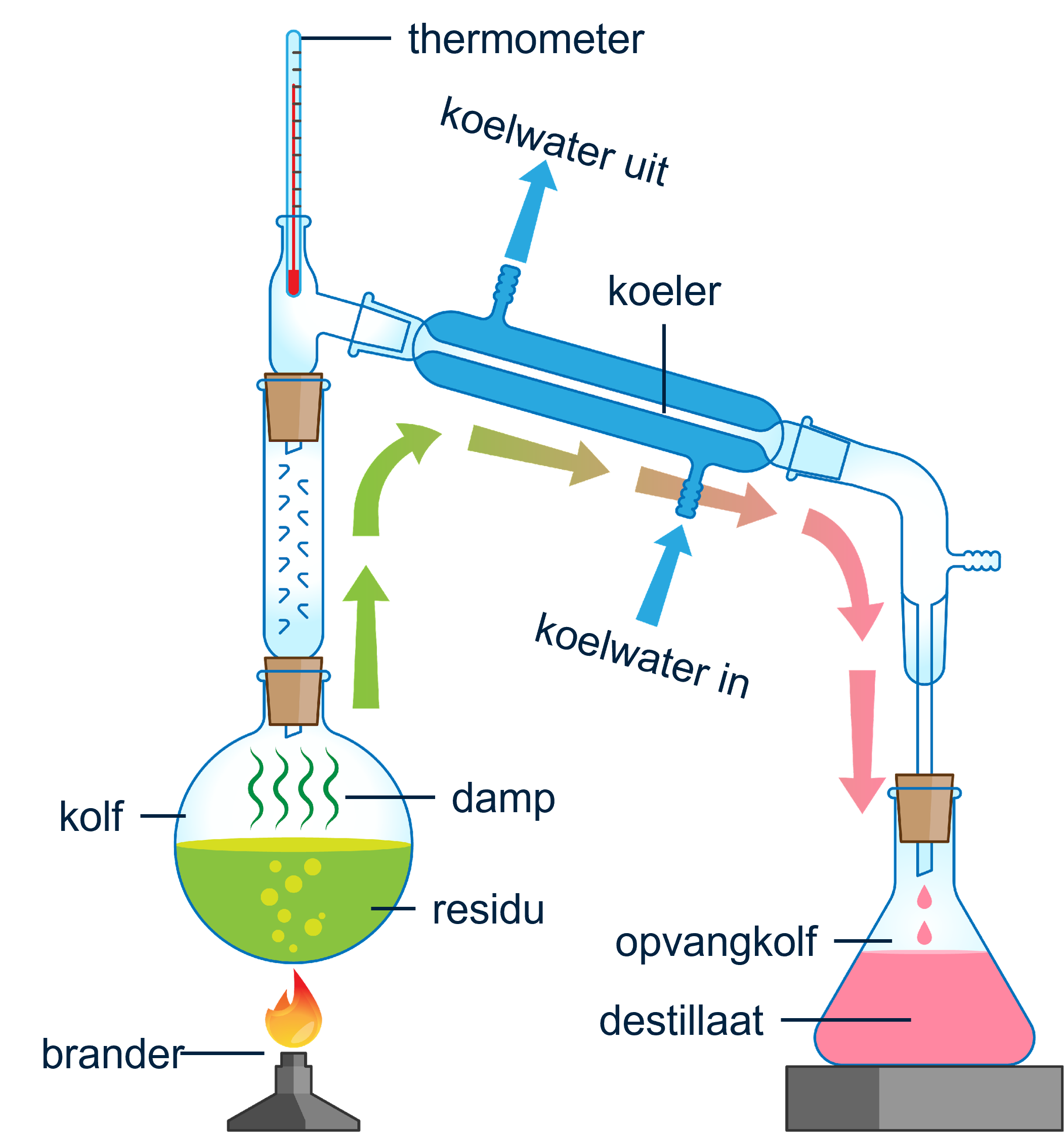
Een destillatieopstelling bestaat uit een kolf met een vloeistof, een thermometer en een koeler. Wanneer de vloeistof wordt verwarmd, verdampt de stof met het laagste kookpunt en stijgt op. Zodra deze stof de thermometer passeert, condenseert deze weer in de koeler en wordt opgevangen als een vloeistof in een opvangkolf. Dit product wordt het destillaat.
De stof die niet verdampt blijft achter in de kolf. Deze overgebleven vloeistof of vaste stof noem je het residu. De koelwateraansluiting is belangrijk voor een goed werkende destillatie: het koelwater stroomt in via het laagste punt van de koeler en verlaat de koeler via het hoogste punt.
Voorbeeld: destilleren van sterke drank
Een bekend voorbeeld van destilleren is het maken van sterke drank, zoals jenever. Dit proces begint met moutwijn, een wijnachtig mengsel dat wordt verhit in een destillatieopstelling. Tijdens het verhitten verdampt de alcohol, omdat die een lager kookpunt heeft dan water. De alcoholdamp condenseert in de koeler en wordt opgevangen in een andere kolf: dit is het destillaat, oftewel de sterke drank. In de oorspronkelijke vloeistof (de moutwijn) blijft voornamelijk water en andere stoffen achter.













