Geef bij de letters A en B aan welke halfreacties plaatsvinden in de halfcel erboven.
Geef bij letter C aan naar welke kant de pijl gewezen moet worden.


 Thijs Brouwer
Thijs BrouwerTest je kennis met de 2 examenvragen die aan dit onderwerp zijn gekoppeld.
Geef bij de letters A en B aan welke halfreacties plaatsvinden in de halfcel erboven.
Geef bij letter C aan naar welke kant de pijl gewezen moet worden.
•Hoe de eerste batterij tot stand kwam
•Wat een elektrode is
•Wat een halfcel is
•Wat een zoutbrug/ elektrolyt is
Het verhaal van de elektrochemische cel begon in 1786 met de Italiaanse genezer Luigi Galvani. Tijdens zijn werk sneed hij in dode kikkers om hun organen en spieren te onderzoeken. Op een dag hing hij de kikkers aan zijn balkon, dat gemaakt was van metaalzink. Terwijl hij zijn koperen mesje vasthield, draaide hij zich om en kwam per ongeluk in aanraking met de kikker. Tot zijn verbazing zag hij de kikker bewegen. Dit leidde hem tot de vraag of doden misschien energie konden hebben.
Alessandro Volta, die in de buurt woonde, hoorde over de opmerkelijke ontdekking van Galvani en besloot zijn eigen experiment te doen. Hij ontwikkelde de zuil van Volta (zie onderstaande afbeelding), die bestaat uit afwisselende koperen en zinken schijfjes met papiertjes tussenin die in een zoutoplossing waren ondergedompeld. Dit resulteerde in de eerste batterij, waarmee hij een lampje kon laten branden.

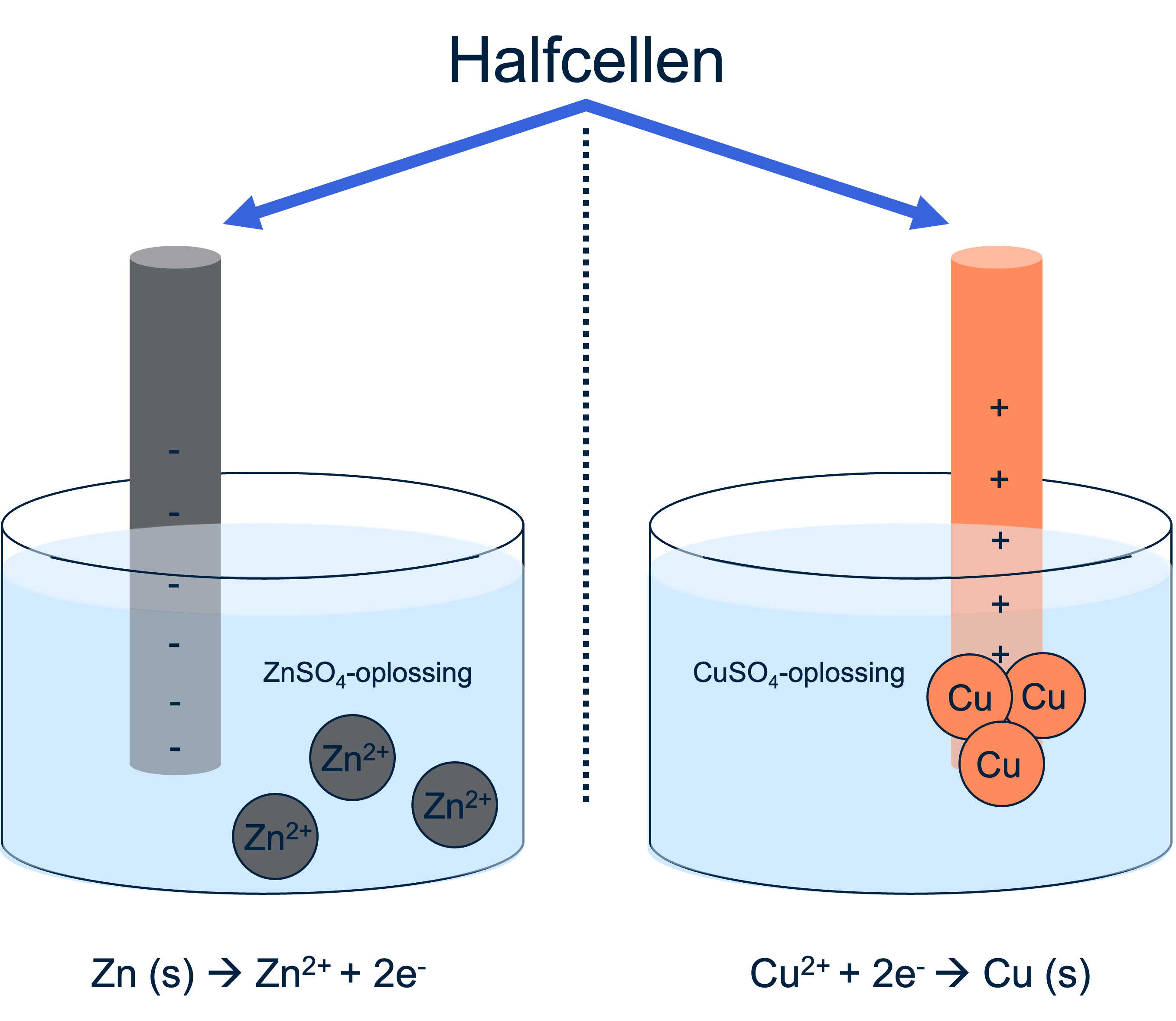
De eerste batterij, ontwikkeld door Volta, bestond uit twee belangrijke componenten:
•Elektroden: De zinken en koperen staafjes die werken als elektroden.
•Halfcellen: De zinksulfaatoplossing met de zinken elektrode en de kopersulfaatoplossing met de koperen elektrode vormen samen een hele cel.
•Reductor: Zink geeft elektronen af en wordt omgezet in zink-ionen (Zn²⁺).
•Oxidator: Koperionen (Cu²⁺) in oplossing nemen elektronen op en worden vaste koperdeeltjes.
De halfreacties zijn als volgt:
Zink: Zn → Zn²⁺ + 2 e⁻ (reductor)
Koper: Cu²⁺ + 2 e⁻ → Cu (oxidator)
De volledige reactie ziet er dan als volgt uit: Zn + Cu²⁺ → Zn²⁺ + Cu
Wat belangrijk is om te onthouden is dat de oxidator altijd reageert aan de pluspool en de reductor altijd reageert aan de minpool. De reductor staat elektronen af en de oxidator neemt ze op.
Een ander belangrijk component in een elektrochemische cel is de zoutbrug, die bestaat uit een oplossing zoals kaliumchloride (KCl). Deze brug zorgt ervoor dat de ladingbalans behouden blijft. Wanneer elektronen van de zinkelektrode naar de koperelektrode bewegen, verplaatst een ion uit de zoutbrug (bijvoorbeeld Cl⁻) naar de zijde die positiever wordt. Dit voorkomt dat de cel stopt met werken.
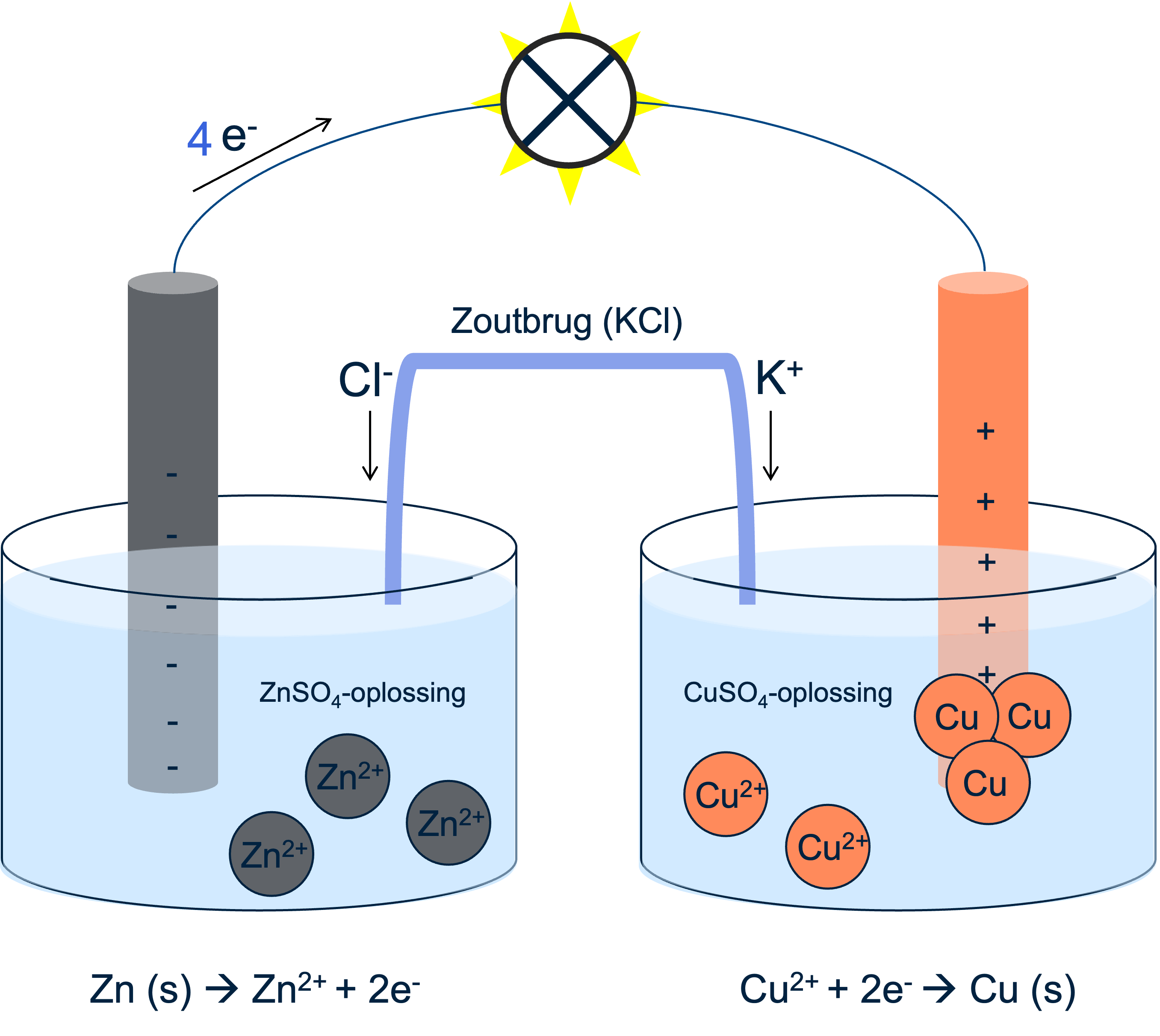
In de afbeelding hierboven zie je ook dat er een lampje is gaan branden en dit komt dus door de elektrochemische batterij. Elektronen komen vanuit de negatieve zinkelektrode en bewegen richting de positieve koperelektrode. Deze bewegende elektronen wekken een stroom op die er dus voor zorgt dat het lampje gaat branden!
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







