Wat zijn isotopen?
Leerdoelen
•Je kunt uitleggen wat isotopen zijn
•Je kunt uitleggen wat radioactiviteit is
•Je kunt uitleggen waarom sommige atomen radioactief zijn
•Je kunt uitleggen wat activiteit is
•Je kunt met halveringstijd rekenen
Isotopen
Je weet waarschijnlijk al wat een atoom is. Maar wist je dat er verschillende versies van hetzelfde atoom kunnen bestaan? Deze versies noemen we isotopen.
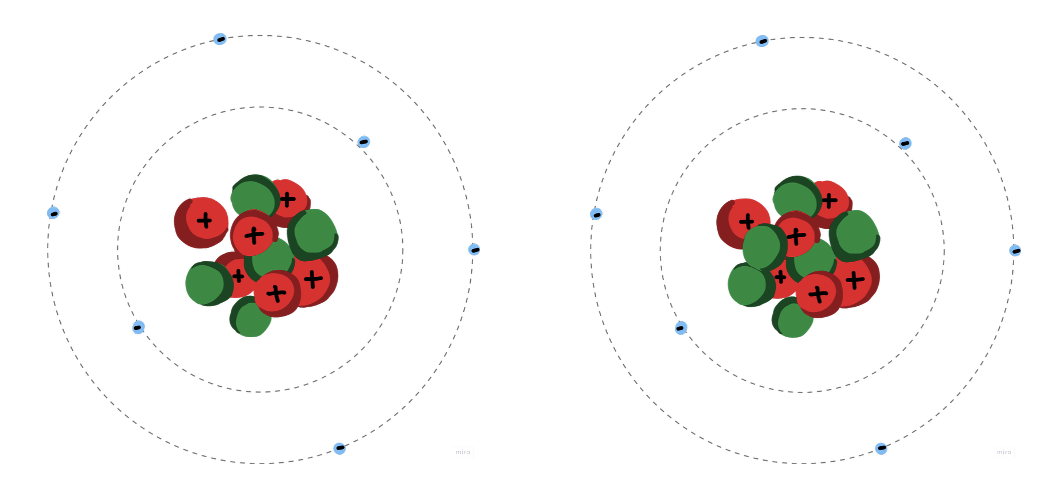
Kijk naar de afbeelding hierboven. Je ziet twee atomen. Ze zijn allebei koolstof, wat betekent dat ze allebei 6 protonen hebben. Het aantal protonen bepaalt namelijk welk element het is. Maar er is een verschil: het ene koolstofatoom heeft 5 neutronen (koolstof-5), en het andere heeft er 6 (koolstof-6).
•Protonen zijn de positief geladen deeltjes in de kern van een atoom.
•Neutronen zijn de neutraal geladen deeltjes in de kern van een atoom.
Het massagetal van een atoom is het totale aantal deeltjes in de kern (protonen + neutronen). Het koolstofatoom met 5 neutronen heeft dus een massagetal van 11 (6 + 5), en het koolstofatoom met 6 neutronen heeft een massagetal van 12 (6 + 6). Ondanks dat ze allebei koolstof zijn, zijn het verschillende isotopen.
Radioactiviteit
Niet alle isotopen zijn hetzelfde. Sommige zijn radioactief. Een radioactief isotoop is een atoom dat instabiel is. Dit komt doordat er te veel of te weinig neutronen in de kern zitten. De kern wil stabieler worden en doet dit door een deeltje weg te schieten.
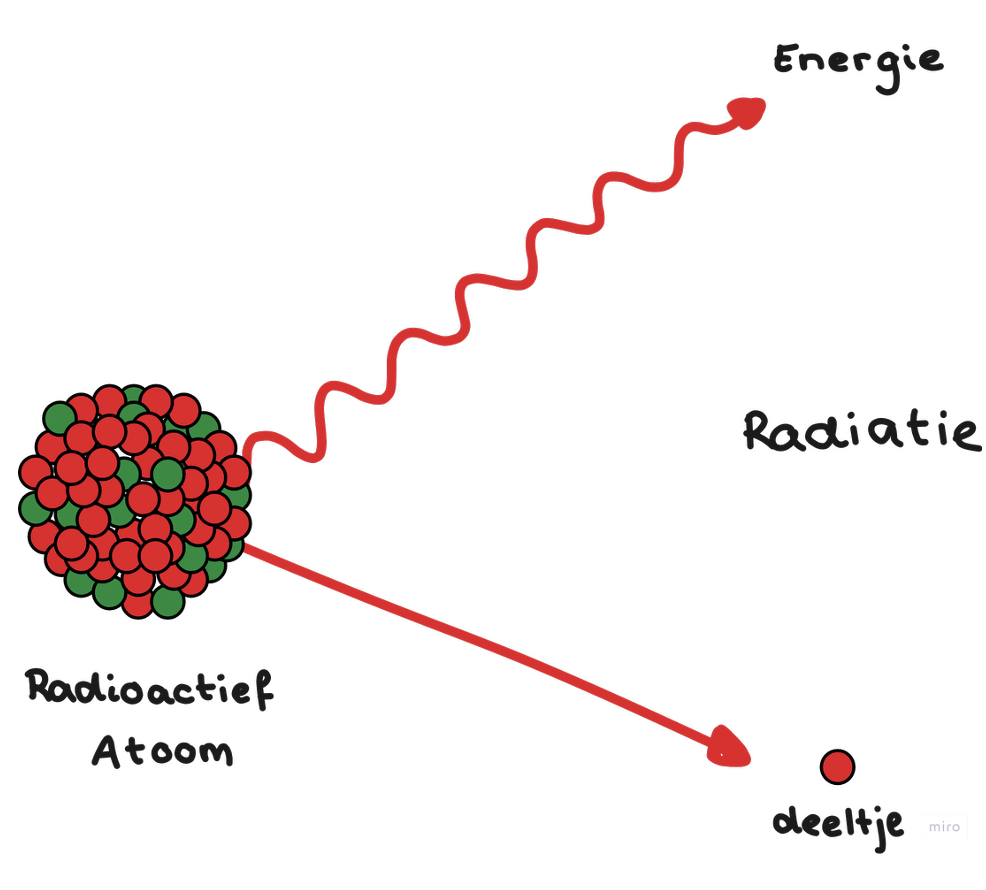
Wanneer een radioactief atoom een deeltje wegschiet, komt er veel energie vrij. Deze energie kan andere stoffen ioniseren, op dat moment botst straling met hoge energie op materie waardoor de materie kapot maakt. Denk aan je huid, maar ook aan andere materialen. Niet alle straling is even gevaarlijk. Hoe hoger de energie, hoe gevaarlijker de straling.
Activiteit
Activiteit geeft aan hoeveel atoomkernen er per seconde vervallen. De eenheid van activiteit is Becquerel (Bq). 1 Becquerel betekent dat er 1 atoomkern per seconde vervalt.
Je kunt de activiteit meten met een Geigerteller. Een Geiger teller tikt elke keer dat er een atoomkern vervalt. Hoe vaker de Geigerteller tikt, hoe hoger de activiteit en hoe gevaarlijker het is.
Halveringstijd
De halveringstijd is de tijd die nodig is voordat de helft van de radioactieve atomen in een stof is vervallen. Na één halveringstijd is de helft van de oorspronkelijke hoeveelheid radioactieve stof verdwenen. Na nog een halveringstijd is weer de helft van wat er over was verdwenen, enzovoort. Overigens wordt na het verstrijken van de halveringstijd ook de activiteit gehalveerd.
Elke radioactieve stof heeft zijn eigen halveringstijd. Sommige stoffen hebben een halveringstijd van seconden, andere van jaren, en weer andere van duizenden jaren.
Rekenvoorbeeld: Halveringstijd
Voorbeeld: Jood-131 heeft een halveringstijd van 8 dagen. De initiële activiteit is 92 megabecquerel. Bereken de activiteit na 48 dagen.
•Gegeven: Beginactiviteit = 92 MBq, Halveringstijd = 8 dagen.
Berekening:Na 8 dagen: 92 MBq / 2 = 46 MBqNa 16 dagen: 46 MBq / 2 = 23 MBqNa 24 dagen: 23 MBq / 2 = 11,5 MBqNa 32 dagen: 11,5 MBq / 2 = 5,75 MBqNa 40 dagen: 5,75 MBq / 2 = 2,875 MBqNa 48 dagen: 2,875 MBq / 2 = 1,438 MBq














