Schrijf het reactieschema op voor deze verbranding. Geef ook de toestandsaanduidingen.
Leerdoelen
•Je kunt een chemische reactie in een reactieschema weergeven met de juiste toestandsaanduiding.
•Je kunt een aantal molecuulformules reproduceren op basis van stofnaam.
•Je kunt een reactieschema omzetten naar een reactievergelijking.
•Je kunt een reactievergelijking kloppend maken door de juiste coëfficiënten te kiezen.
Wat zijn reactieschema's en reactievergelijkingen?
Een reactieschema is een verkorte manier om een chemische reactie weer te geven. In een reactieschema staan de beginstoffen aan de linkerkant van een pijl en de reactieproducten aan de rechterkant. Bij elk stof moet tussen haakjes ook een toestandsaanduiding worden toegevoegd. De toestandsaanduidingen zijn:
•g voor (gas).
•l voor vloeistof (liquid).
•s voor vaste stof (solid).
•aq voor opgeloste stoffen (aqueous).
Voorbeeld van een reactieschema
Bij de reactie tussen waterstof en zuurstof ontstaat water. Het reactieschema zou er als volgt uitzien:
Reactieschema:
waterstof (g) + zuurstof (g) → water (l)
Hierbij zijn waterstof (H2) en zuurstof (O2) de beginstoffen in gas vorm en water (H₂O) het reactieproduct in vloeibare vorm.
Molecuulformules
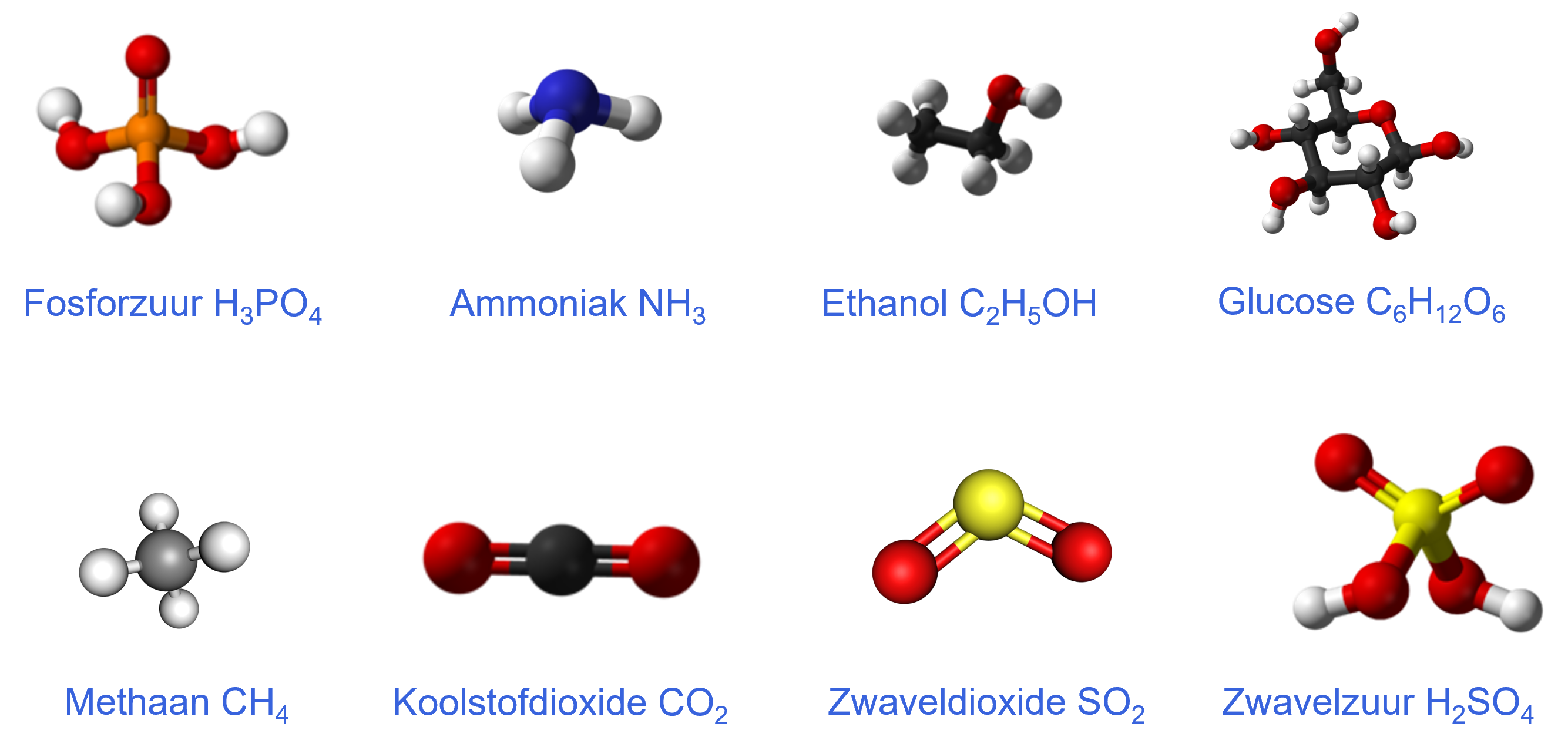
Voor het omzetten van een reactieschema naar een reactievergelijking is het belangrijk dat je enkele molecuulformules kent. Hier zijn enkele voorbeelden die je uit je hoofd moet leren:
•Fosforzuur: H3PO4
•Ammoniak: NH3
•Ethanol: C2H5OH
•Glucose: C6H12O6
•Methaan: CH4
•Koolstofdioxide: CO2
•Zwaveldioxide: SO2
•Zwavelzuur: H2SO4
Wat is de index?
In molecuulformules komt een index voor, die het aantal atomen van een bepaald element aangeeft. Het getal staat rechts van het element. Bijvoorbeeld, in H3PO4 betekent de index 3 dat er drie waterstofatomen zijn, 1 fosforatoom (P) en 4 zuurstofatomen (O).
Twee-atomige elementen
Er zijn zeven twee-atomige elementen in de chemie. Deze elementen komen nooit alleen voor en vormen altijd een paar:
•Cl2 (chloor)
•F2 (fluor)
•N2 (stikstof)
•H2 (waterstof)
•O2 (zuurstof)
•I2 (jood)
•Br2 (broom)
Het omzetten naar reactievergelijkingen
Om een reactieschema om te zetten naar een reactievergelijking, moet je weten wat de symbolen zijn van de stoffen. Neem bijvoorbeeld de verbranding van koolstof. Er ontstaat koolstofdioxide uit de verbranding van koolstof. Hieruit volgt:
Reactieschema:
koolstof(s) + zuurstof(g) → koolstofdioxide(g)
Reactievergelijking:
C(s) + O2(g) → CO₂(g)
Hierbij zijn de toestandsaanduidingen van belang. Koolstof is een vaste stof (s) en zuurstof is een gas (g).
Kloppende reactievergelijkingen
Volgens de wet van Lavoisier gaat massa niet verloren. Dit betekent dat het aantal atomen van elke stof aan de linkerkant van de pijl gelijk moet zijn aan dat aan de rechterkant. Bij het kloppend maken van een reactievergelijking mag je de index van de moleculen niet veranderen, maar je kunt wel de coëfficiënt aanpassen.
Voorbeeld: Verbranding van waterstof
De reactievergelijking voor de verbranding van waterstof ziet er als volgt uit:
Reactievergelijking:
2H2(g) + O2(g) → 2H2O(g)
Hier heb je ervoor gezorgd dat het aantal atomen waterstof en zuurstof links en rechts van de pijl gelijk is.
Praktische voorbeelden
Verbranding van methaangas:
Reactievergelijking:
CH4(g) + O2(g) → CO₂(g) + H₂O(l)
Coëfficiënten toevoegen om kloppend te maken:
CH4(g) + 2O2(g) → CO₂(g) + 2H2O(l)
Kalium en broom:
Reactievergelijking: K(s)+ Br2(l) → KBr(s)
Coëfficiënten toevoegen om kloppend te maken: 2K(s)+ Br2(l) → 2KBr(s)
Extra zuurstof in lucifers
In de vorige video werd het idee besproken dat er in lucifers extra zuurstof vrijkomt om het houtje te laten branden. Dit gebeurt doordat kaliumchloraat ontleedt in kaliumchloride (KCl) en zuurstof (O2). Hierdoor komt er extra zuurstof vrij om de verbranding te ondersteunen.













