Wat is de juiste naam voor de verbinding NO₂?
Moleculaire stoffen: naamgeving en atoombindingen
Naamgeving van moleculaire stoffen
Bij het benoemen van moleculaire stoffen gebruiken we voorvoegsels om het aantal atomen van elk element in de formule aan te geven. Deze voorvoegsels zijn belangrijk om de juiste naam te geven aan de verbindingen.
Voorvoegsel | Betekenis |
|---|---|
Mono | 1 (wordt weggelaten bij het eerste element) |
Di | 2 |
Tri | 3 |
Tetra | 4 |
Penta | 5 |
Hexa | 6 |
Hepta | 7 |
Octa | 8 |
Voorbeelden:
•NO is stikstofmonooxide (één stikstof, één zuurstof).
•NO₂ is stikstofdioxide (één stikstof, twee zuurstoffen).
•P₂O₃ is difosfortrioxide (twee fosfor, drie zuurstoffen).
Atoombinding en covalentie
De atoombinding, ook wel de covalente binding genoemd, is de binding die voorkomt in moleculaire stoffen. Atomen streven naar een edelgaskonfiguratie, waarbij ze een volle buitenste schil van elektronen hebben. Dit bereiken ze door elektronen te delen.
Voorbeeld: waterstof en water
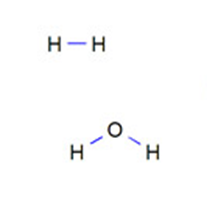
•Waterstof (H₂): Twee waterstofatomen delen elk één elektron om een volle schil te bereiken. Dit vormt een enkele atoombinding.
•Water (H₂O): Zuurstof heeft zes elektronen in de buitenste schil en deelt twee elektronen met twee waterstofatomen om een volle schil te bereiken. Dit resulteert in twee atoombindingen.
Covalentie en structuurformules
Covalentie is het aantal bindingen dat een atoom kan vormen. Dit is afhankelijk van het aantal elektronen dat het atoom nodig heeft om een volle schil te bereiken.
Element | Covalenties |
|---|---|
Waterstof | Covalentie van 1 |
Zuurstof | Covalentie van 2 |
Stikstof | Covalentie van 3 |
Koolstof | Covalentie van 4 |
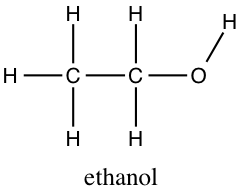
Bij het tekenen van structuurformules is het belangrijk om de covalentie van elk element in acht te nemen. Bijvoorbeeld, in C₂H₆O moet koolstof vier bindingen vormen, waterstof één, en zuurstof twee.
Waarom breken atoombindingen?
Atoombindingen zijn sterk en worden niet zomaar verbroken. Ze breken alleen tijdens een chemische reactie, waarbij atomen opnieuw worden gerangschikt om nieuwe moleculen te vormen. Tijdens faseovergangen worden alleen de zwakkere Van der Waalskrachten verbroken.
Sneeuwkristallen en symmetrie
Sneeuwkristallen zijn een prachtig voorbeeld van de diversiteit van moleculaire structuren. Ze vormen zich in verschillende vormen door variaties in luchtdruk en temperatuur. De symmetrie van sneeuwkristallen, vaak met een zesvoudige as, is een gevolg van de manier waarop watermoleculen zich rangschikken in een kristalrooster.













