Wat is de molariteit van calciumchloride?
Leerdoelen
•Je kunt de concentratie van een oplossing aangeven en ermee rekenen.
•Je kunt de symbolen en eenheden van molariteit benoemen.
•Je kunt uitleggen hoe coëfficiënten in een oplosvergelijking de molverhouding van ionen weergeven.
Wat is molariteit?
In de scheikunde is molariteit een maat voor de concentratie van opgeloste stof in een oplossing. Het wordt aangeduid met het symbool M en gemeten in mol per liter (mol/L ofmol \cdot L^{-1}). Deze notaties wijzen allemaal op hetzelfde: de hoeveelheid opgeloste stof per liter oplossing. Het is belangrijk om deze hoofdletter M niet te verwarren met de molaire massa, die de massa van een mol stof in grammen aangeeft. Hoewel dit verwarrend kan zijn, is dit de standaardnotatie.
Formule voor molariteit
De basisvergelijking voor molariteit is:

Voorbeeld:
Als je 20 gram keukenzout (NaCl) oplost in 500 milliliter water, zou je de molariteit als volgt berekenen:
1.Bepaal eerst het aantal mol NaCl door 20 gram te delen door de molaire massa van NaCl (58,443 g/mol).
2.Deel vervolgens het aantal mol door het volume oplossing in liter (0,5 L).
3.Het resultaat is de molariteit van de NaCl-oplossing, uitgedrukt in.

Molverhoudingen in oplossing
Bij het oplossen van een zout gebruik je de oplosvergelijking om de molverhouding tussen het vaste zout en de gevormde ionen af te lezen. Dit doe je door eerst de verhoudingsformule op te stellen en vervolgens naar de coëfficiënten in de oplosvergelijking te kijken:
Uit deze vergelijking lees je de verhouding 1:1:1 af.
Voor een ander zout, zoals natriumfosfaat, geldt:
Na_3PO_4(s)\rightarrow3Na^{+}(aq)+PO_4^{3-}(aq)
Hier is de verhouding 1:3:1, waardoor een oplossing van 0,3 molairNa_3PO_4Na_3PO_{\placeholder{}}Na_3PONa_3PO4Na_{\placeholder{}}PO4NaPO4leidt tot 0,9 molairNa^{+}Na^{\placeholder{}}en 0,3 molairPO_4^{3-}PO_4^{3-}PO_4^3PO_4^{3-}PO_4^{3--}PO_4^{3-}PO_4^3PO_4^{\placeholder{}}PO_4PO_{\placeholder{}}.
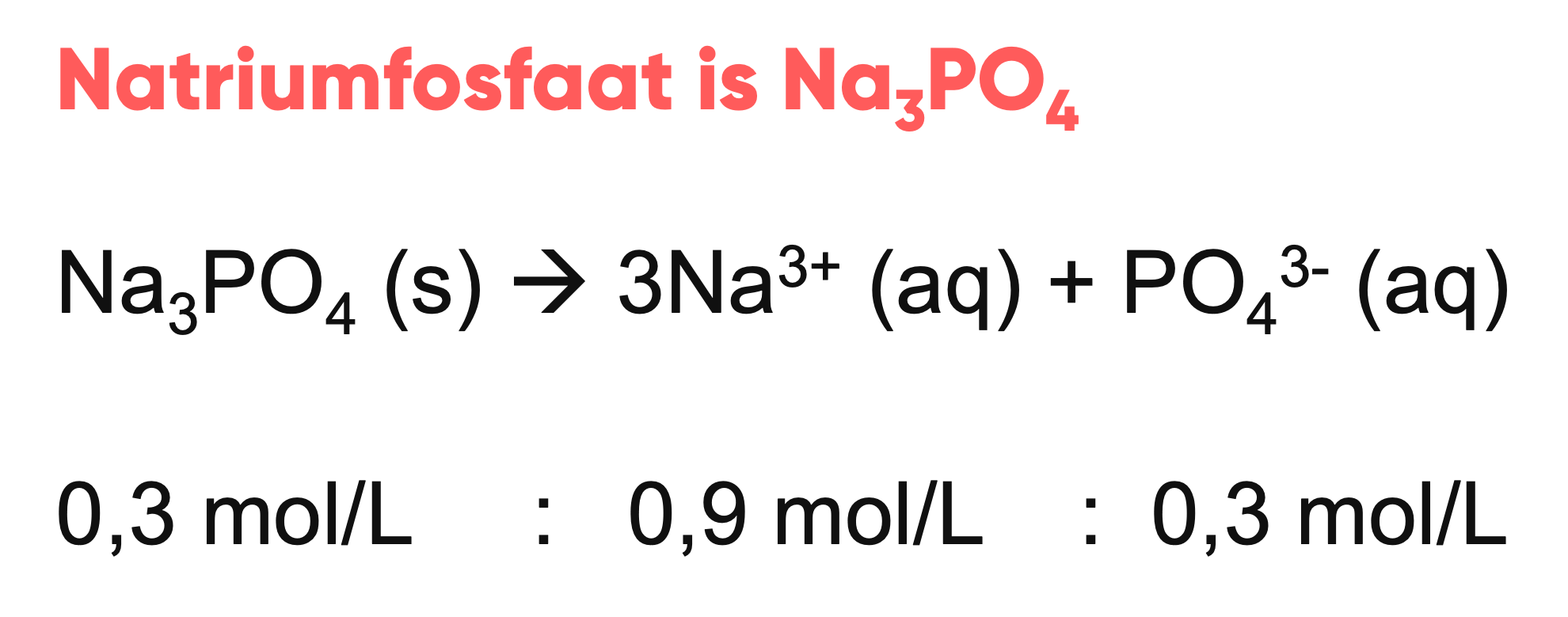
Berekeningen met molariteit
De molariteit van een oplossing is het aantal mol opgeloste stof per liter oplossing:met in mol enin liter. Daarnaast gebruiken we om van gram naar mol te gaan:waarbijde massa in gram is en M de molaire massa.
VoorbeeldAlCl_3AlCl_{\placeholder{}}
25g aluminiumchloride wordt opgelost tot een volume van 2,0L:
1. Molaire massa bepalen
M(AlCl_3)=133{,}34~g\cdot mol^{-1}M(AlCl_3)=133{,}34~g\cdot mol^{-1}(AlCl_3)=133{,}34~g\cdot mol^{-1}M(AlCl_3)=133{,}34~g\cdot mol^{-1}M_{}(AlCl_3)=133{,}34~g\cdot mol^{-1}M_{r}(AlCl_3)=133{,}34~g\cdot mol^{-1}M_{r}(AlCl_3)=13334~g\cdot mol^{-1}M_{r}(AlCl_3)=133.34~g\cdot mol^{-1}M_{r}(AlCl_3)=133.34~gmol^{-1}M_{r}(AlCl_3)=133.34~\frac{g}{}mol^{-1}M_{r}(AlCl_3)=133.34~\frac{g}{=}mol^{-1}M_{r}(AlCl_3)=133.34~\frac{g}{\placeholder{}}mol^{-1}M_{r}(AlCl_3)=133.34~gmol^{-1}M_{r}(AlCl_3)=133.34~gmol^{-1}M_{r}(AlCl_3)=133.34~gmol^{-1}M_{r}(AlCl_3)=133.34~gmol^{-1}
2. Aantal mol
n(AlCl_3)=\frac{m}{M_{}}=\frac{25}{133{,}34}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{133{,}34}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{13334}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{133.34}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{13334}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{133.34}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{13334}n(AlCl_3)=\frac{m}{M_{r}}=\frac{25}{133.34}n(AlCl_3)=\frac{m}{M_{r}}\frac{25}{133.34}n(AlCl_3)=\frac{m}{M_{r}}\frac{25n}{133.34}n(AlCl_3)=\frac{m}{M_{r}}\frac{25}{133.34}n(AlCl_3)=\frac{m}{M_{\placeholder{}}}\frac{25}{133.34}n(AlCl_3)=\frac{m}{\placeholder{}_{\placeholder{}}}\frac{25}{133.34}n(AlCl_3)=\frac{m}{\placeholder{}}\frac{25}{133.34}n(AlCl_3)=m\frac{25}{133.34}
3. Molariteit van de oplossing
M(AlCl_3)=\frac{n}{V}=\frac{25/133,34\text{ mol}}{2,0\text{ L}}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133,34\text{ mol}}{2,0\text{ L}}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=2\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/1\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/13\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}3\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}34\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}34m\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}34mo\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=25/133{,}34mol\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mM(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~moM(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~molM(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdotM(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdot LM(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdot L^{}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdot L^{-}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0L}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mol}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34mo}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34m}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}=\frac{25/133{,}34}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133{,}34}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/13334}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2{,}0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{20}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2.0}\approx0{,}094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2.0}\approx0094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2.0}\approx0.094~mol\cdot L^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2.0}\approx0.094~molL^{-1}M(AlCl_3)=\frac{n}{V}\frac{25/133.34}{2.0}\approx0.094~mol,L^{-1}M(AlCl_3)=\frac{n}{\placeholder{}}\frac{25/133.34}{2.0}\approx0.094~mol,L^{-1}M(AlCl_3)=\frac{\placeholder{}}{\placeholder{}}\frac{25/133.34}{2.0}\approx0.094~mol,L^{-1}
Dus de oplossing is 0,094
4. Ionenconcentratie in de oplossing
Oplosvergelijking:AlCl_3(s)\rightarrow Al^{3+}(aq)+3Cl^{-}(aq)
De verhouding is 1:1:3, dus:
[Al^{3+}]=0{,}094~mol\cdot L^{-1}[Al^{3+}]=0094~mol\cdot L^{-1}[Al^{3+}]=0.094~mol\cdot L^{-1}[Al^{3+}]=0.094~molL^{-1}[Al^{3+}]=0.094~mol,L^{-1}
[Cl^{-}]=3\times0{,}094=0{,}281~mol\cdot L^{-1}[Cl^{-}]=3\times0{,}094=0281~mol\cdot L^{-1}[Cl^{-}]=3\times0{,}094=0.281~mol\cdot L^{-1}[Cl^{-}]=3\times0094=0.281~mol\cdot L^{-1}[Cl^{-}]=3\times0.094=0.281~mol\cdot L^{-1}[Cl^{-}]=3\times0.094=0.281~molL^{-1}
Voorbeeld
De molariteit vanin een oplossing waarin 3,0gL^{-1}gL^{-}gL^{\placeholder{}}gLgL-NO_3^{-}aanwezig is:
1. Oplosvergelijking en verhouding
Ca(NO_3)_2(s)\rightarrow Ca^{2+}(aq)+2NO_3^{-}(aq)
De verhouding is dus 1:1:2
2. Molaire massa van
M(NO_3^{-})=62~g\cdot mol^{-1}M(NO_3^{-})=62~g\cdot mol^{-1}M_{}(NO_3^{-})=62~g\cdot mol^{-1}M_{r}(NO_3^{-})=62~g\cdot mol^{-1}M_{r}(NO_3^{-})=62~gmol^{-1}
3. Molariteit van
M(NO_3^{-})=\frac{3{,}0}{62}mol\cdot L^{-1}M(NO_3^{-})=\frac{30}{62}mol\cdot L^{-1}M(NO_3^{-})=\frac{3.0}{62}mol\cdot L^{-1}M(NO_3^{-})=\frac{3.0}{62}molL^{-1}M(NO_3^{-})=\frac{3.0}{62}molL^{-}M(NO_3^{-})=\frac{3.0}{62}molL^{\placeholder{}}M(NO_3^{-})=\frac{3.0}{62}molLM(NO_3^{-})=\frac{3.0}{62}molM(NO_3^{-})=\frac{3.0}{62}moM(NO_3^{-})=\frac{3.0}{62}molM(NO_3^{-})=\frac{3.0}{62}moM(NO_3^{-})=\frac{3.0}{62}m
4. Molariteit van
Omdat per moltwee molontstaan, is de molariteit van{Ca(NO_3)_2}{Ca(NO_3)_2}\cdotde helft van die van:
M(Ca(NO_3)_2)=\frac{1}{2}M(NO_3^{-})=0{,}024~mol\cdot L^{-1}M(Ca(NO_3)_2)=\frac{1}{2}M(NO_3^{-})=0024~mol\cdot L^{-1}M(Ca(NO_3)_2)=\frac{1}{2}M(NO_3^{-})=0.024~mol\cdot L^{-1}M(Ca(NO_3)_2)=\frac{1}{2}M(NO_3^{-})=0.024~molL^{-1}
De molariteit van de oplossing is dus0{,}0240{,}024~0{,}024~mol\cdot L^{-1}{Ca(NO_3)_2}0{,}024~mol\cdot L^{-1}0024~mol\cdot L^{-1}0.024~mol\cdot L^{-1}













