Vul de woorden in die de juiste beschrijving vormen van de vierde fase bij metalen en legeringen.
Leerdoelen
•Je kunt de eigenschappen van metalen verklaren op micro- en mesoniveau.
•Je kunt de invloed van roosterfouten op de eigenschappen van metalen beschrijven.
Wat is plasma?
Naast de bekende fasen gas, vloeistof en vast, bestaat er nog een vierde toestand van materie: plasma. Plasma ontstaat bij extreem hoge temperaturen, waarbij atomen geïoniseerd raken. Dit betekent dat ze hun elektronen verliezen, waardoor een mengsel ontstaat van positief geladen atoomkernen en vrije elektronen. Plasma komt voor in extreme omstandigheden, zoals in een kernfusiereactor waar de temperaturen gigantisch hoog zijn. Maar het wordt ook dichter bij huis toegepast, bijvoorbeeld bij de fabricage van chipszakken. Het metaallaagje aan de binnenkant van zo'n zak wordt met behulp van plasma opgebracht.
Niveaus van verklaring: macro, meso en micro
Om de eigenschappen van metalen te begrijpen, kijken we naar verschillende niveaus:
•Macroniveau: Dit zijn eigenschappen die je met het blote oog kunt waarnemen. Denk aan het hoge smelt- en kookpunt van wolfraam en tin, materialen die gebruikt worden in reactoren. Je ziet dat een blok metaal stroom geleidt als een lampje gaat branden.
•Mesoniveau: Op dit niveau kijken we naar een klein aantal atomen of ionen, maar nog niet naar één enkel deeltje. Hier kunnen we bijvoorbeeld de sterke metaalbinding verklaren, die zorgt voor hoge smeltpunten. Ook de geleidbaarheid van metalen kan op mesoniveau worden verklaard door de beweging van vrije elektronen door een deel van het rooster.
•Microniveau: Dit is het niveau van individuele atomen en elektronen. Op dit niveau kunnen we de geleidbaarheid verklaren door te kijken hoe één elektron van het ene atoom naar het andere springt en vrij kan bewegen.
Edelheid en standaard elektrodepotentiaal
De edelheid van metalen is een belangrijke eigenschap, vooral bij het ontwerpen van constructies. De edelheid van een metaal hangt samen met de standaard elektrodepotentiaal.
Edelheid | Naam stof | V0 |
|---|---|---|
Edel | goud | +1,50 |
Edel | platina | +1,20 |
Halfedel | kwik | +0,80 |
Halfedel | koper | +0,34 |
Onedel | ijzer | -0,45 |
Onedel | chroom | -0,74 |
Zeer onedel | aluminium | -1,66 |
Zeer onedel | magnesium | -2,37 |
Metalen met een hoge (positieve) standaard elektrodepotentiaal, zoals goud en platina, zijn edele metalen. Ze staan hun elektronen niet gemakkelijk af en zijn daardoor minder gevoelig voor corrosie (roestvorming of oxidatie). Dit is waarom ze vaak worden gebruikt voor juwelen, zoals ringen en oorbellen. Metalen met een lage (negatieve) standaard elektrodepotentiaal, zoals aluminium en magnesium, zijn zeer onedele metalen. Ze staan hun elektronen gemakkelijk af en zijn daardoor zeer corrosiegevoelig.
Bescherming tegen corrosie
Omdat veel metalen in het dagelijks leven worden gebruikt en sommige erg corrosiegevoelig zijn, is het vaak nodig om ze te beschermen. Het is te duur en schaars om alles van goud te maken. Daarom brengen we beschermende lagen aan op goedkopere, corrosiegevoelige materialen. Sommige metalen beschermen zichzelf:
•Chroom: Vormt direct een afsluitend laagje chroomoxide (Cr2O3) aan het oppervlak.
•Aluminium: Vormt een afsluitend laagje aluminiumoxide (Al2O3) aan het oppervlak. Dit laagje voorkomt dat het onderliggende aluminium verder oxideert.
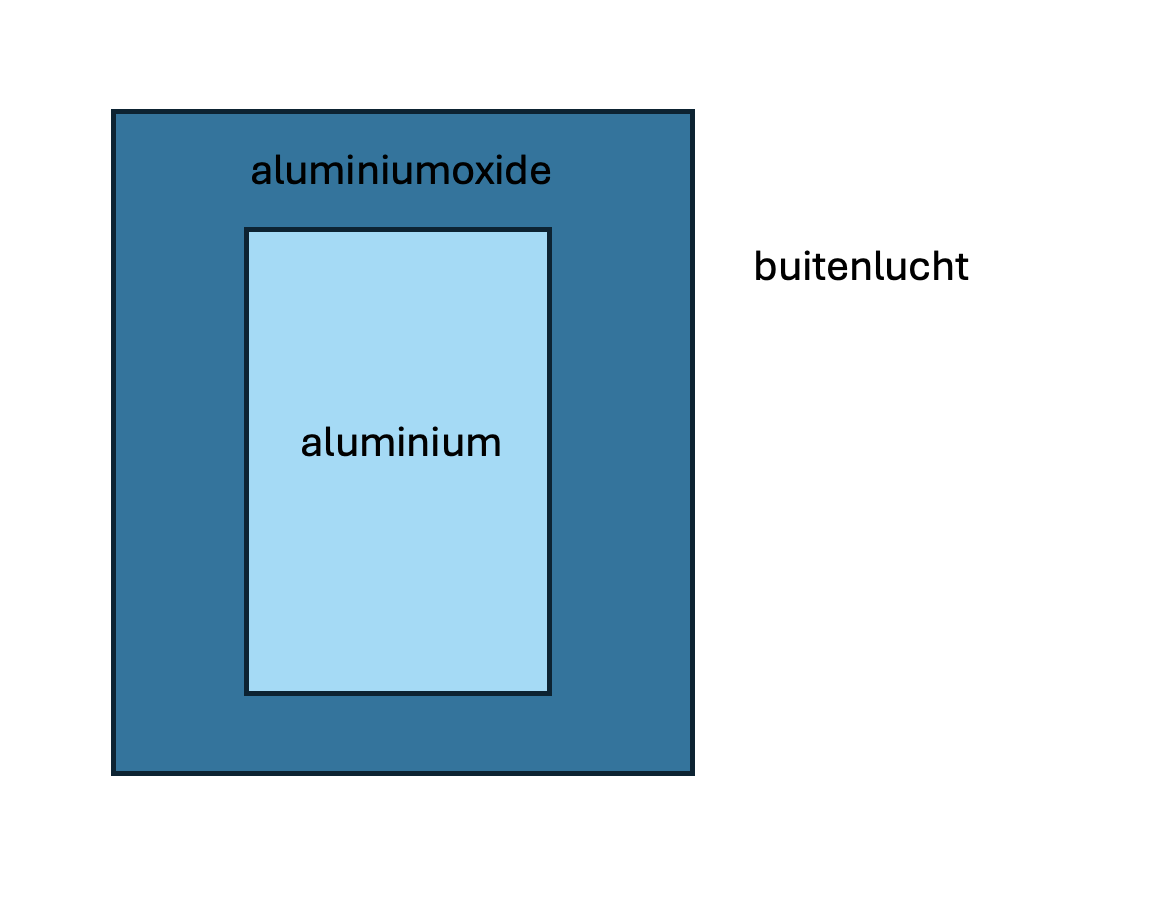
Andere beschermingsmogelijkheden zijn:
•Afdekken met een verflaag: Denk aan verkeersborden, die van staal (corrosiegevoelig) zijn gemaakt en beschermd worden door verf.
•Verzinken: Het materiaal wordt ondergedompeld in een bad met gesmolten zink. Er ontstaat een laagje zink op het oppervlak. Dit zink zal wel oxideren, maar het gevormde zinkoxide (ZnO) vormt een afsluitende laag die het onderliggende materiaal beschermt.
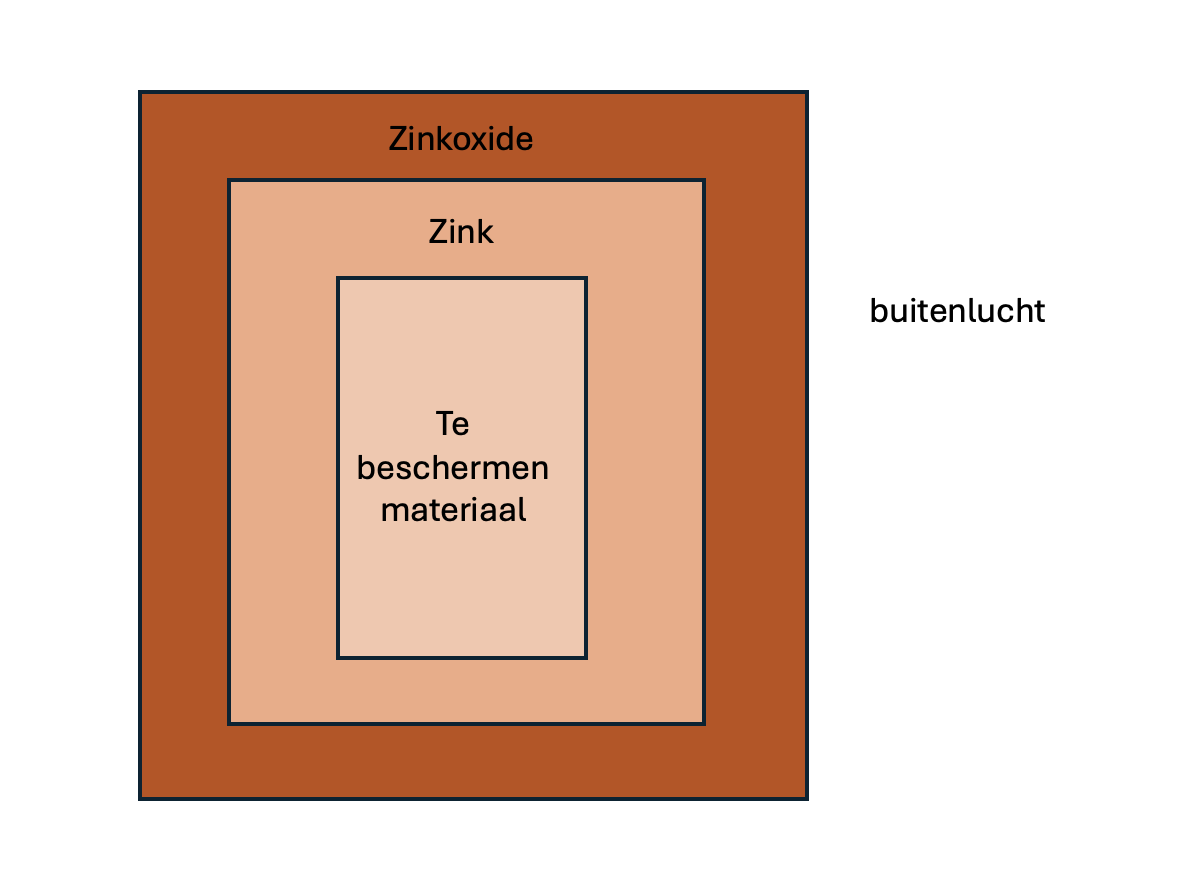
•Poedercoaten: Het materiaal wordt onder potentiaal gezet, waarna poederverf zich door elektrostatische aantrekking gelijkmatig over het oppervlak verspreidt en een mooie, beschermende laag vormt.
De sterke metaalbinding en elektrische geleiding
Metalen bestaan uit een metaalrooster van positief geladen metaalionen, omgeven door een 'zee' van vrij bewegende valentie-elektronen. Deze elektronen zijn niet gebonden aan één specifiek atoom, maar kunnen vrij door het hele rooster bewegen.
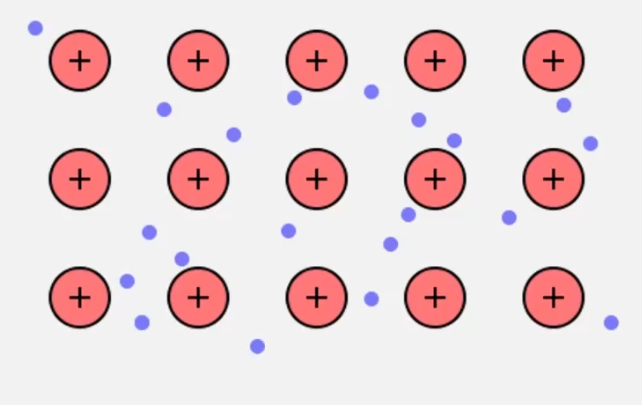
Deze vrije valentie-elektronen zijn verantwoordelijk voor twee belangrijke eigenschappen:
1.Elektrische geleiding: Doordat de elektronen vrij kunnen bewegen, kunnen ze gemakkelijk een elektrische stroom transporteren.
2.Sterke metaalbinding: De positief geladen metaalionen worden bij elkaar gehouden door de negatief geladen elektronen die eromheen bewegen. Deze sterke aantrekkingskracht zorgt voor een zeer sterke metaalbinding. Een direct gevolg van deze sterke metaalbinding is dat metalen over het algemeen zeer hoge smeltpunten hebben. Er is veel energie nodig om de bindingen te verbreken en de ionen uit hun vaste rooster te laten bewegen.
Buigzaamheid van metalen
Metalen zijn vaak buigzaam of vervormbaar. Dit komt doordat de lagen van positief geladen metaalionen in het rooster ten opzichte van elkaar kunnen verschuiven wanneer er voldoende kracht op wordt uitgeoefend. De vrije elektronen bewegen mee en blijven de metaalionen bij elkaar houden, zelfs als de lagen verschuiven.
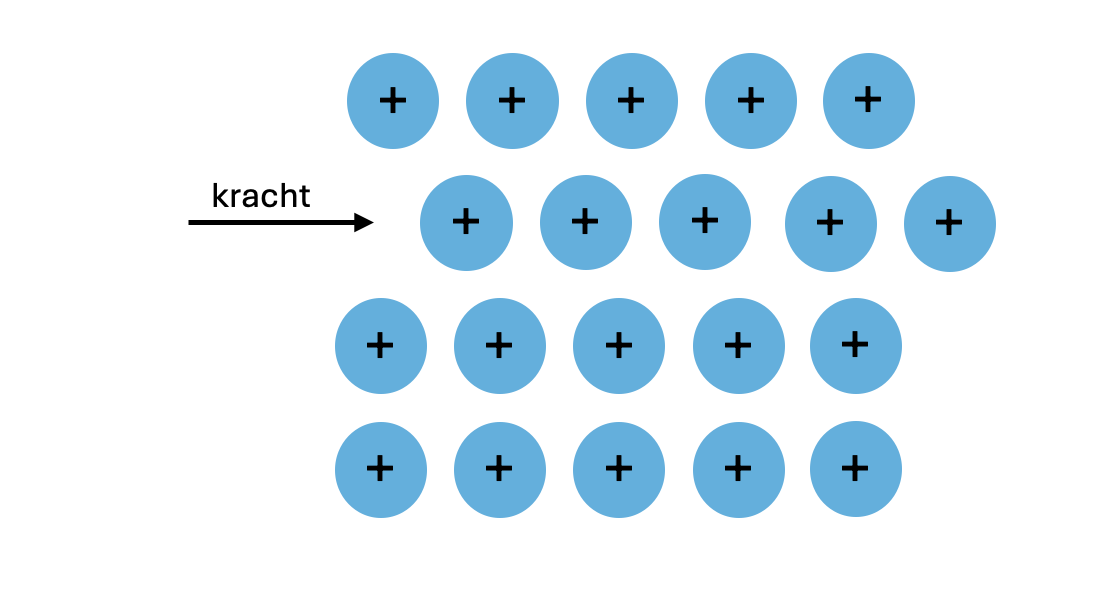
Echter, als je een metaal te vaak of te ver buigt, kan de beweging tussen de kristallen (kleine geordende gebieden in het metaal) moeilijker worden. Er ontstaat weerstand tussen de kristalgrenzen, waardoor het metaal minder buigzaam wordt en uiteindelijk kan breken. Om de buigzaamheid te herstellen, kan een metaal worden gegloeid. Dit is een proces waarbij het metaal wordt verwarmd. Door de warmte smelten sommige kristallen en vloeien ze samen, waardoor de kristalgrenzen verdwijnen en de interne spanningen afnemen. Hierdoor neemt de buigzaamheid van het metaal weer toe.
Legeringen
Zuivere metalen zijn vaak relatief zacht, omdat de lagen van metaalionen gemakkelijk over elkaar heen kunnen schuiven. Om metalen harder en sterker te maken, worden vaak legeringen gemaakt. Een legering is een mengsel van twee of meer metalen, of een metaal met een niet-metaal. Een bekend voorbeeld is brons, een legering van koper en tin. Door een ander metaal (of element) toe te voegen, ontstaan er roosterfouten in het metaalrooster. Deze vreemde atomen kunnen kleiner of groter zijn dan de oorspronkelijke metaalatomen.
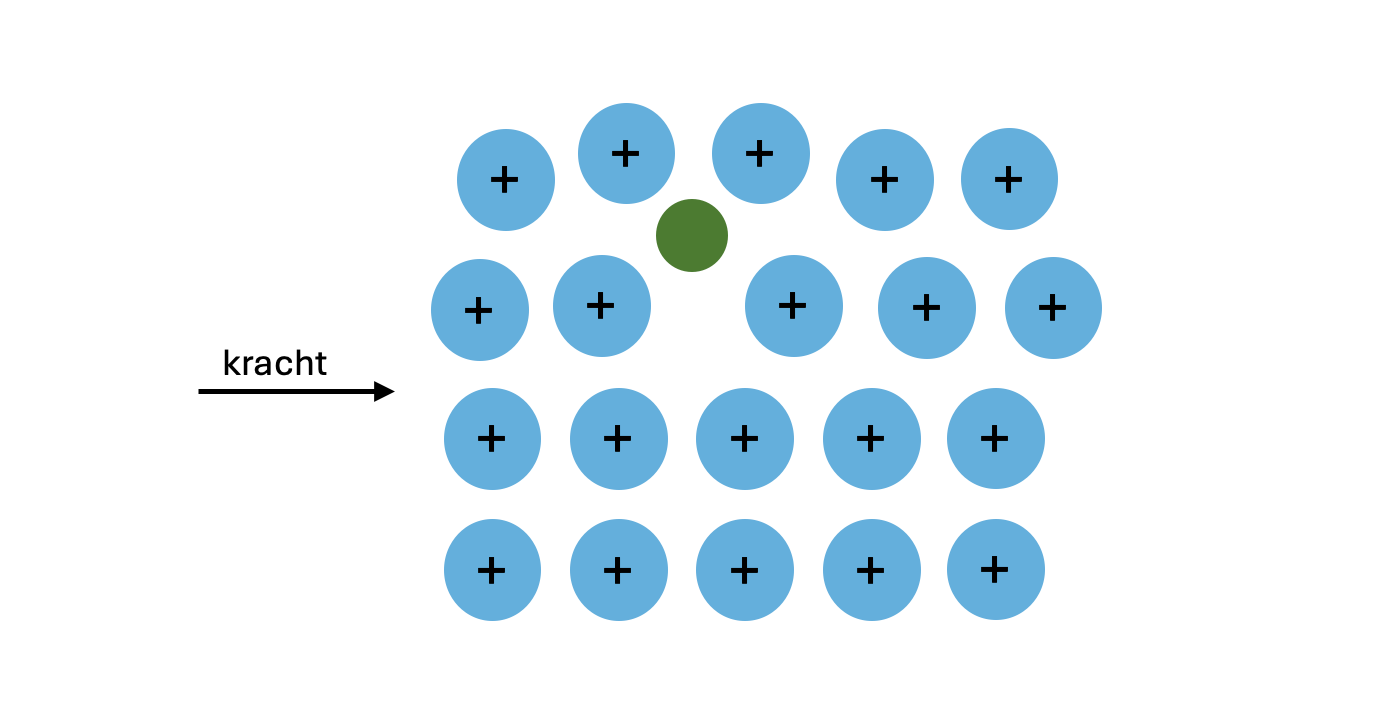
Wanneer een kracht wordt uitgeoefend op een legering, botsen de verschuivende lagen tegen deze ingebouwde vreemde atomen. Dit belemmert het gemakkelijk verschuiven van de lagen, waardoor de legering harder en sterker wordt dan het zuivere metaal.
Nitinol
Een bijzondere legering is Nitinol, een legering van nikkel en titanium. Nitinol staat bekend als een geheugenmateriaal vanwege zijn unieke vormgeheugeneffect. Het principe werkt als volgt:
1.Verwarm Nitinol tot ongeveer 500 graden Celsius en breng het in de gewenste 'oorspronkelijke' vorm (bijvoorbeeld een rechte staaf).
2.Laat het afkoelen tot kamertemperatuur.
3.Bij kamertemperatuur kun je het materiaal vervormen (bijvoorbeeld buigen in de vorm van een kromme ruggengraat). Het neemt dan een andere roosterstructuur aan.
4.Als je het daarna weer een klein beetje verwarmt (bijvoorbeeld tot lichaamstemperatuur van 37 graden Celsius), keert het materiaal terug naar de oorspronkelijke vorm die het had bij 500 graden Celsius.

Een mogelijke toepassing van Nitinol wordt onderzocht in de medische wereld. Stel, een patiënt heeft een kromme ruggengraat. Een Nitinol-staafje wordt bij 500 graden Celsius recht gemaakt en vervolgens bij kamertemperatuur in de vorm van de kromme ruggengraat gebogen. Dit gebogen staafje wordt dan tijdens een operatie in het lichaam van de patiënt geplaatst. Zodra het staafje de lichaamstemperatuur van 37 graden Celsius bereikt, zal het terugbuigen naar zijn oorspronkelijke rechte vorm, waardoor de rug van de patiënt recht wordt getrokken. Dit is een voorbeeld van hoe nieuwe materialen deels onderzocht en deels al in gebruik zijn.













