Rangschik de volgende producten op basis van hun gehalte koolhydraten.
Leerdoelen
•Je kunt uitleggen wat koolhydraten zijn.
•Je kunt uitleggen hoe een condensatiereactie zorgt voor het koppelen van monosachariden tot di- en polysachariden.
•Je kunt uitleggen hoe hydrolyse bij koolhydraten werkt.
•Je kunt de open en ringstructuur van glucose onderscheiden.
•Je kunt uitleggen dat glucose als reductor, maar ook als oxidator kan optreden.
Wat zijn koolhydraten?
Koolhydraten zijn belangrijke organische verbindingen die je overal om je heen vindt, van je eten tot in hout. Ze hebben de algemene formule CnH2mOm. Vroeger dacht men dat koolhydraten letterlijk 'gehydrateerde koolstof' waren, met een vast aantal watermoleculen (H2O) per koolstofatoom (C). Later bleek dit niet helemaal correct te zijn, maar de naam is blijven hangen. Je vindt koolhydraten in veel voedingsmiddelen zoals pasta, brood en suiker, vaak in de vorm van zetmeel. Ook in hout zijn ze aanwezig, dan in de vorm van cellulose. Koolhydraten worden ook wel sachariden of suikers genoemd. In BiNaS-tabel 67F1 en 67F2 vind je voorbeelden van mono-, di- en polysachariden. Het is handig om deze tabellen te raadplegen als je meer wilt weten over hun structuren.
Fotosynthese en verbranding
Koolhydraten worden gevormd in planten via het proces van fotosynthese. Hierbij reageren koolstofdioxide (CO₂) en water (H₂O) in de bladgroenkorrels van planten onder invloed van licht tot glucose en zuurstof (O₂). De bijbehorende reactievergelijking is: 6 CO₂ (g) + 6 H₂O (l) → C₆H₁₂O₆ (aq) + 6 O₂ (g) De zuurstof die vrijkomt bij fotosynthese wordt door mensen en dieren ingeademd. In ons lichaam wordt deze zuurstof gebruikt als oxidator voor de verbranding van glucose, om zo energie op te wekken. Dit is precies de omgekeerde reactie van fotosynthese: C6H12O6 (aq) + 6 O2 (g) → 6 CO2 (g) + 6 H2O (l) Bij deze verbranding komt energie vrij die ons lichaam nodig heeft voor alle levensprocessen.
Monosachariden: de bouwstenen
De eenvoudigste koolhydraten zijn monosachariden. Dit zijn de bouwstenen waaruit grotere koolhydraten zijn opgebouwd. Een bekend voorbeeld is glucose. Monosachariden hebben vaak een ringstructuur. In deze ring zitten koolstofatomen op de hoekpunten en één zuurstofatoom (O) in de ring. Daarnaast bevatten monosachariden veel hydroxylgroepen (-OH). De molecuulformule van glucose is C6H12O6. Door de aanwezigheid van al die -OH-groepen zijn monosachariden, en daarmee alle sachariden, goed oplosbaar in water.
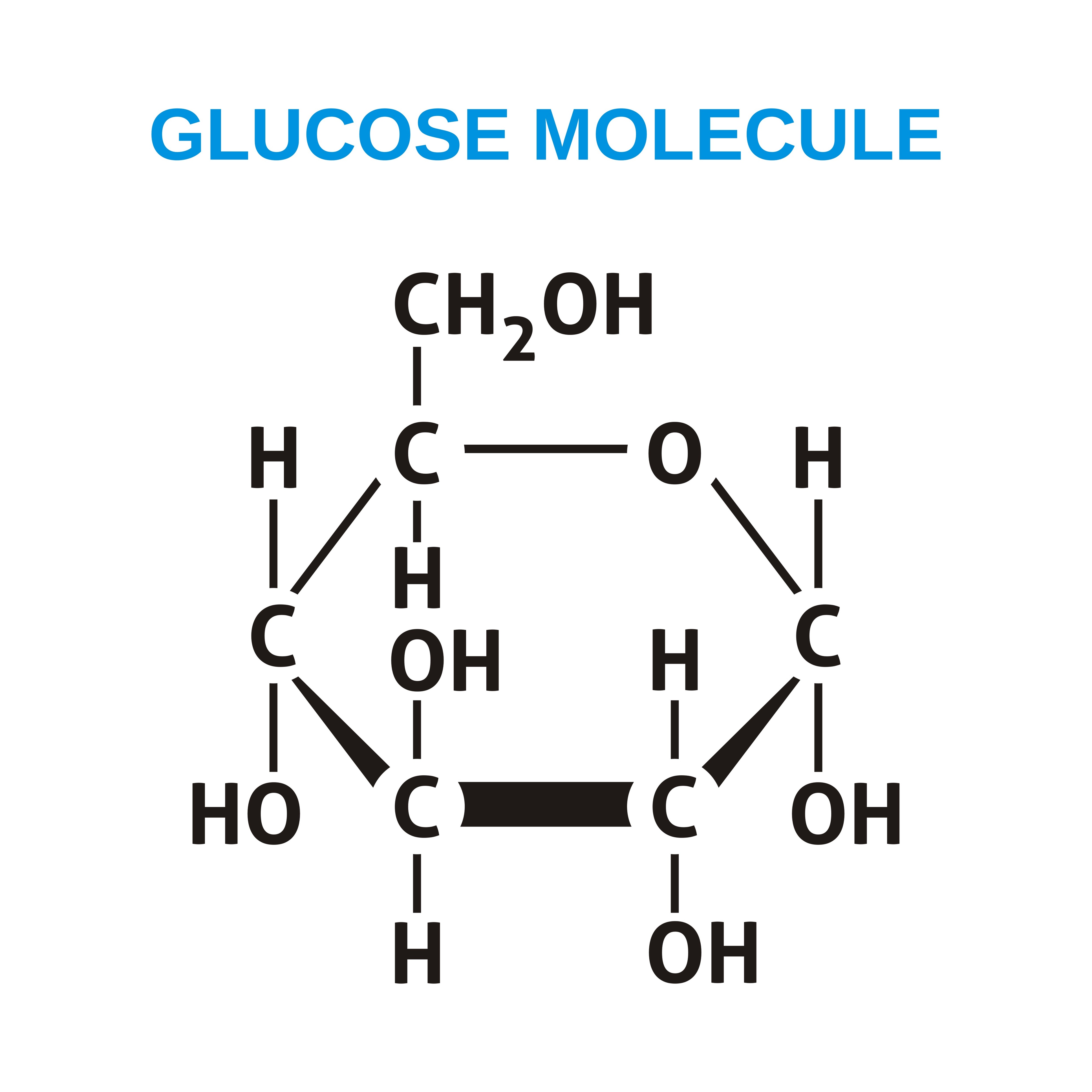
Glucose en fructose
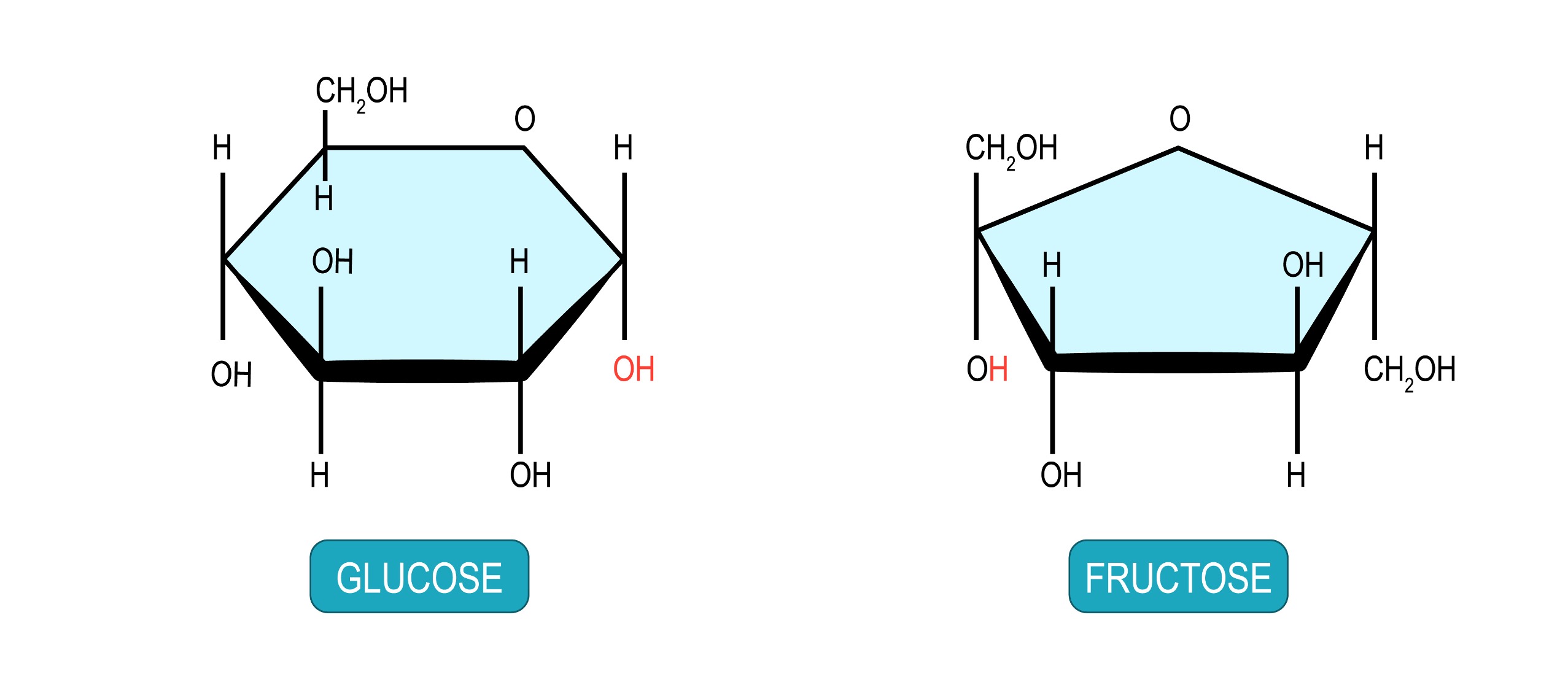
Glucose en fructose zijn beide monosachariden met dezelfde molecuulformule (C6H12O6), maar ze verschillen in hun structuur.
•Glucose heeft een ring met vijf koolstofatomen en één koolstofatoom buiten de ring.
•Fructose heeft een ring met vier koolstofatomen en twee koolstofatomen buiten de ring.
Condensatiereacties: van klein naar groot
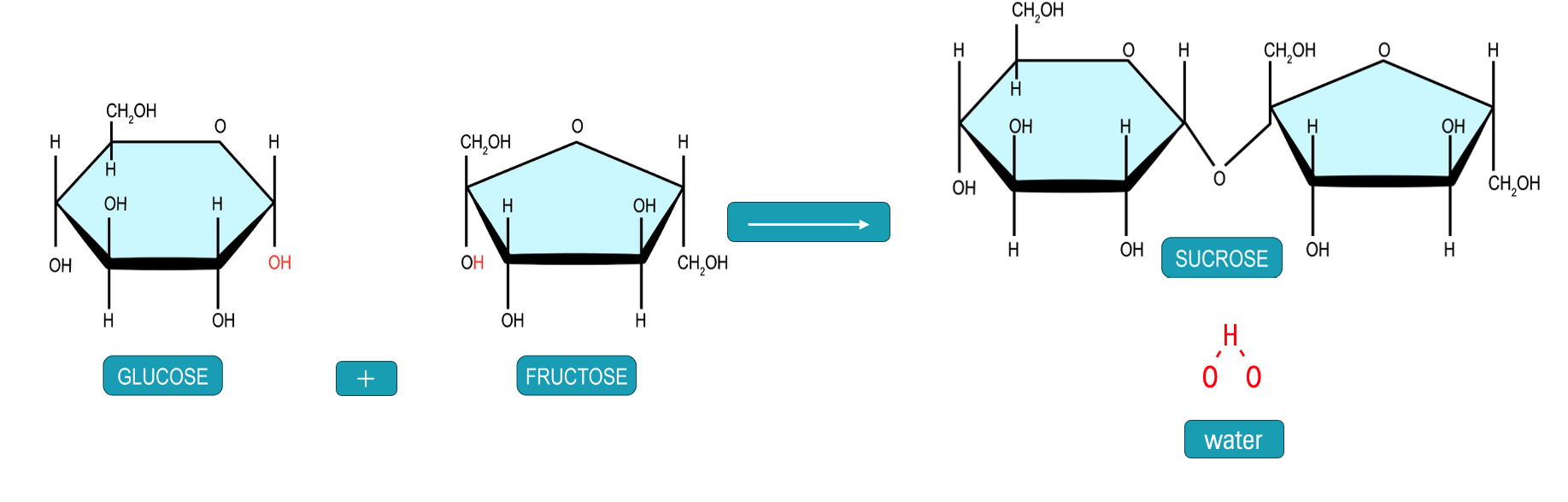
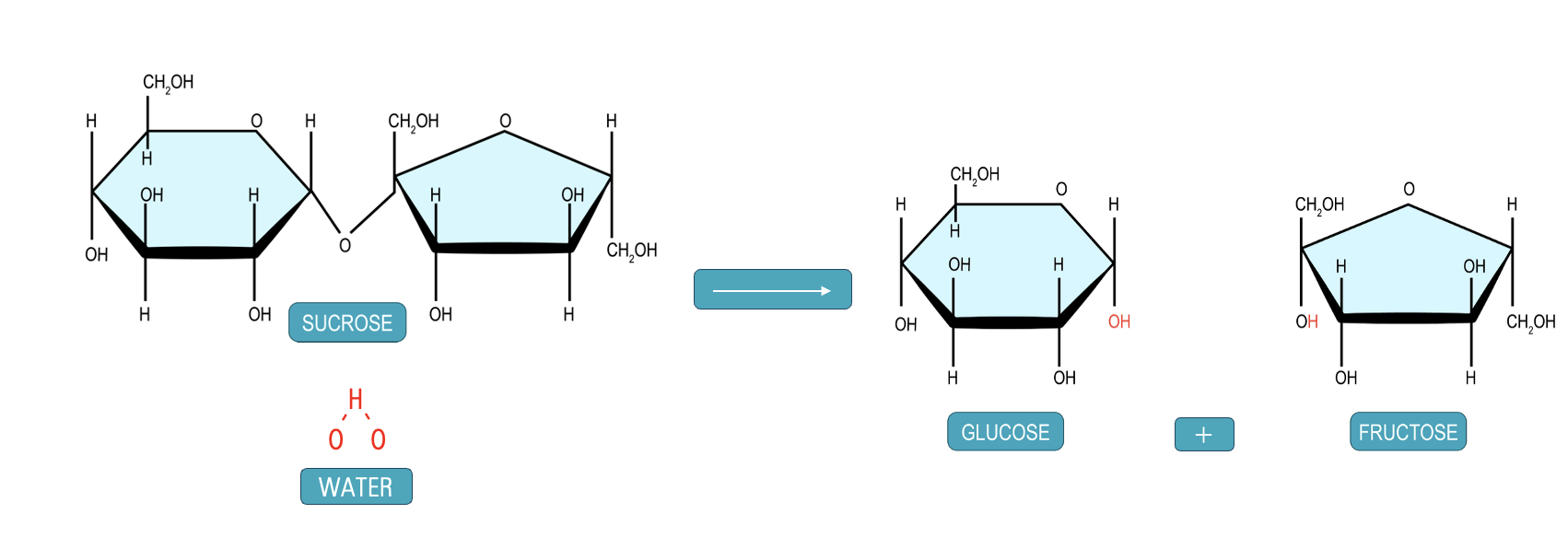
Monosachariden kunnen aan elkaar koppelen via een condensatiereactie om grotere koolhydraten te vormen. Bij een condensatiereactie worden twee moleculen aan elkaar gekoppeld onder afsplitsing van een klein molecuul, meestal water. Bij koolhydraten reageren twee hydroxylgroepen (-OH) van verschillende monosachariden met elkaar. Eén -OH-groep levert een H-atoom en de andere -OH-groep levert de resterende OH-groep; samen vormen ze een watermolecuul (H₂O). De twee monosachariden worden dan via een zuurstofatoom aan elkaar gekoppeld. Deze binding heet een glycosidische binding.
Disachariden
Wanneer twee monosachariden aan elkaar koppelen, ontstaat een disacharide. Een voorbeeld is de vorming van sacharose (gewone tafelsuiker) uit glucose en fructose, zoals hierboven afgebeeld. Glucose + Fructose → Sacharose + H₂O
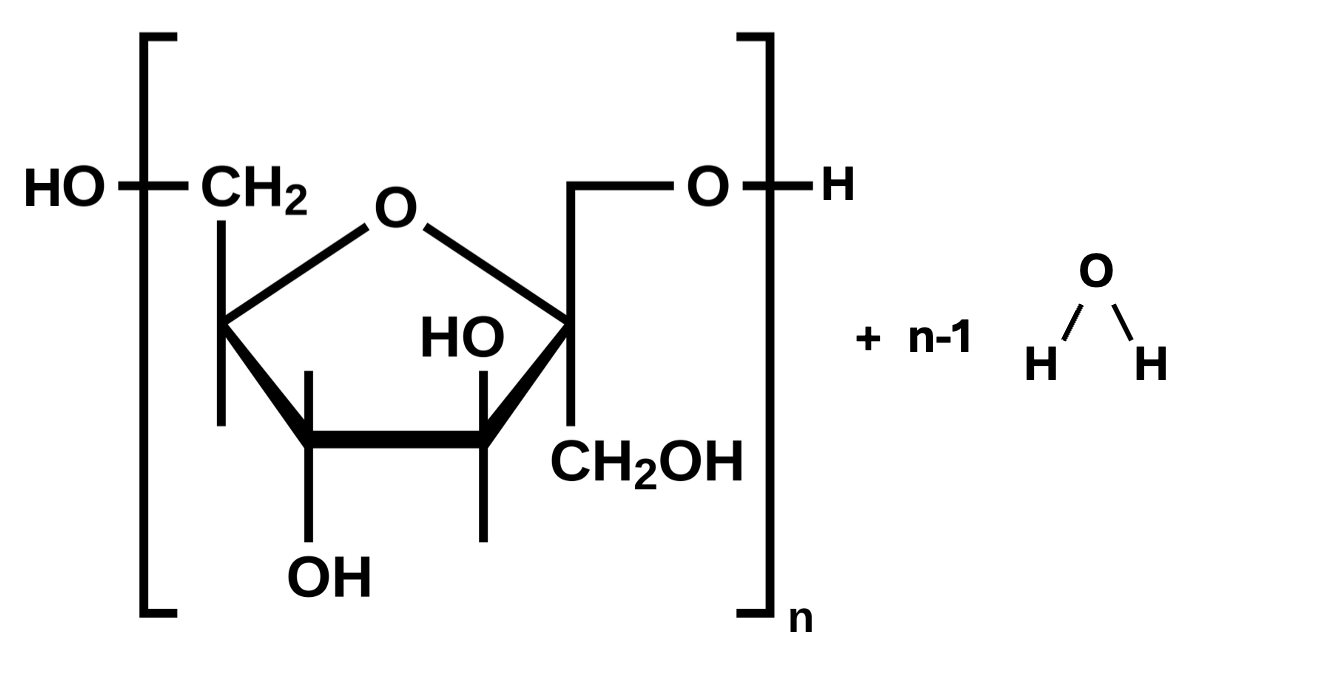
Polysachariden
Als veel monosachariden aan elkaar koppelen, ontstaat een polysacharide. Denk hierbij aan zetmeel en cellulose, die beide zijn opgebouwd uit vele glucose-eenheden. De vorming van een polymeer uit N monosachariden gaat gepaard met de afsplitsing van N-1 watermoleculen.
Hydrolyse: van groot naar klein
Hydrolyse is het omgekeerde van een condensatiereactie. Bij hydrolyse wordt een groter koolhydraat (een di- of polysacharide) met behulp van water weer afgebroken tot kleinere monosachariden. Het woord 'hydrolyse' komt van 'hydro' (water) en 'lyse' (knippen). Je kunt het je voorstellen als een watermolecuul dat de glycosidische binding tussen twee monosachariden 'knipt'. Het watermolecuul (H-OH) splitst zich: een H-atoom hecht zich aan het zuurstofatoom van de glycosidische binding, en de overgebleven -OH-groep hecht zich aan het andere koolstofatoom dat betrokken was bij de binding. Hierdoor ontstaan weer twee afzonderlijke monosachariden, elk met hun oorspronkelijke hydroxylgroepen.
Glucose: open- en ringstructuur
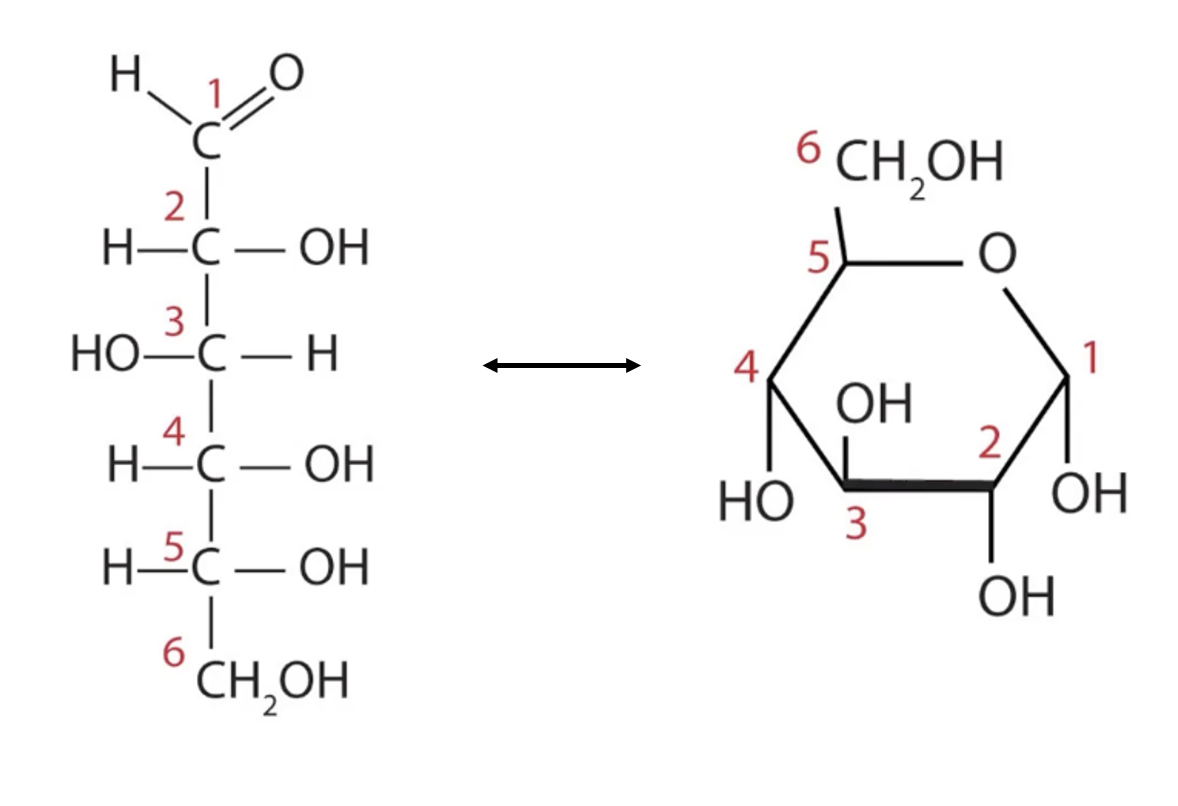
Glucose kan in water in twee vormen voorkomen: een ringstructuur en een open ketenstructuur. Hoewel de ringstructuur verreweg het meest voorkomt (ongeveer 99% van de tijd), is de open ketenstructuur (ongeveer 1% van de tijd) cruciaal voor bepaalde chemische reacties van glucose. De overgang tussen de ring- en de open structuur is een interne omzetting die voortdurend plaatsvindt. De molecuulformule (C6H12O6) blijft hetzelfde, maar de rangschikking van de atomen verandert.
De aldehydegroep
Het belangrijkste verschil tussen de ring- en de open structuur van glucose zit in de functionele groepen.
•De ringstructuur van glucose bevat alleen hydroxylgroepen (-OH).
•De open ketenstructuur van glucose bevat naast hydroxylgroepen ook een aldehydegroep (-CHO) op het eerste koolstofatoom (C1). Deze aldehydegroep is van groot belang, omdat deze glucose in staat stelt om als reductor op te treden.
Glucose als reductor
Door de aanwezigheid van de aldehydegroep in zijn open ketenstructuur kan glucose reageren als een reductor. Een reductor is een stof die elektronen afstaat en daarbij zelf geoxideerd wordt. Wanneer glucose als reductor reageert, wordt de aldehydegroep omgezet in een zuurgroep (-COOH). Dit gebeurt op het eerste koolstofatoom (C1). De halfreactie voor de oxidatie van de aldehydegroep naar een zuurgroep is als volgt: C=O-H (aldehydegroep) + H2O → C=O-O-H (zuurgroep) + 2 H+ + 2 e- Laten we deze halfreactie balanceren:
1.Koolstof (C): aan beide kanten 1 C-atoom.
2.Zuurstof (O): Links 1 O in de aldehydegroep + 1 O uit H₂O = 2 O. Rechts 2 O in de zuurgroep. Zuurstof is gebalanceerd.
3.Waterstof (H): Links 1 H in de aldehydegroep + 2 H uit H₂O = 3 H. Rechts 1 H in de zuurgroep + 2 H+ = 3 H. Waterstof is gebalanceerd.
4.Lading: Links totale lading 0. Rechts +2 (van 2 H+) en -2 (van 2 e-) = 0. Lading is gebalanceerd.
Deze halfreactie laat zien dat de aldehydegroep een zuurstofatoom opneemt (uit water) en twee protonen (H+) en twee elektronen (e-) afstaat. De afgestane elektronen kunnen worden opgenomen door een andere stof, de oxidator.
Glucose als oxidator
Glucose kan niet alleen als reductor optreden, maar ook als oxidator. Een oxidator is een stof die elektronen opneemt en daarbij zelf gereduceerd wordt. Wanneer glucose als oxidator reageert, wordt de aldehydegroep omgezet in een alcoholgroep (-CH2OH). Dit gebeurt ook op het eerste koolstofatoom (C1). De halfreactie voor de reductie van de aldehydegroep naar een alcoholgroep is als volgt: C=O-H (aldehydegroep) + 2 H+ + 2 e- → CH2OH (alcoholgroep) Laten we deze halfreactie balanceren:
1.Koolstof (C): Aan beide kanten 1 C-atoom.
2.Zuurstof (O): Links 1 O in de aldehydegroep. Rechts 1 O in de alcoholgroep. Zuurstof is gebalanceerd.
3.Waterstof (H): Links 1 H in de aldehydegroep + 2 H+ = 3 H. Rechts 2 H in de CH2 + 1 H in de OH = 3 H. Waterstof is gebalanceerd.
4.Lading: Links +2 (van 2 H+) en -2 (van 2 e-) = 0. Rechts 0. Lading is gebalanceerd.
Deze halfreactie laat zien dat de aldehydegroep twee protonen (H+) en twee elektronen (e-) opneemt. De opgenomen elektronen zijn afkomstig van een andere stof, de reductor.













