Geef van de onderstaande elementen aan wat de edelgasconfiguratie zal zijn en hoe het deze kan bereiken.
1. H
2. Li
3. Na
4. K
5. Ca


 Thijs Brouwer
Thijs BrouwerTest je kennis met de 2 examenvragen die aan dit onderwerp zijn gekoppeld.
Geef van de onderstaande elementen aan wat de edelgasconfiguratie zal zijn en hoe het deze kan bereiken.
1. H
2. Li
3. Na
4. K
5. Ca
Als je naar het periodiek systeem kijkt, zie je het chlooratoom aangegeven in een vierkant vakje. Dit atoom heeft 17 protonen, die zich in het midden van het atoom bevinden, en 17 elektronen. De verdeling van deze elektronen is als volgt: de K-schil kan slechts 2 elektronen bevatten, de L-schil kan 8 elektronen bevatten, wat betekent dat de overige 7 elektronen in de M-schil zitten.
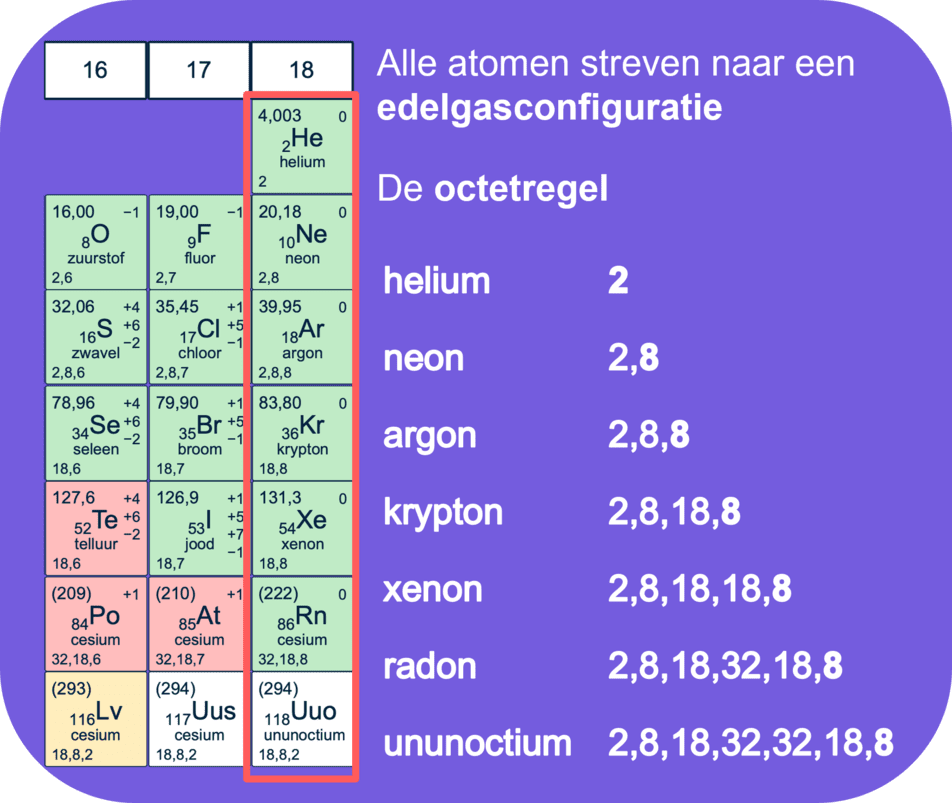
Hier zien we een belangrijk aspect van de structuur van atomen: atomen streven naar gevulde schillen, net zoals de edelgassen in de meest rechtse kolom van het periodiek systeem. Edelgassen hebben volledig gevulde schillen, wat ze zeer stabiel maakt.
Dit streven naar stabiliteit, of de volledige bezetting van de buitenste schil, staat bekend als de octetregel. Octet betekent acht. Dus atomen willen acht elektronen in de buitenste schil met uitzondering van de eerste schil waar er twee in gaan. En als je opgelet hebt kunnen je zeggen ‘Dat klopt niet, want in de derde schil (M) gaan er 18 en niet acht!’. En dat heb je dan goed gezien, maar de hoofdschillen waar we het eerder over gehad hebben (K,L,M) bevatten subschillen. En de telling van de subschillen is 2,8,8,8,8 etc. Dus in de buitenste altijd acht. En de buitenste subschil is belangrijk voor de reactiviteit van deeltjes en of ze een ion worden bijvoorbeeld. Het chlooratoom bijvoorbeeld, dat 7 elektronen in zijn buitenste schil heeft, wil graag nog een extra elektron verwerven om een volledige schil van 8 elektronen te hebben. Dit zal resulteren in een ion met een lading van min 1, omdat het een elektron meer heeft dan het aantal protonen. Dit nieuwe ion heeft dan dezelfde elektronenconfiguratie als Argon, namelijk 2,8,8.

Wanneer we naar de edelgassen kijken zien we dat de buitenste schil meestal 8 elektronen bevat, vandaar de term 'octet'. De enige uitzondering is Helium, dat 2 elektronen op de buitenste schil heeft, omdat het de eerste schil is.
Het ontstaan van ionen hangt dus nauw samen met deze octetregel. Ionen ontstaan wanneer atomen zich aanpassen - door elektronen op te nemen of af te staan - om aan deze regel te voldoen en de stabiliteit van een edelgasconfiguratie te bereiken.
Met deze kennis kunnen we nu kijken naar een ander atoom: natrium. Natrium heeft atoomnummer 11, wat betekent dat het 11 protonen en 11 elektronen heeft. Voor Natrium, om aan de octetregel te voldoen, is het echter gemakkelijker om een elektron te verliezen dan om de zeven elektronen te winnen die nodig zijn om op het volgende edelgas, Argon, te lijken.
Dus, natrium verliest een elektron en wordt daardoor positief geladen, resulterend in het natriumion. Dit proces van het verliezen of winnen van elektronen om aan de octetregel te voldoen, is hoe ionen ontstaan.

Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







