Wat is de juiste definitie van een molecuul?
Leerdoelen
•Je kunt uitleggen wat een molecuul is
•Je kunt het verschil uitleggen tussen een verbinding en een element
Wat is een molecuul?
Een molecuul is opgebouwd uit atomen, de kleinste bouwstenen van stoffen. Een bekend voorbeeld is een watermolecuul, dat bestaat uit twee waterstofatomen (H) en één zuurstofatoom (O). Moleculen kunnen verschillende structuren hebben, afhankelijk van hoe de atomen met elkaar verbonden zijn.
Verschil tussen verbindingen en elementen
•Verbinding: Een molecuul dat uit meerdere soorten atomen bestaat, zoals koolstofdioxide (CO₂).
•Element: Een molecuul dat alleen één soort atoom bevat, zoals zuurstofgas (O₂).
Als een molecuul slechts één soort atoom bevat, noemen we het een element. Bestaat het uit meerdere soorten atomen, dan is het een verbinding.
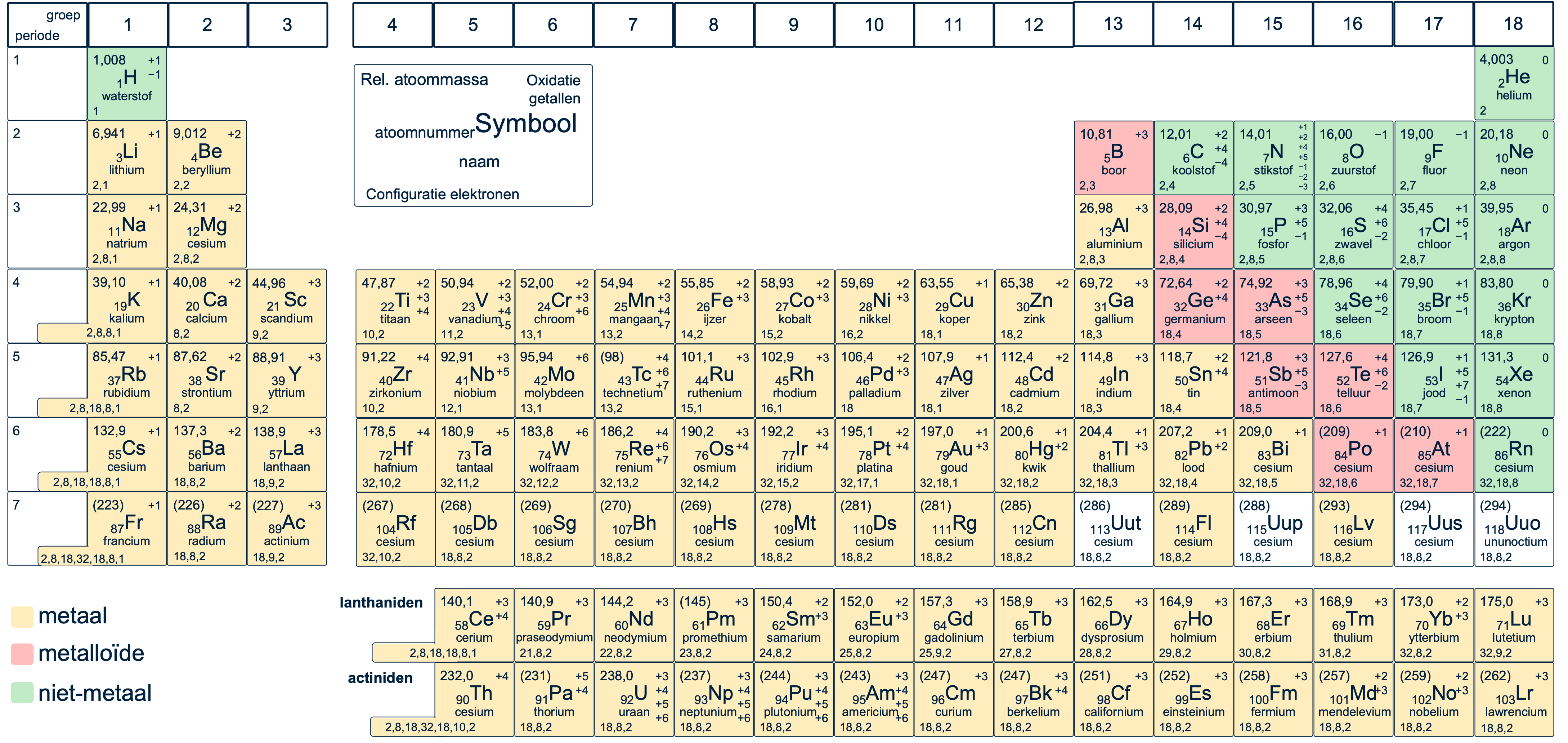
Het periodiek systeem
Het periodiek systeem is een tabel waarin alle bekende atoomsoorten worden weergegeven. Er zijn ongeveer 110 verschillende atoomsoorten, elk met een unieke naam en symbool. Deze symbolen bestaan uit één hoofdletter en soms een kleine letter, bijvoorbeeld:
•Aluminium: Al
•Barium: Ba
atoomsoorten | |||||
|---|---|---|---|---|---|
metalen | niet-metalen | ||||
naam | symbool | naam | symbool | naam | symbool |
aluminium | Al | platina | Pt | argon | Ar |
barium | Ba | radium | Ra | broom | Br |
calcium | Ca | tin (stannum) | Sn | chloor | Cl |
chroom | Cr | titaan | Ti | fluor | F |
goud (aurum) | Au | uraan | U | fosfor (phosphorus) | P |
kalium | K | wolfraam | W | helium | He |
kobalt | Co | ijzer (ferrum) | Fe | jood (iodum) | I |
koper (cuprum) | Cu | zilver (argentum) | Ag | koolstof (carboneum) | C |
kwik (hydrargurum) | Hg | zink | Zn | neon | Ne |
lood (plumbum) | Pb | silicium | Si | ||
magnesium | Mg | stikstof (nitrogenium) | N | ||
mangaan | Mn | waterstof (hydrogenium) | H | ||
natrium | Na | zuurstof (oxygenium) | O | ||
nikkel | Ni | zwavel (sulfur) | S | ||
Groepen en periodes
De tabel heeft:
•Groepen: Verticale kolommen waarin elementen met vergelijkbare eigenschappen staan, zoals:
Groep 1: Alkalimetalen (bijv. natrium, kalium).
Groep 2: Aardalkalimetalen (bijv. magnesium, calcium).
Groep 17: Halogenen (bijv. fluor, chloor).
Groep 18: Edelgassen (bijv. helium, neon).
•Periodes: Horizontale rijen waarin de atoommassa toeneemt.
Metalen, niet-metalen en metalloïden
Elementen worden verdeeld in:
•Metalen: Geleiden warmte en elektriciteit, hebben een glanzend oppervlak, en kunnen vervormd worden.
•Niet-metalen: Hebben geen gemeenschappelijke eigenschappen zoals metalen.
•Metalloïden: Liggen tussen metalen en niet-metalen in.
Bijzondere delen van het periodiek systeem
•Lanthaniden en actiniden: Deze rijen staan onderaan het periodiek systeem, maar horen eigenlijk tussen andere elementen.
De ontdekking van het periodiek systeem
Dimitri Mendelejev ordende de elementen in 1896 op basis van hun massa en eigenschappen. Hij ontdekte dat elementen met vergelijkbare eigenschappen in groepen onder elkaar geplaatst konden worden. Mendelejev liet zelfs lege plekken open voor elementen die nog ontdekt moesten worden, en zijn voorspellingen bleken later correct.
Dankzij Mendelejev kunnen we vandaag het periodiek systeem gebruiken om miljoenen moleculen te bouwen, net zoals je dat met legosteentjes doet.













