Wat is de belangrijkste binding tussen moleculen in een moleculaire stof?
Leerdoelen
•Je kunt uitleggen wat een moleculaire stof is.
•Je kunt uitleggen wat de vanderwaalsbinding is.
•Je kunt uitleggen hoe de VWD-binding het kookpunt beïnvloedt.
•Je kunt uitleggen wat een structuurformule, een atoombinding en de covalentie is.
De overgang van een vloeistof naar een gas
Een vloeistof bestaat uit moleculen die elkaar aanraken, terwijl in de gasfase de moleculen los van elkaar bewegen. Dit komt doordat de van der Waals krachten tussen de moleculen worden verbroken wanneer de stof verdampt.
Van der Waals krachten en het kookpunt
De van der Waals kracht is de fundamentele binding tussen moleculen in een moleculaire stof. Deze krachten zijn afhankelijk van de massa van de moleculen. Hoe groter de massa van een molecuul, hoe sterker de van der Waals krachten en hoe hoger het kookpunt. Dit is bijvoorbeeld te zien bij methaan (CH₄, 16u), ethaan (C₂H₆, 30u) en propaan (C₃H₈), waarbij het kookpunt toeneemt met de molecuulmassa.
Daarnaast speelt het contactoppervlak een rol. Een langwerpig molecuul zoals pentaan heeft een groter contactoppervlak dan een bolvormig molecuul zoals methylbutaan. Hierdoor zijn de van der Waals krachten sterker bij pentaan en is het kookpunt hoger.
Atoombinding en covalentie
In een moleculaire stof worden de atomen bij elkaar gehouden door een atoombinding, ook wel een covalente binding genoemd. Atomen delen elektronen om een stabiele edelgasconfiguratie te bereiken. De covalentie van een atoom geeft aan hoeveel bindingen het kan vormen:
•Waterstof (H), fluor (F), chloor (Cl), broom (Br) en jood (I): covalentie 1
•Zuurstof (O) en zwavel (S): covalentie 2
•Stikstof (N) en fosfor (P): covalentie 3
•Koolstof (C) en silicium (Si): covalentie 4
Bijvoorbeeld: in een waterstofmolecuul (H₂) delen twee waterstofatomen elk een elektron om samen een stabiele binding te vormen.
Structuurformules
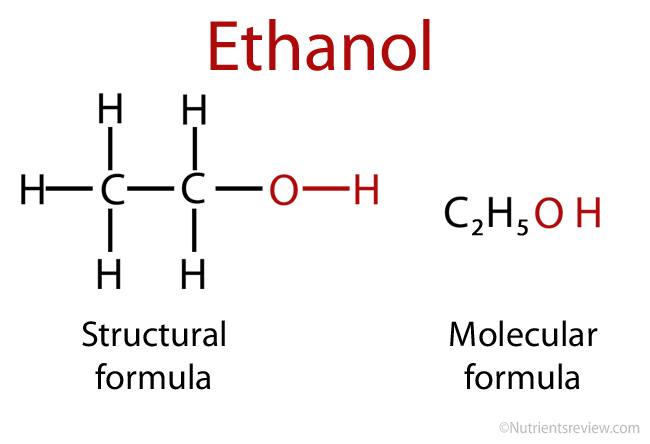
Een structuurformule geeft de atoombindingen in een molecuul weer met streepjes. Bijvoorbeeld ethanol (C₂H₆O): bevat koolstof (C) met vier bindingen, waterstof (H) met één binding en zuurstof (O) met twee bindingen.
Waterstofbruggen en oplosbaarheid
Sommige moleculen vormen waterstofbruggen, een extra sterke intermoleculaire kracht die voorkomt bij moleculen met een OH- of NH-groep. Waterstofbruggen zorgen ervoor dat stoffen een hoger kookpunt hebben en goed oplossen in water. Waterstofbruggen ontstaan bijvoorbeeld in water (H₂O) en ethanol (C₂H₆O), waardoor deze stoffen goed mengbaar zijn.
•Oplosbaarheid in water hangt af van de polariteit:
•Hydrofiele stoffen lossen goed op in water en bevatten vaak OH- of NH-groepen.
•Hydrofobe stoffen lossen niet op in water en bevatten alleen C- en H-atomen (bijvoorbeeld methaan).
•Emulgatoren helpen hydrofobe en hydrofiele stoffen mengen door een hydrofiele kop en een hydrofobe staart.
Gevaar van zwemmen tijdens onweer
Zuiver water (H₂O) geleidt geen stroom, maar water in meren of zwembaden bevat opgeloste zouten en ionen die wél stroom geleiden. Tijdens onweer kan bliksem inslaan in het water, waardoor stroom door het water geleid wordt en levensgevaarlijk kan zijn. Daarom moet je nooit in open water zwemmen als het onweert.














