Wat gebeurt er met de ionen in een zout wanneer het wordt opgelost in water?
Leerdoelen
•Je kunt uitleggen wat een ionrooster en de ionbinding zijn.
•Je kunt uitleggen waarom en metaal buigzaam is en een zout breekt.
Het ionrooster en de ionbinding
Zouten zijn verbindingen die bestaan uit metaalionen en niet-metaalionen, en ze vormen een ionrooster. In dit rooster worden de ionen bij elkaar gehouden door sterke ionbindingen. Deze bindingen zijn elektrostatische krachten tussen de positief geladen metaalionen en de negatief geladen niet-metaalionen.
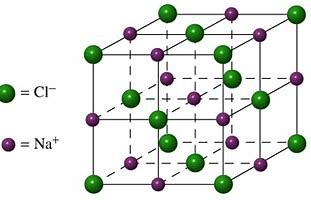
Eigenschappen van zouten
•Geleiding van elektriciteit: Zouten kunnen elektriciteit geleiden wanneer ze gesmolten zijn of opgelost in water, omdat de ionen dan vrij kunnen bewegen.
•Sterke bindingen: De ionbinding is sterker dan de Van-der-Waalsbinding, wat resulteert in hoge smeltpunten voor zouten.
Voorbeeld: natriumchloride
Natriumchloride (NaCl) is een klassiek voorbeeld van een zout. Het bestaat uit natriumionen (Na⁺) en chloride-ionen (Cl⁻). In vaste toestand trillen de ionen op hun plek in het ionrooster en kunnen ze geen stroom geleiden. Wanneer NaCl wordt opgelost in water of gesmolten, kunnen de ionen vrij bewegen en geleidt het wel elektriciteit.
Metaal vs. zout: buigzaamheid en breekbaarheid
Waarom zijn metalen buigzaam?
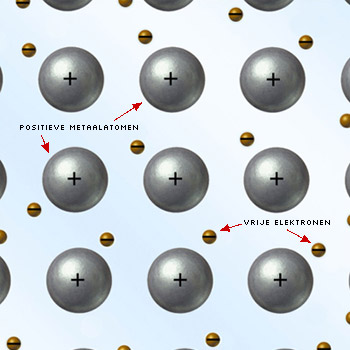
Metalen zijn buigzaam omdat hun structuur bestaat uit metaalionen omgeven door vrije elektronen. Deze elektronen kunnen vrij door het metaalrooster bewegen en houden de metaalionen bij elkaar, zelfs als het metaal wordt vervormd. Dit betekent dat de metaalbinding intact blijft, waardoor het metaal niet breekt.
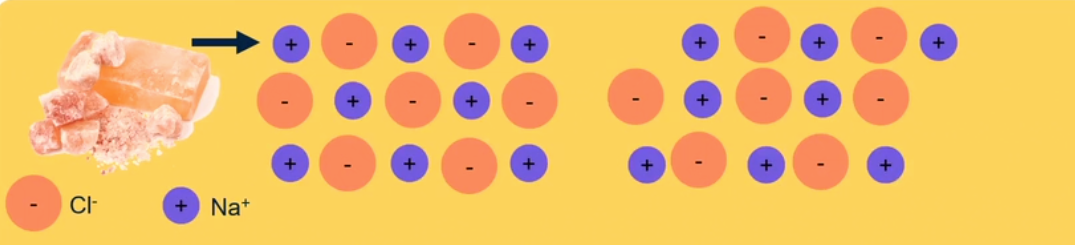
Waarom breken zouten?
Zouten zijn daarentegen breekbaar. In een ionrooster worden de positieve en negatieve ionen afwisselend gerangschikt. Wanneer er kracht op een zout wordt uitgeoefend, kunnen de lagen van ionen verschuiven. Dit resulteert in een situatie waarin gelijke ladingen (plus boven plus, min boven min) tegenover elkaar komen te liggen, wat leidt tot afstoting en breuk van het zout.
Toepassing: Het vrijheidsbeeld
Het Vrijheidsbeeld is een interessant voorbeeld van de overgang van een metaal naar een zout. Oorspronkelijk gemaakt van brons (een legering van koper en tin), is de buitenkant van het beeld geoxideerd tot kopercarbonaat (CuCO₃), een zout. Dit proces heeft het beeld zijn kenmerkende groen-blauwe kleur gegeven.














