Hoeveel eieren zitten er in 1,5 dozijn eieren?
Leerdoelen
•Je kunt benoemen hoeveel deeltjes er in een mol zitten.
•Je kunt uitleggen waarom de mol handig is.
•Je kunt de molecuulmassa bepalen en uitleggen dat dit hetzelfde is als de molaire massa.
•Je kunt het molrekenschema gebruiken.
Wat is een mol?
Een mol is een eenheid in de scheikunde waarmee je grote aantallen deeltjes (zoals atomen, moleculen of ionen) gemakkelijk kunt beschrijven. In1\text{ mol}1111111111111\;1\;m1\;mo1\;mol zitten altijddeeltjes. Dit enorme getal heet het getal van Avogadro en wordt vaak afgekort alsN_{A}.
Waarom is de mol handig?
De mol maakt het rekenen met deeltjes eenvoudiger. In plaats van te werken met enorme getallen zoals triljoenen deeltjes, gebruik je de mol om het aantal deeltjes om te rekenen naar een massa in gram. Bovendien heeft de mol een bijzondere eigenschap: de molecuulmassa van een stof in u (atoommassa-eenheden) is numeriek gelijk aan de molaire massa in gram.
Voorbeeld:
De molecuulmassa van water\left(H_2O\right)\left(H_2O\right)is18{,}02\text{ u}18{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}018{,}1818,18,018,02.
De molaire massa van water is 18{,}02\text{ gram}18{,}02\text{ gram}18{,}02\text{gram}18{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}0218{,}018{,}1818,18,018,0218,02\;18,02\;g18,02\;gr18,02\;gra18,02\;gram18,02\;gram=18,02\;gramper mol. Dit betekent dat 1 mol water, bestaande uitmoleculen, preciesweegt.
Molecuulmassa en molaire massa
De molecuulmassa van een stof is de som van de massa's van alle atomen in een molecuul. Deze waarden kun je vinden in het periodiek systeem.
Rekenvoorbeeld: koolstofdioxide\left(CO_2\right)\left(CO_2\right)
1.Koolstof (C) heeft een atoommassa van12{,}01\text{ u}.12{,}01\text{ u}12{,}0112{,}0112{,}0112{,}0112{,}0112{,}0112{,}0112{,}0112{,}0112{,}0112{,}012{,}1212\;12\;u12,\;u12,0\;u12,01\;u
2.Zuurstof (O) heeft een atoommassa van16{,}00\text{ u}.16{,}00\text{ u}.16{,}00\text{ u}16{,}0016{,}0016{,}0016{,}0016{,}0016{,}0016{,}0016{,}0016{,}0016{,}0016{,}016{,}1616,16,016,00.
3.De molecuulmassa vanis: 12{,}01+2\times16{,}00=44{,}01\text{ u}12{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}0112{,}01+2\times16{,}00=44{,}012{,}01+2\times16{,}00=44{,}12{,}01+2\times16{,}00=4412{,}01+2\times16{,}00=44,12{,}01+2\times16{,}00=44,012{,}01+2\times16{,}00=44,0112{,}01+2\times16{,}00=44,01u12{,}01+2\times16{,}00=44,01u12{,}01+2\times16{,}0=44,01u12{,}01+2\times16{,}=44,01u12{,}01+2\times16=44,01u12{,}01+2\times16,=44,01u12{,}01+2\times16,0=44,01u12{,}01+2\times16,00=44,01u12{,}01+2\times16,00=44,01u12{,}0+2\times16,00=44,01u12{,}+2\times16,00=44,01u12+2\times16,00=44,01u12,+2\times16,00=44,01u12,0+2\times16,00=44,01u Dus de molaire massa is 44,01 gram per mol.
Het molrekenschema
Het molrekenschema is een handig hulpmiddel om berekeningen met mollen te maken. Hiermee kun je eenvoudig rekenen van massa naar mol, van mol naar aantal deeltjes of andersom.
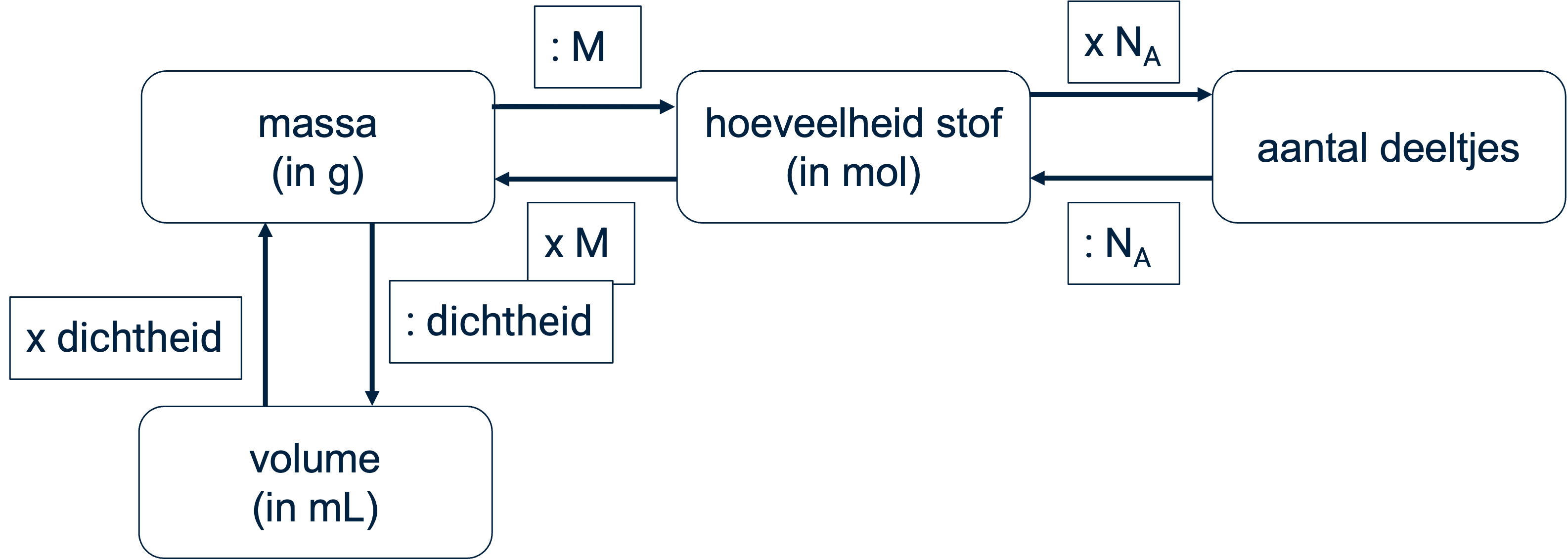
Het schema:
•Om van massa (in gram) naar mol te rekenen: deel de massa door de molaire massa (M).
•Om van mol naar massa te rekenen: vermenigvuldig de mol met de molaire massa (M).
•Om van mol naar aantal deeltjes te rekenen: vermenigvuldig de mol met het getal van Avogadro\left(N_{A}\right).\left(N_{A}\right)N_{A})
•Om van aantal deeltjes naar mol te rekenen: deel het aantal deeltjes door\left(N_{A}\right).N_{A}).N_{A})
Voorbeeld
Hoeveel mol is 10 gram vanP_2O_5?
1.De molaire massa vanis142{,}00\text{ g/mol.}142{,}00\text{ g/mol}142{,}00\text{ g/mol}142{,}00\text{g/mol}142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00142{,}00^{}142{,}00^{\prime}142{,}00142{,}00\;142{,}00\;g142{,}00\;g/142{,}00\;g/m142{,}00\;g/mo142{,}00\;g/mol142{,}0\;g/mol142{,}\;g/mol142\;g/mol142,\;g/mol142,0\;g/mol142,00\;g/mol
2.Berekening:10\text{ g}\div142{,}00\text{ g/mol}=0{,}07\text{ mol}10\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}0710\text{ g}\div142{,}00\text{ g/mol}=0{,}010\text{ g}\div142{,}00\text{ g/mol}=0{,}0610\text{ g}\div142{,}00\text{ g/mol}=0{,}010\text{ g}\div142{,}00\text{ g/mol}=0{,}10\text{ g}\div142{,}00\text{ g/mol}=010\text{ g}\div142{,}00\text{ g/mol}=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00=10\text{ g}\div142{,}00\;=10\text{ g}\div142{,}00\;g=10\text{ g}\div142{,}00\;g/=10\text{ g}\div142{,}00\;g/m=10\text{ g}\div142{,}00\;g/mo=10\text{ g}\div142{,}00\;g/mol=10\text{ g}\div142{,}0\;g/mol=10\text{ g}\div142{,}\;g/mol=10\text{ g}\div142\;g/mol=10\text{ g}\div14\;g/mol=10\text{ g}\div142\;g/mol=10\text{ g}\div1420\;g/mol=10\text{ g}\div14200\;g/mol=10\text{ g}\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10\div142,00\;g/mol=10g\div142,00\;g/mol=10g\div142,00g/mol=10g\div142,00g/mol10g\div142,00g/mol~10g\div142,00g/mol10g\div142,00g/mol\degree10g\div142,00g/mol
Toepassing: hoeveel watermoleculen in een glas?
Stel dat je wilt weten hoeveel watermoleculen er in een glas van 250 milliliter water zitten. Hiervoor gebruik je het molrekenschema én de dichtheid van water\left(1{,}00\text{ g/ml}\right).\left(1{,}00\text{ g/mol}\right).\left(1{,}00\text{ g/mol}\right)\left(1{,}00\text{ g/mol}\right)\left(1{,}0\text{ g/mol}\right)\left(1{,}\text{ g/mol}\right)\left(1\text{ g/mol}\right)\left(1,\text{ g/mol}\right)\left(1,0\text{ g/mol}\right)\left(1,00\text{ g/mol}\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\right)\left(1,00\;\right)\left(1,00\;g\right)\left(1,00\;g/\right)\left(1,00\;g/m\right)\left(1,00\;g/ml\right)\left(1,00\;g/ml\right)1,00\;g/ml
Stap 1: Bereken de massa. 250\text{ ml}\times1{,}00\text{ g/ml}=250\text{ g}250\text{ ml}\times1{,}00\text{ g/mol}=250\text{ g}250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250250\text{ ml}\times1{,}00\text{ g/mol}=250\;250\text{ ml}\times1{,}00\text{ g/mol}=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00=250\;g250\text{ ml}\times1{,}00\;=250\;g250\text{ ml}\times1{,}00\;g=250\;g250\text{ ml}\times1{,}00\;g/=250\;g250\text{ ml}\times1{,}00\;g/m=250\;g250\text{ ml}\times1{,}00\;g/ml=250\;g250\text{ ml}\times1{,}0\;g/ml=250\;g250\text{ ml}\times1{,}\;g/ml=250\;g250\text{ ml}\times1\;g/ml=250\;g250\text{ ml}\times1,\;g/ml=250\;g250\text{ ml}\times1,0\;g/ml=250\;g250\text{ ml}\times1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g250\text{ ml}1,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g2501,00\;g/ml=250\;g250\;1,00\;g/ml=250\;g250\;m1,00\;g/ml=250\;g250\;ml1,00\;g/ml=250\;g250\;ml\times1,00\;g/ml=250\;g250ml\times1,00\;g/ml=250\;g250ml\times1,00g/ml=250\;g
Stap 2: Bereken het aantal mol. 250\text{ g}\div18{,}02\text{ g/mol}=13,87\text{ mol}250\text{ g}\div18{,}02\text{ g/mol}=13,87\text{ mol}.250\text{ g}\div18{,}02\text{ g/mol}=13,87\text{ mol}250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87250\text{ g}\div18{,}02\text{ g/mol}=13,87\;250\text{ g}\div18{,}02\text{ g/mol}=13,87\;m250\text{ g}\div18{,}02\text{ g/mol}=13,87\;mo250\text{ g}\div18{,}02\text{ g/mol}=13,87\;mol250\text{ g}\div18{,}02\text{ g/mol}=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02=13,87\;mol.250\text{ g}\div18{,}02\;=13,87\;mol.250\text{ g}\div18{,}02\;g=13,87\;mol.250\text{ g}\div18{,}02\;g/=13,87\;mol.250\text{ g}\div18{,}02\;g/m=13,87\;mol.250\text{ g}\div18{,}02\;g/mo=13,87\;mol.250\text{ g}\div18{,}02\;g/mol=13,87\;mol.250\text{ g}\div18{,}0\;g/mol=13,87\;mol.250\text{ g}\div18{,}\;g/mol=13,87\;mol.250\text{ g}\div18\;g/mol=13,87\;mol.250\text{ g}\div18,\;g/mol=13,87\;mol.250\text{ g}\div18,0\;g/mol=13,87\;mol.250\text{ g}\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\div18,02\;g/mol=13,87\;mol.250\;\div18,02\;g/mol=13,87\;mol.250\;g\div18,02\;g/mol=13,87\;mol.250\;g\div18,02\;g/mol=13,87mol.250g\div18,02\;g/mol=13,87mol.
Stap 3: Bereken het aantal moleculen. 13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\text{ moleculen}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;m13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;mo13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;mol13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;mole13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;molec13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;molecu13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;molecul13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;molecule13{,}87\text{ mol}\times6{,}02\times10^{23}\text{ moleculen/mol}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;m=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;mo=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;mole=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;molec=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;molecu=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;molecul=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;molecule=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;moleculen=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;moleculen/=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;moleculen/m=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;moleculen/mo=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}0\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6{,}\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6,\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6,0\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\text{ mol}\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}8\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}9\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13{,}\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,8\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\;\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\;m\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\;mo\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}\;moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^{24}moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^2moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^24moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^2moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^24moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10^2moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times10moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times1moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times14moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times104moleculen13,87\;mol\times6,02\times10^{23}\;moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^{23}\;moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^{23}moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^{23}3moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^23moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^233moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10^23moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times103moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times10\&3moleculen/mol=8,35\times1024moleculen13,87mol\times6,02\times103moleculen/mol=8,35\times1024moleculen














