Hoe heet de binding die de deeltjes in een zout bij elkaar houdt?
Leerdoelen
•Je kunt uitleggen hoe zouten worden gevormd.
•Je kunt verschillende ionsoorten benoemen.
•Je kunt beschrijven hoe een ionrooster ontstaat.
•Je kunt namen en formules van zouten opstellen.
Atomen en ionbindingen
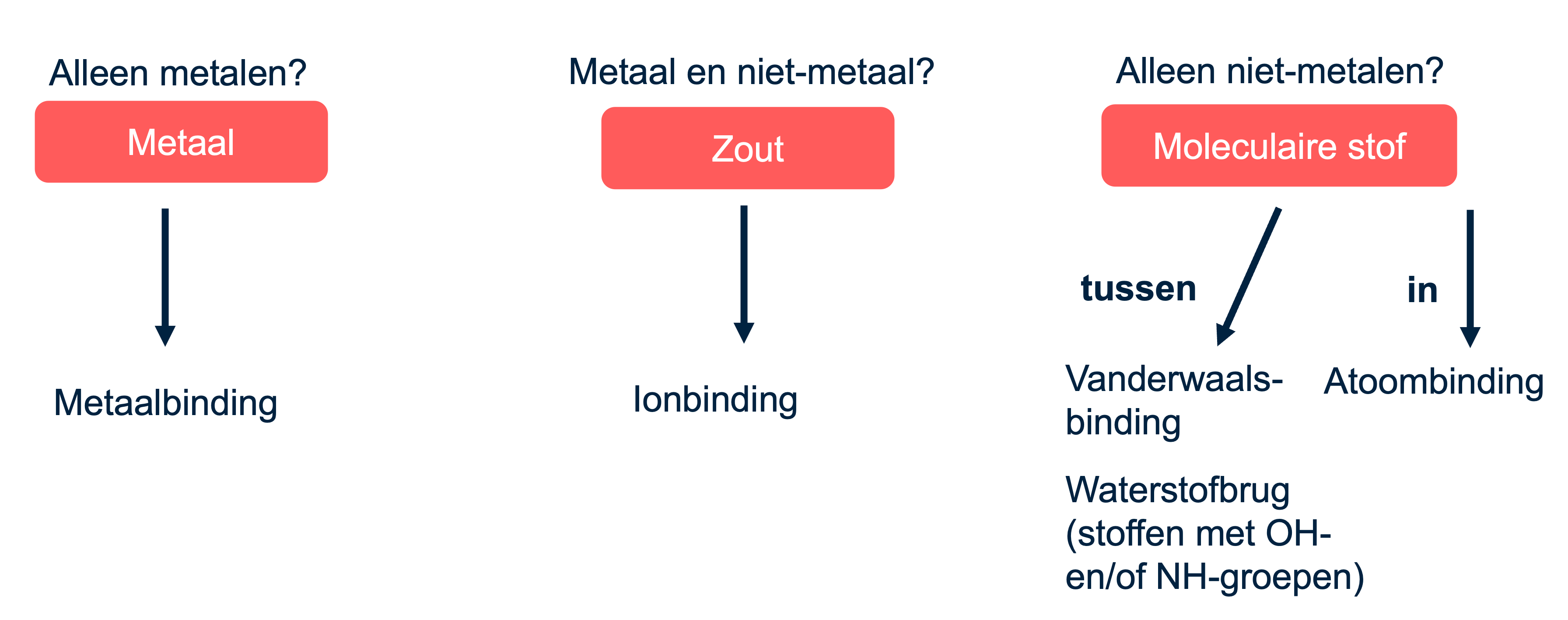
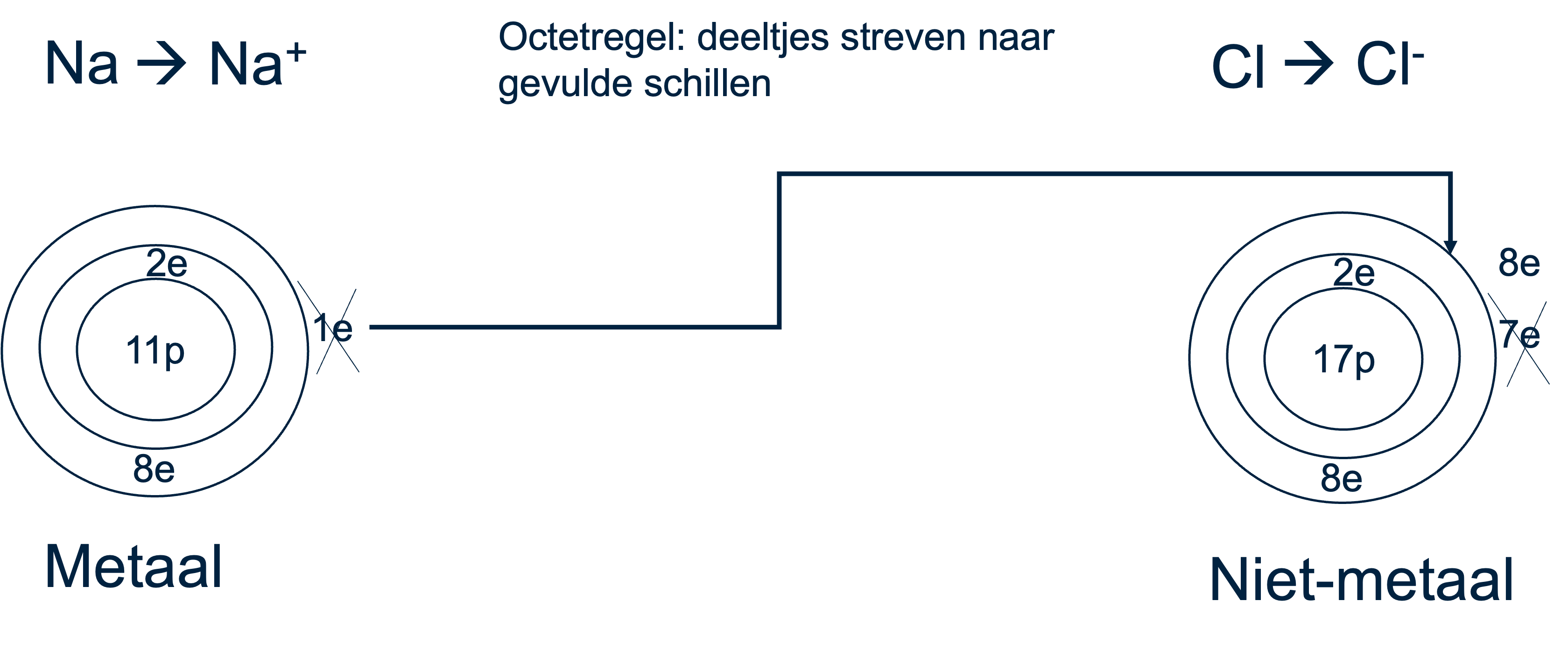
De kern van het begrijpen van zouten ligt bij de vorming van ionbindingen. Ionbindingen ontstaan tussen metalen en niet-metalen door de overdracht van elektronen. Een goed voorbeeld hiervan is de binding tussen natrium en chloor. Natrium (Na), een metaal, en chloor (Cl), een niet-metaal, combineren door een elektronoverdracht waarbij het natriumatoom een positief geladen ionen (Na+) wordt en het chlorideatoom een negatief geladen chloride-ion (Cl-) wordt. Deze overdracht leidt tot een elektrostatische aantrekking tussen de ionen, wat resulteert in de vorming van natriumchloride, oftewel keukenzout.
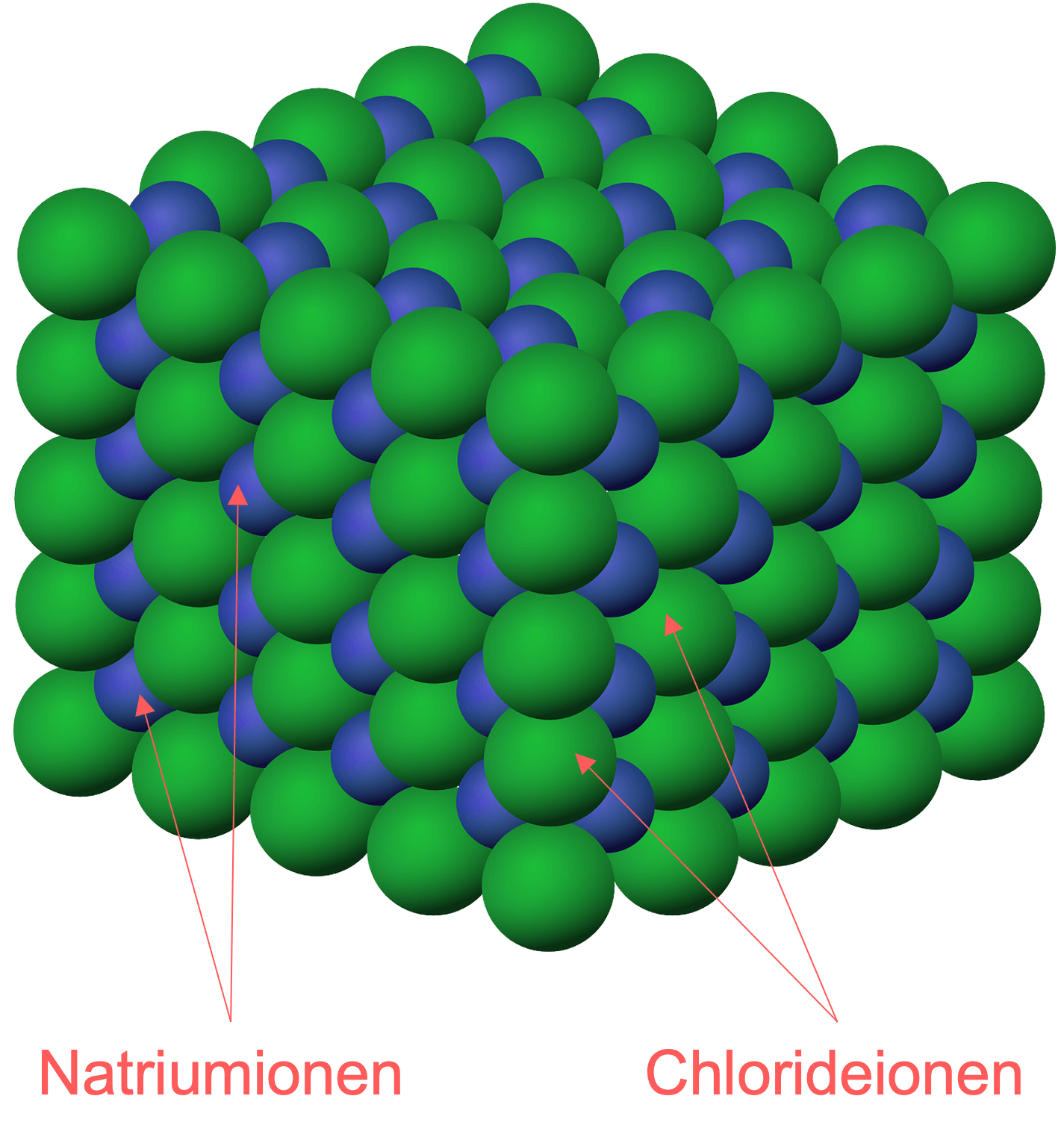
Het ionrooster
Zouten in de vaste fase zijn georganiseerd in een ionrooster, waarbij de positieve en negatieve ionen elkaar afwisselen. Ze vormen daarbij een neutraal geheel.
Ionbindingen zijn sterke elektrostatische aantrekkingskrachten tussen positieve en negatieve ionen. Daardoor hebben zouten hoge smel- en kookpunten en is veel energie nodig om het ionrooster te verbreken.
Natriumchloride vormt bijvoorbeeld kubische kristallen, waarbij de natrium-ionen (iets kleiner) en chloride-ionen in een specifieke verhouding gerangschikt zijn.
De natrium-ionen zijn kleiner dan de chloride-ionen omdat natrium na het afstaan van één elektron één gevulde schil minder heeft dan chloor. Het natrium-ion heeft daardoor minder elektronenlagen dan het chloride-ion, en dus een kleinere straal.
Namen en formules van zouten
Het benoemen van zouten is gestandaardiseerd. Positieve ionen behouden de naam van het atoom. Negatieve ionen krijgen de uitgang ‘-ide’, zoals ‘chloride' van ’chloor'. Voor metalen die maar één mogelijke lading hebben (zoals natrium of calcium) wordt geen extra aanduiding gebruikt. Voor metalen die meer dan één positieve lading kunnen hebben, zoals ijzer (Fe2+ en Fe3+) en goud (en), wordt een Romeins cijfer in de naam gezet. Dit Romeinse cijfer geeft de lading van het metaalion aan.
Bepalen Romeinse cijfer
Een zout is altijd elektrisch neutraal. Dat betekent: totale pluslading = totale minlading.
De lading van het metaalion wordt dus afgeleid uit de totale negatieve lading van de niet-metaalionen. Je bepaalt het Romeinse cijfer in drie stappen:
1.Bepaal de lading van het negatieve ion.
2.Vermenigvuldig met het aantal negatieve ionen.
3.Leid daaruit de lading van het metaal af.
Voorbeeld:
Chloride heeft lading -1 en er zijn drie chloride-ionen:
Totale minlading =3\cdot\left(-1\right)=-33\cdot\left(-1\right)=-33\cdot\left(-1\right)=-3\cdot\left(-1\right)=3\cdot\left(-1\right)3\cdot\left(-1\right)3\cdot\left(-\right)3\cdot\left(\right)3\cdot3
Om het zout neutraal te maken, moet ijzer dus +3 zijn. De naam wordt: ijzer(III)chloride. Het Romeinse cijfer III geeft aan dat het omgaat.
Molecuulformule | Naam |
|---|---|
Al_2O_3Al_2O_{\placeholder{}}Al_2OAl_2Al_{2O}Al_2Al_{\placeholder{}}AlAlxAlAlsAlssAlsAlA | Aluminiumoxide |
FeCl_3FeCl_{\placeholder{}}FeClFeCFeF | IJzer(III)chloride |
CaF_2CaF_{\placeholder{}}CaFCaC | Calciumfluoride |
Au_2S_3Au_2_3Au_2O_3A_2O_3_2O_3A_2O_3 | Goud(III)sulfide |
In BiNaS tabel 66B staan veelvoorkomende samengestelde ionen.
Een samengesteld ion bestaat uit meerdere niet-metalen die met atoombinding aan elkaar zitten, maar samen één geheel met één vaste lading vormen. Je behandelt het dus als één deeltje bij het benoemen en opstellen van formules.
Voorbeelden:(nitraat),(sulfaat),(fosfaat),(ammonium)
Bij het opstellen van formules:
•Zorg dat totale pluslading = totale minlading.
•Gebruik de lading van het samengestelde ion als geheel.
•Gebruik haakjes als er meerdere samengestelde ionen nodig zijn.
Voorbeeld: ,de haakjes zorgen ervoor dat het hele nitraation twee keer wordt genomen.
Het maken van zoutformules
Om de formules van zouten correct op te stellen, wat ook wel bekend staat als de verhoudingsformule of ionformule, moet je naar de balans tussen het aantal positief en negatief geladen ionen kijken. Deze balans zorgt ervoor dat het zout elektrisch neutraal is. De elektrovalentie is essentieel, wat aangeeft hoeveel elektronen een atoom opneemt of afstaat om aan de octetregel te voldoen en daardoor een ion wordt.
Richtlijnen voor ionladingen:
•Groep 1-metalen vormen -ionen
•Groep 2-metalen vormen -ionen
•Groep 16-niet-metalen vormen-ionen
•Groep 17-niet-metalen vormen-ionen
Voor elementen die niet in groep 1, 2, 16 of 17 staan (zoals overgangsmetalen), kun je de ionlading niet direct uit het groepsnummer afleiden. In dat geval moet je de lading opzoeken in BiNaS tabel 40A.
Dit is vooral belangrijk bij metalen zoals: aluminium (), ijzer (of) en goud (of).














