Een katalysator wordt verbruikt tijdens een reactie.
Leerdoelen
•Je kunt de vijf factoren die de reactiesnelheid bepalen benoemen en hun invloed uitleggen.
•Je kunt met het botsende deeltjesmodel de invloed van de verdelingsgraad, concentratie en temperatuur op de reactiesnelheid verklaren.
•Je kunt in een energiediagram de invloed van een katalysator op de activeringsenergie aanwijzen en uitleggen.
Factoren die de reactiesnelheid beïnvloeden
Verdelingsgraad
De verdelingsgraad bepaalt het reactieoppervlak. Hoe groter het oppervlak waarop de deeltjes kunnen reageren, hoe hoger de reactiesnelheid. Denk maar aan het kauwen van voedsel: door het in kleinere stukjes te verdelen, vergroot je het oppervlak voor de spijsverteringsenzymen, waardoor het sneller verteerd wordt.
Soort stof
Niet alle stoffen reageren met dezelfde snelheid. De soort stof is een bepalende factor voor hoe snel een reactie plaatsvindt. De soort stof bepaalt de hoogte van de activeringsenergie en een lagere activeringsenergie leidt tot een snellere reactie. Dit hangt samen met de stabiliteit van de deeltjes en de sterkte van de chemische bindingen die verbroken moeten worden.
Concentratie
Een hogere concentratie van reactanten leidt tot een hogere reactiesnelheid. Dit komt doordat meer deeltjes dicht bij elkaar zijn, waardoor de kans op botsingen tussen de reactieve deeltjes toeneemt. Vergelijk het met een drukke dansvloer: hoe meer mensen er zijn, hoe groter de kans dat ze tegen elkaar aan botsen.
Temperatuur
Temperatuur speelt ook een essentiële rol. Wanneer de temperatuur toeneemt, bewegen deeltjes sneller en botsen ze harder tegen elkaar, waardoor de kans op een effectieve botsing toeneemt. Dit resulteert in een hogere reactiesnelheid.
Katalysator
Een katalysator of enzym verhoogt de reactiesnelheid zonder zelf verbruikt te worden. Dit gebeurt doordat de katalysator de activeringsenergie verlaagt die nodig is om een reactie te laten plaatsvinden.
Het botsende deeltjesmodel
Volgens het botsende deeltjesmodel vinden reacties plaats wanneer deeltjes botsen met een energie die groot genoeg is om een reactie te veroorzaken. Ineffectieve botsingen veranderen niets; de deeltjes botsen, maar reageren niet. Effectieve botsingen daarentegen resulteren in de vorming van reactieproducten. Hoe meer botsingen er plaatsvinden, hoe groter ook het aantal effectieve botsingen zal zijn, wat leidt tot een hogere reactiesnelheid.
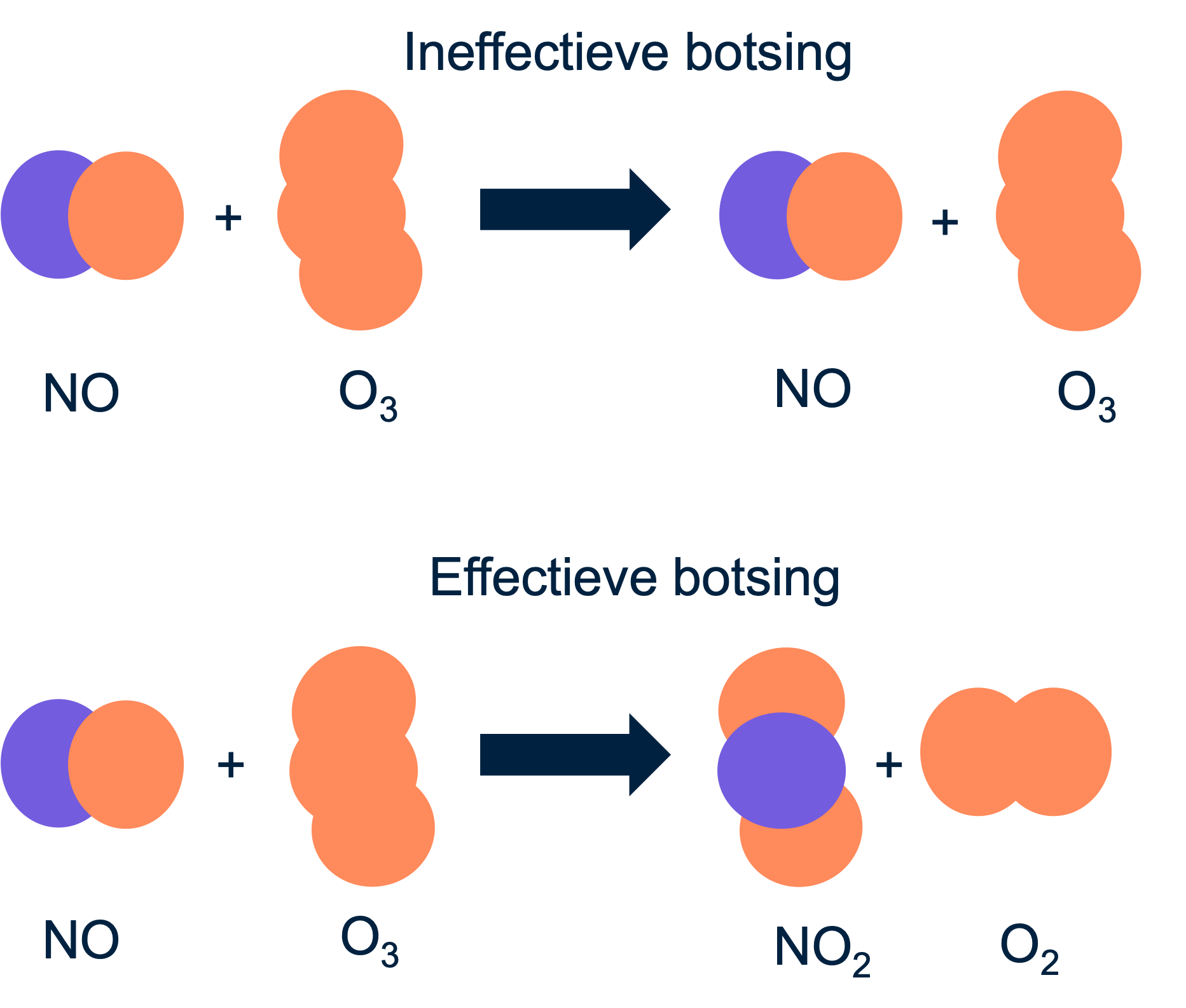
Een hogere verdelingsgraad en concentratie leiden tot meer botsingen (en dus meer effectieve botsingen), terwijl een hogere temperatuur leidt tot hardere en energierijkere botsingen, waardoor de kans op een effectieve botsing per botsing toeneemt.
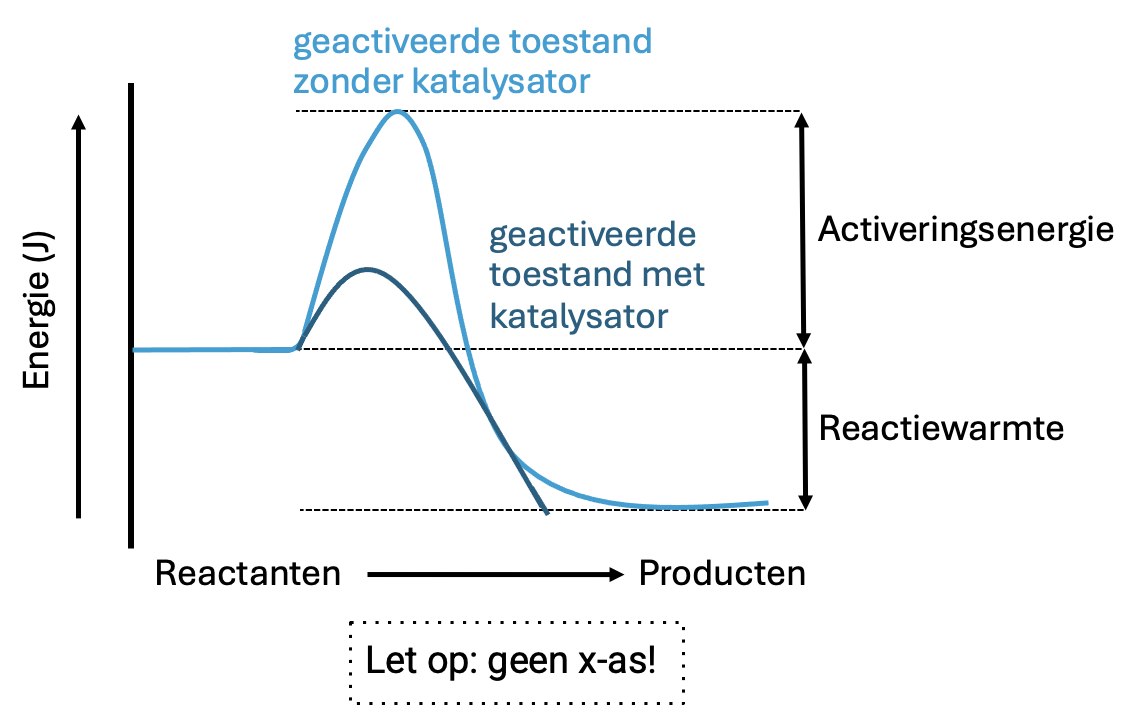
Het energiediagram
Een energiediagram laat de activeringsenergie zien, de energie die nodig is om een reactie te starten. De activeringsenergie loopt van het energieniveau van de beginstoffen tot de top van de energiebarrière in het diagram. Hoe hoger de activeringsenergie, hoe langzamer de reactie. Een katalysator verlaagt de activeringsenergie, waardoor de reactie sneller verloopt. In een energiediagram is de activeringsenergie met een katalysator lager dan zonder katalysator.