Wat is het verschil tussen 1,2-additie en 1,4-additie?
Leerdoelen
•Je kunt het radicaalmechanisme van een additiereactie beschrijven.
•Je kunt het ionair mechanisme van een additiereactie beschrijven.
•Je kunt uitleggen hoe 1,2- en 1,4-additie plaatsvinden bij buta-1,3-dieen.
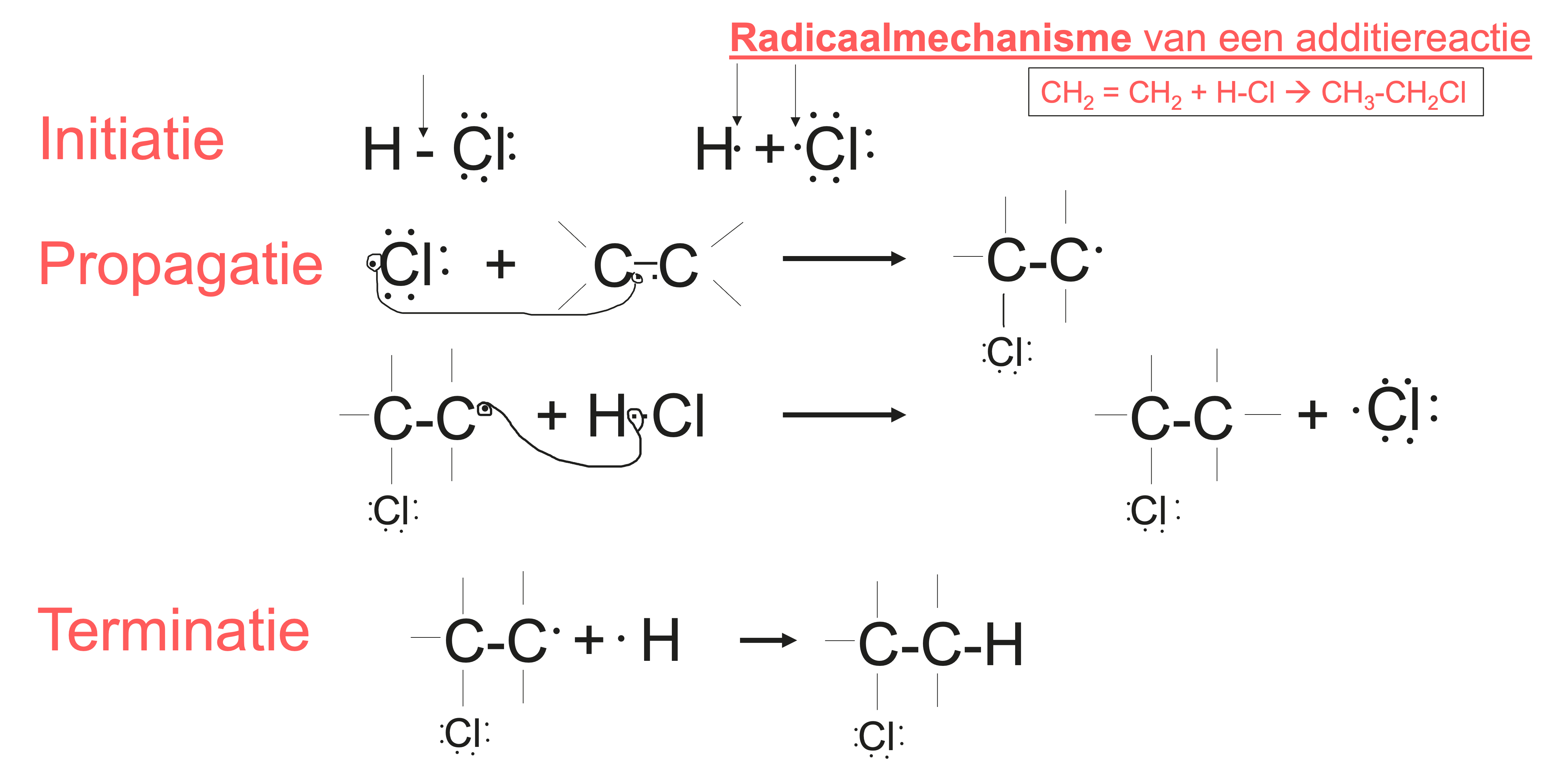
Het radicaalmechanisme in focus
Initiatiefase: de basis leggen
In de initiatiefase wordt een atoombinding van een molecuul homolytisch verbroken, waardoor twee radicalen ontstaan. Een radicaal is een deeltje met een ongepaard elektron. Deze fase start de kettingreactie.
Propagatiefase: de kern van de reactie
In de propagatiefase reageert een radicaal met een stabiel molecuul, waarbij een nieuwe binding en een nieuw radicaal ontstaan. Omdat er steeds een nieuw radicaal wordt gevormd, kan de reactie als kettingreactie doorgaan.
Terminatiefase: het eindresultaat
In de terminatiefase reageren twee radicalen met elkaar tot een stabiel molecuul. Hierdoor blijven er geen radicalen meer over en stopt de kettingreactie.
Het ionair mechanisme onder de loep
Reactie tussen etheen en chloor
Een ander mechanisme, het ionair mechanisme, treedt in werking zodra er ionen bij betrokken zijn. Als voorbeeld nemen we de reactie tussen etheen en chloor. In deze reactie wordt 1,2-dichloorethaan gevormd, waarbij aan elk van de twee koolstofatomen van de oorspronkelijke dubbele binding een chlooratoom wordt gebonden.
De rol van dubbele bindingen en polarisatie
De dubbele binding van etheen kan een chloormolecuul aantrekken en polariseren, doordat de elektronen van de dubbele binding de elektronen van het chloormolecuul wegduwen. Hierdoor wordt één chlooratoom gedeeltelijk positief geladen en het andere gedeeltelijk negatief.
De dubbele binding valt vervolgens het gedeeltelijk positieve chlooratoom aan. Daarbij ontstaat een chloride-ion () en een carbocation-intermediair, waarbij één koolstofatoom positief geladen is en het andere aan een chlooratoom gebonden is. Daarna valt het chloride-ion het positief geladen koolstofatoom aan, waardoor uiteindelijk 1,2-dichloorethaan ontstaat.

Meer dan één reactieproduct: het geval van buta-1,3-dieen
Een interessante observatie bij additiereacties is dat sommige beginstoffen tot meer dan één reactieproduct kunnen leiden. Een voorbeeld hiervan is de reactie van buta-1,3-dieen met chloormoleculen. Afhankelijk van hoe de reactie verloopt, kan dit leiden tot zowel 1,2-additie als 1,4-additie.
Mesomerie: een sleutelbegrip
De variatie in reactieproducten is mede te danken aan mesomerie binnen moleculen, waardoor de positie van dubbele bindingen en ladingen kan verschuiven. Hierdoor kan de positieve lading zich binnen het molecuul verplaatsen, waardoor het chloride-ion op verschillende plaatsen kan binden. Dit leidt uiteindelijk tot verschillende additieproducten.














