Hoeveel valentie elektronen heeft C_2O_4^{\;\;2-}C_2O_4^{\;2-}C_2O_4^{2-}C_2O_4^2C_2O_4C_2O_4^{}C_2O_4C_2O_42C_2O_42-C_2O2-C_2O42-C_2O442-C_2O42-C_2O42-CO42- (oxalaat)
Wat is mesomerie?
In de wereld van scheikunde is het begrip mesomerie of resonantie van cruciaal belang om de stabiliteit van moleculen te begrijpen. Mesomerie helpt ons uit te leggen waarom sommige organische verbindingen, zoals azijnzuur en fenol kunnen functioneren als zuren, terwijl anderen, zoals ethanol, dat niet kunnen. Mesomere grensstructuren zijn alternatieve Lewisstructuren van een molecuul die aantonen hoe elektronen binnen het molecuul kunnen worden verplaatst om verschillende configuraties te vormen.
Het azijnzuurion: Een voorbeeld van mesomerie
Wanneer azijnzuur (CH3COOH) een H+ ion afstaat, wordt het een azijnzuurion (CH3COO-). Dit ion toont duidelijk mesomerie; het elektronenpaar op de zuurstof (O) kan zich verplaatsen naar de C=O dubbele binding, wat resulteert in twee verschillende Lewisstructuren. Deze structuren laten zien dat de negatieve lading verdeeld wordt over twee zuurstofatomen, wat bijdraagt aan de stabiliteit van het molecuul.
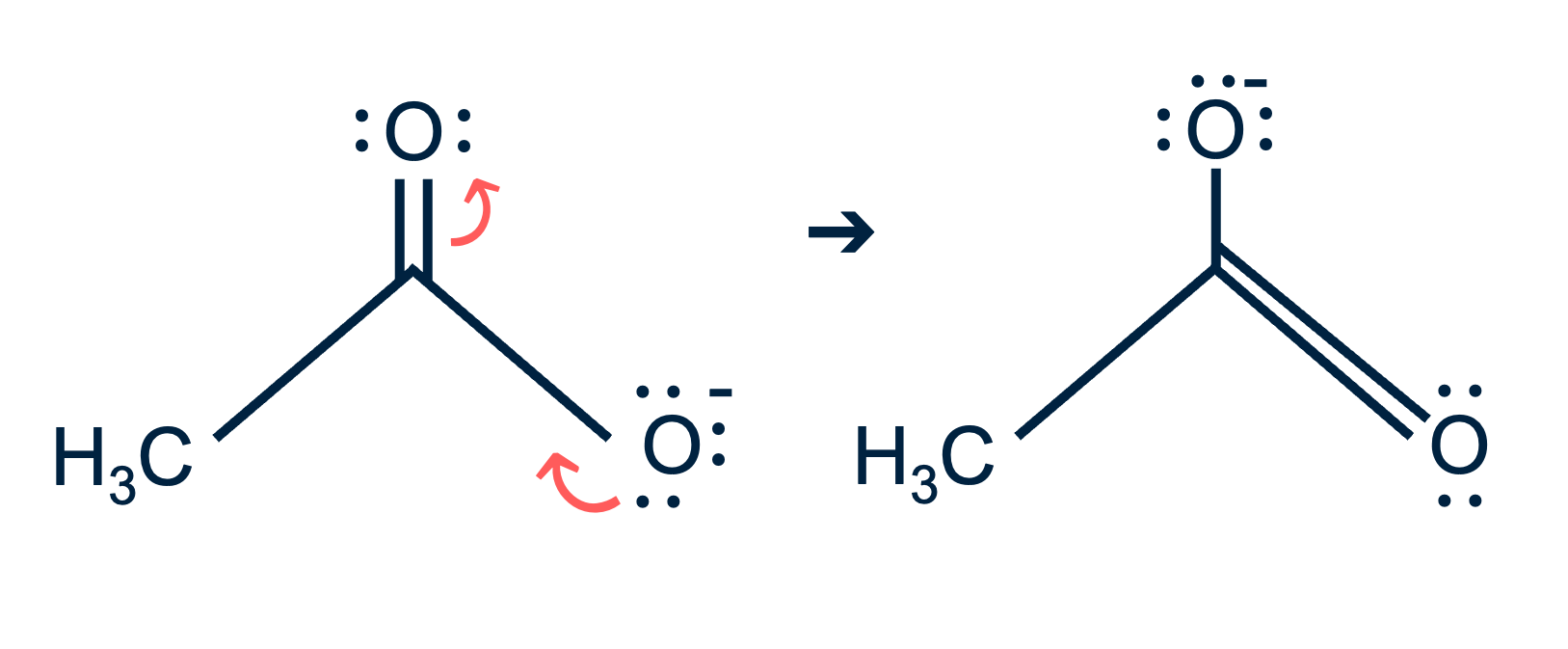
Mesomerie in benzeen
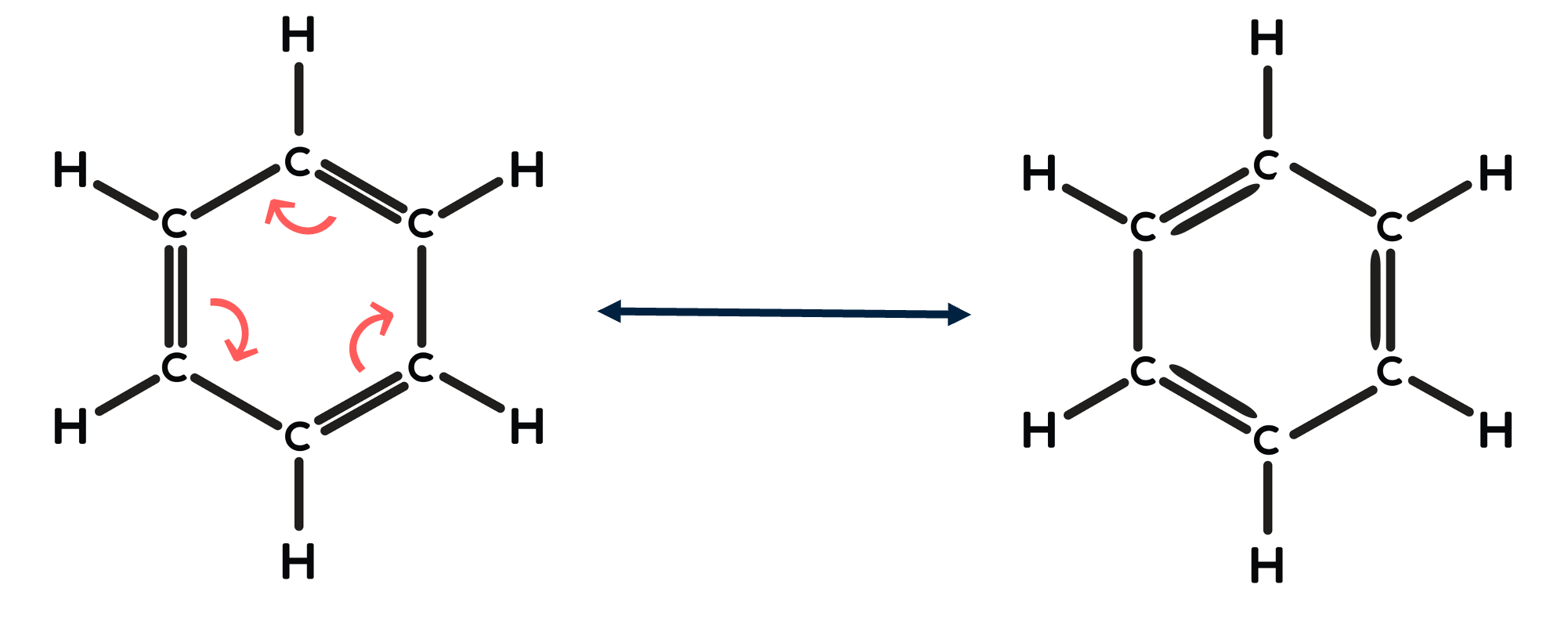
Een klassiek voorbeeld van mesomerie is te vinden in benzeen (C6H6). Benzeen heeft een ringstructuur met afwisselend enkele en dubbele bindingen tussen de koolstofatomen. Door de dubbele bindingen te verschuiven, kunnen verschillende grensstructuren worden gegenereerd. In realiteit is de elektronenverdeling gelijkmatig, waardoor alle bindingen identiek zijn, wat de uitzonderlijke stabiliteit van benzenen verklaart.
Carbonaat Ion: Een ander voorbeeld
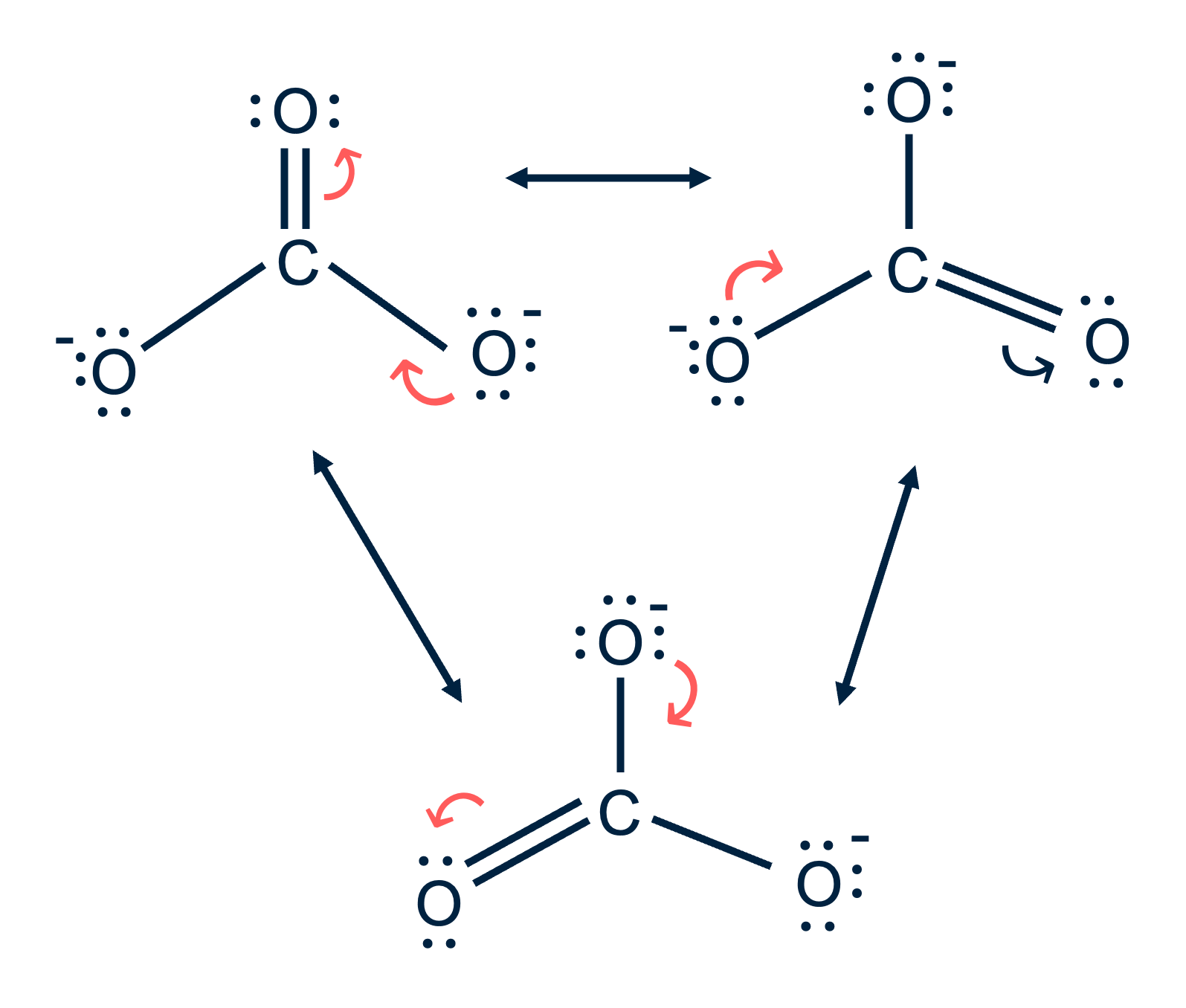
Het carbonaat ion (CO32-) demonstreert ook mesomerie met drie mogelijke grensstructuren door het verschuiven van dubbele bindingen en elektronenparen op zuurstofatomen. Dit toont aan dat, net als bij azijnzuurion en benzenen, de stabiliteit van het carbonaat ion wordt vergroot door de verdeling van de lading over meerdere atomen.
Algemene principes van mesomere grensstructuren
Het opstellen van mesomere grensstructuren volgt enkele fundamentele stappen:
1.Elektronenpaar naar pi-binding: Een ongebonden elektronenpaar op een atoom kan verplaatsen om een pi-binding (een dubbele binding) met een aangrenzend atoom te vormen.
2.Pi-binding wordt een nieuwe pi-binding: Een bestaande pi-binding kan zich verplaatsen naar een aangrenzend atoom om een nieuwe pi-binding te vormen.
3.Pi-binding naar ongebonden paar: Een pi-binding kan worden omgezet in een ongebonden paar op een aangrenzend atoom.
Deze principes laten zien hoe elektronen binnen een molecuul zich kunnen verplaatsen om verschillende structuren te vormen, wat bijdraagt aan de algehele stabiliteit van het molecuul.













