Welke van de volgende reacties is een voorbeeld van een exotherme reactie?
Leerdoelen
•Je kunt een (endotherm en exotherm) energiediagram schetsen.
•Je kunt aangeven wat de activeringsenergie is.
•Je kunt met het botsende-deeltjesmodel de invloed van concentratie, temperatuur en verdelingsgraad verklaren.
Endotherme en exotherme reacties
Elke chemische reactie heeft een energie-effect. Er zijn twee soorten reacties:
•Endotherme reacties: hierbij is energie nodig om de reactie te laten verlopen. Denk aan fotolyse, thermolyse en elektrolyse. Dit zijn ontledingsreacties, waarbij één beginstof wordt omgezet in meerdere reactieproducten. De energiebronnen kunnen zijn:
1.Fotolyse: licht als energiebron
2.Thermolyse: warmte als energiebron
3.Elektrolyse: elektriciteit als energiebron
•Exotherme reacties: hierbij komt energie vrij. Verbrandingsreacties zijn hier een goed voorbeeld van. Ze geven warmte af en worden gebruikt in bijvoorbeeld centrale verwarming of bij het koken van een ei.
Energiediagrammen
Om de energieverandering bij een reactie weer te geven, gebruiken we een energiediagram.
Belangrijke elementen in een energiediagram:
•Verticale as (y-as): geeft de energie weer
•Beginstoffen: startniveau van de energie
•Reactieproducten: eindniveau van de energie
•Activeringsenergie: de energie die nodig is om de reactie te laten beginnen
•Geactiveerde toestand: overgangsfase tussen beginstoffen en reactieproducten
•Reactiewarmte: verschil in energie tussen beginstoffen en reactieproducten
Endotherm vs. Exotherm in een diagram
Endotherme reactie: het energieniveau van de reactieproducten ligt hoger dan dat van de beginstoffen.
Exotherme reactie: het energieniveau van de reactieproducten ligt lager dan dat van de beginstoffen.
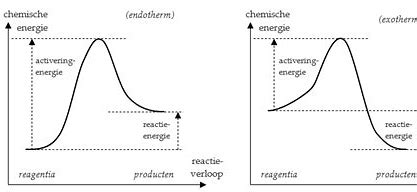
Activeringsenergie
Elke chemische reactie heeft een activeringsenergie nodig. Dit is de energie die nodig is om een reactie op gang te brengen. Een voorbeeld hiervan is het ontsteken van een lucifer om gas te laten branden. Zonder die eerste energiebron zou het gas niet vanzelf ontbranden.
Reactiesnelheid en het botsende deeltjesmodel
De reactiesnelheid bepaalt hoe snel beginstoffen verdwijnen en reactieproducten ontstaan. Dit kunnen we verklaren met het botsende deeltjesmodel.
Effectieve en ineffectieve botsingen
•Een effectieve botsing leidt tot een chemische reactie.
•Een ineffectieve botsing gebeurt wanneer de deeltjes elkaar raken, maar niet voldoende energie hebben om te reageren.
Hoe meer botsingen er plaatsvinden, hoe groter de kans op een effectieve botsing en hoe sneller de reactie verloopt.
Factoren die de reactiesnelheid beïnvloeden
De reactiesnelheid wordt beïnvloed door:
1. Verdelingsgraad
Hoe fijner een stof verdeeld is, hoe groter het reactieoppervlak en hoe meer botsingen er kunnen plaatsvinden. Voorbeeld: Kauwen van voedsel vergroot het oppervlak, waardoor vertering sneller verloopt.
2. Concentratie
Hoe hoger de concentratie van de beginstoffen, hoe meer botsingen er per seconde kunnen plaatsvinden en hoe sneller de reactie verloopt. Voorbeeld: Een hogere zuurgraad in de maag zorgt voor snellere vertering van voedsel.
3. Temperatuur
Bij een hogere temperatuur bewegen de deeltjes sneller en botsen ze harder. Dit vergroot de kans op effectieve botsingen en versnelt de reactie. Voorbeeld: Een reactie verloopt sneller bij 80 °C dan bij kamertemperatuur.
Waarom hebben mensen tanden en kiezen?
Tanden en kiezen helpen om voedsel te malen en te verkleinen, waardoor de verdelingsgraad groter wordt. Hierdoor kunnen maagsappen beter inwerken op het voedsel en vindt de chemische vertering sneller plaats. Dit is een praktisch voorbeeld van het botsende deeltjesmodel in het dagelijks leven.













