De reagentia in een brandstofcel
Wat is de oxidator en wat is de reductor in een brandstofcel?


 Thijs Brouwer
Thijs BrouwerTest je kennis met de 3 examenvragen die aan dit onderwerp zijn gekoppeld.
Wat is de oxidator en wat is de reductor in een brandstofcel?
•Welke vaste kenmerken een brandstofcel heeft
•Hoe een brandstofcel werkt
Een brandstofcel is een apparaat dat chemische energie omzet in elektrische energie door middel van een elektrochimische reactie. Bij deze reactie worden brandstoffen zoals koolwaterstoffen (bijvoorbeeld methaan, ethaan of propaan) gebruikt en zuurstof uit de lucht als oxidator.
Om de werking van een brandstofcel goed te begrijpen, is het belangrijk om het verschil met een accu te kennen. Een brandstofcel vereist dat de beginstoffen continu worden aangevoerd. Dit betekent dat er stofjes naar binnen gaan en andere stofjes naar buiten komen. In een autoaccu daarentegen, is het een gesloten systeem; er hoeft geen zuurstof verbruikt te worden omdat de reacties binnenin de accu plaatsvinden zonder externe aanvoer van stoffen.
Een brandstofcel bestaat uit twee halfcellen die gescheiden zijn door een membraan. Dit membraan laat bepaalde ionen door, maar voorkomt dat de oxidator en reductor zich mengen.
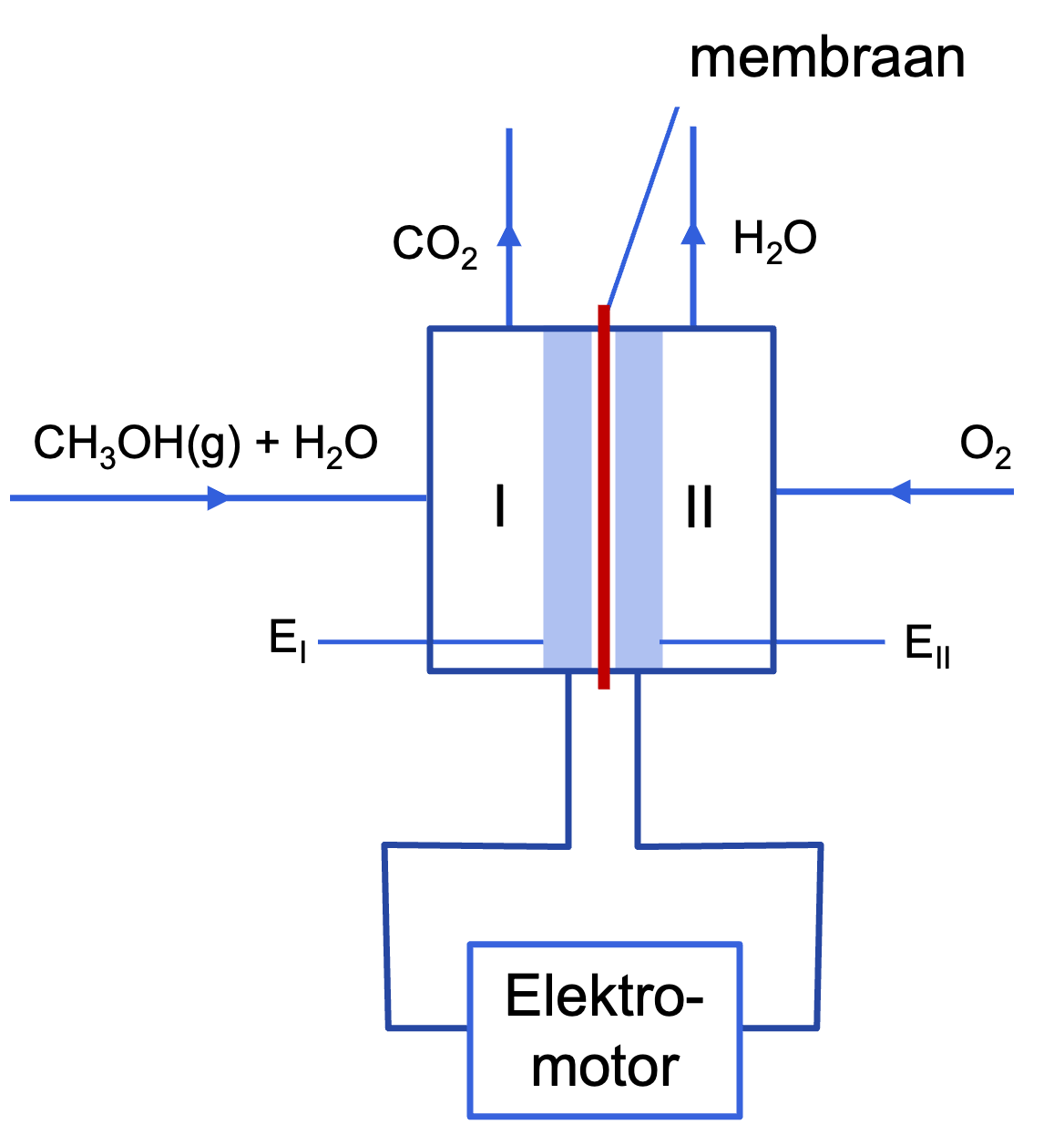
•Oxidator: Zuurstof (O2) uit de lucht.
•Reductor: Koolwaterstoffen zoals methanol of andere organische verbindingen.
In de halfcel waar zuurstof werkt als oxidator, verloopt de onderstaande reactie: O_2+4H^{+}+4e^{-}\to2H_2OO_2+4H^{+}+4e^{-}\to2H_2O_2+4H^{+}+4e^{-}\to2HO_2+4H^{+}+4e^{-}\to2O_2+4H^{+}+4e^{-}\toO_2+4H^{+}+4e^{-}-O_2+4H^{+}+4e^{-}O_2+4H^{+}+4eO_2+4H^{+}+4O_2+4H^{+}+O_2+4H^{+}O_2+4HO_2+4O_2+O_2OOO-O-2O-O
Hierbij gaat zuurstof naar binnen en water naar buiten.
In de halfcel waar methanol als reductor werkt, is de reactie: CH_3OH+H_2O\to CO_2+6H^{+}+6e^{-}C_{}H_3OH+H_2O\to CO_2+6H^{+}+6e^{-}C_3H_3OH+H_2O\to CO_2+6H^{+}+6e^{-}C_3H_3OH+H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_3OH+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_{83}OH+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8OH+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8O+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8O_{}+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8O_3+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8O_3+3H_2O\to3CO_2+6H^{+}+6e^{-v}C_3H_8O_3+3H_2O\to3CO_2+6H^{+}+6e^{-}C_3H_8O_3+3H_2O\to3CO_2+6H^{+}+6eC_3H_8O_3+3H_2O\to3CO_2+6H^{+}+6C_3H_8O_3+3H_2O\to3CO_2+6H^{+}+C_3H_8O_3+3H_2O\to3CO_2+6H^{+}C_3H_8O_3+3H_2O\to3CO_2+6HC_3H_8O_3+3H_2O\to3CO_2+6C_3H_8O_3+3H_2O\to3CO_2+C_3H_8O_3+3H_2O\to3CO_2C_3H_8O_3+3H_2O\to3COC_3H_8O_3+3H_2O\to3CC_3H_8O_3+3H_2O\to3C_3H_8O_3+3H_2O\toC_3H_8O_3+3H_2O-C_3H_8O_3+3H_2O-?C_3H_8O_3+3H_2O-C_3H_8O_3+3H_2OC_3H_8O_3+3H_2C_3H_8O_3+3HC_3H_8O_3+3C_3H_8O_3+C_3H_8O_3C_3H_8OC_3H_8C_3HC_3C
Om een totaalreactie op te stellen, moeten de halfreacties bij elkaar worden opgeteld. Het hogere aantal elektronen in de reductor halfvergelijking dwingt ons om deze reactie aan te passen. De uiteindelijke reactie is:
2CH_3OH+3O_2\to2CO_2+4H_2O2CH_3OH+3O_2\to2CO_2+4H_22CH_3OH+3O_2\to2CO_2+4H2CH_3OH+3O_2\to2CO_2+42CH_3OH+3O_2\to2CO_2+2CH_3OH+3O_2\to2CO_22CH_3OH+3O_2\to2CO2CH_3OH+3O_2\to2CO-2CH_3OH+3O_2\to2CO2CH_3OH+3O_2\to2C2CH_3OH+3O_2\to22CH_3OH+3O_2\to2CH_3OH+3O_2-2CH_3OH+3O_22CH_3OH+3O_{}2CH_3OH+3O_32CH_3OH+3O2CH_3OH+32CH_3OH+2CH_3OH2CH_3O2CH_32CH2C2
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







