Geef de naam van de volgende stoffen (check wel of het moleculaire stoffen zijn).
1.
2.
3.
4.


 Thijs Brouwer
Thijs BrouwerTest je kennis met de examenvraag die aan dit onderwerp is gekoppeld.
Geef de naam van de volgende stoffen (check wel of het moleculaire stoffen zijn).
1.
2.
3.
4.
•Je kunt de naamgeving van een aantal moleculaire stoffen reproduceren.
•Je kunt uitleggen hoe een atoombinding (covalente binding) wordt gevormd en deze weergeven met een streepje in een structuurformule.
•Je kunt de covalentie van een atoomsoort afleiden uit het periodiek systeem.
•Je kunt bepalen of een binding polair of apolair is op basis van het verschil in elektronegativiteit.
In de scheikunde maken we onderscheid tussen verschillende soorten stoffen. Een belangrijke categorie zijn de moleculaire stoffen. Dit zijn stoffen die uitsluitend bestaan uit niet-metalen. Ze vormen moleculen waarin atomen door atoombindingen aan elkaar vastzitten. Zodra er een metaalatoom in de verbinding zit, spreken we van een zout en gelden andere regels.
Bij de naamgeving van moleculaire stoffen gebruiken we specifieke voorvoegsels om aan te geven hoe vaak een atoomsoort in de molecuulformule voorkomt. Deze voorvoegsels zijn telwoorden:
aantal atomen | naamgeving |
|---|---|
1 | mono |
2 | di |
3 | tri |
4 | tetra |
5 | penta |
6 | hexa |
7 | hepta |
8 | octa |
9 | nona |
10 | deca |
Een belangrijke regel is dat het voorvoegsel 'mono' wordt weggelaten als het de eerste atoomsoort in de formule betreft. Voorbeelden:
•NO: stikstofmonoxide (niet monostikstofmonoxide)
•NO2: stikstofdioxide (niet monostikstofdioxide)
•P2O3: difosfortrioxide
•SiCl4: siliciumtetrachloride (niet monosiliciumtetrachloride)
•H2S: diwaterstofsulfide
Let op: deze telwoorden gebruik je alleen bij moleculaire stoffen (dus tussen niet-metalen). Bij zouten, die bestaan uit een metaal en een niet-metaal, gebruik je geen telwoorden. Zo is Na2S gewoon natriumsulfide, en niet dinatriumsulfide.
Atomen streven naar een edelgasconfiguratie. Dit betekent dat ze een gevulde buitenste elektronenschil willen hebben, net als de edelgassen (groep 18 in het periodiek systeem). Een gevulde schil maakt een atoom stabiel. De eerste elektronenschil kan maximaal twee elektronen bevatten, terwijl de tweede en derde schil (voor de meeste atomen die we hier bespreken) acht elektronen kunnen bevatten om stabiel te zijn.
Om een gevulde buitenste schil te krijgen, kunnen atomen elektronen met elkaar delen. Dit delen van elektronen vormt een atoombinding, ook wel covalente binding genoemd.
Neem bijvoorbeeld waterstof (H). Een waterstofatoom heeft één proton en één elektron. De eerste schil wil twee elektronen hebben om op helium te lijken. Als twee waterstofatomen bij elkaar komen, kunnen ze elk hun ene elektron inbrengen en deze twee elektronen met elkaar delen. Deze twee gedeelde elektronen draaien dan om beide kernen heen, waardoor beide waterstofatomen het gevoel hebben dat ze twee elektronen in hun buitenste schil hebben.
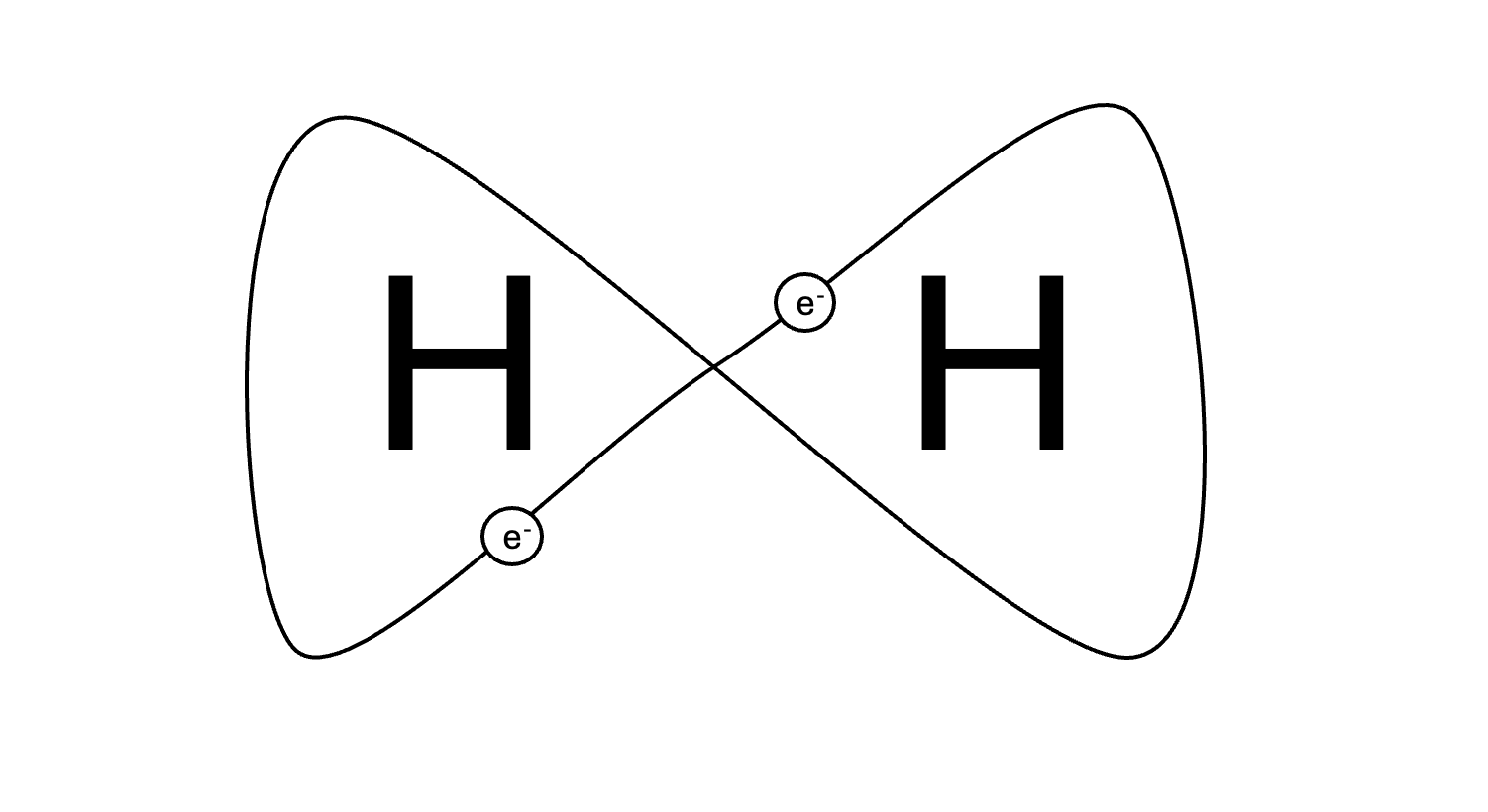
In een structuurformule wordt een atoombinding weergegeven met een streepje. Dit streepje staat voor twee bindingselektronen die door de twee atomen worden gedeeld.
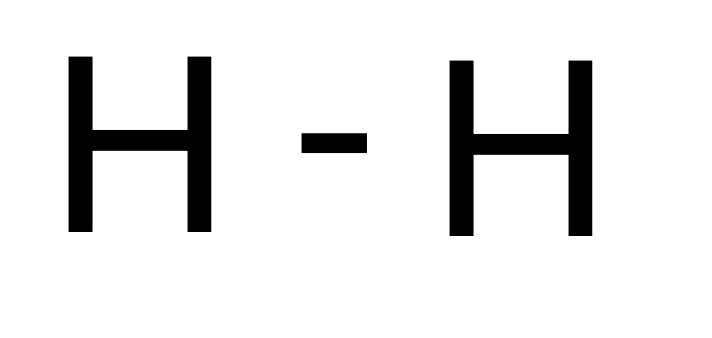
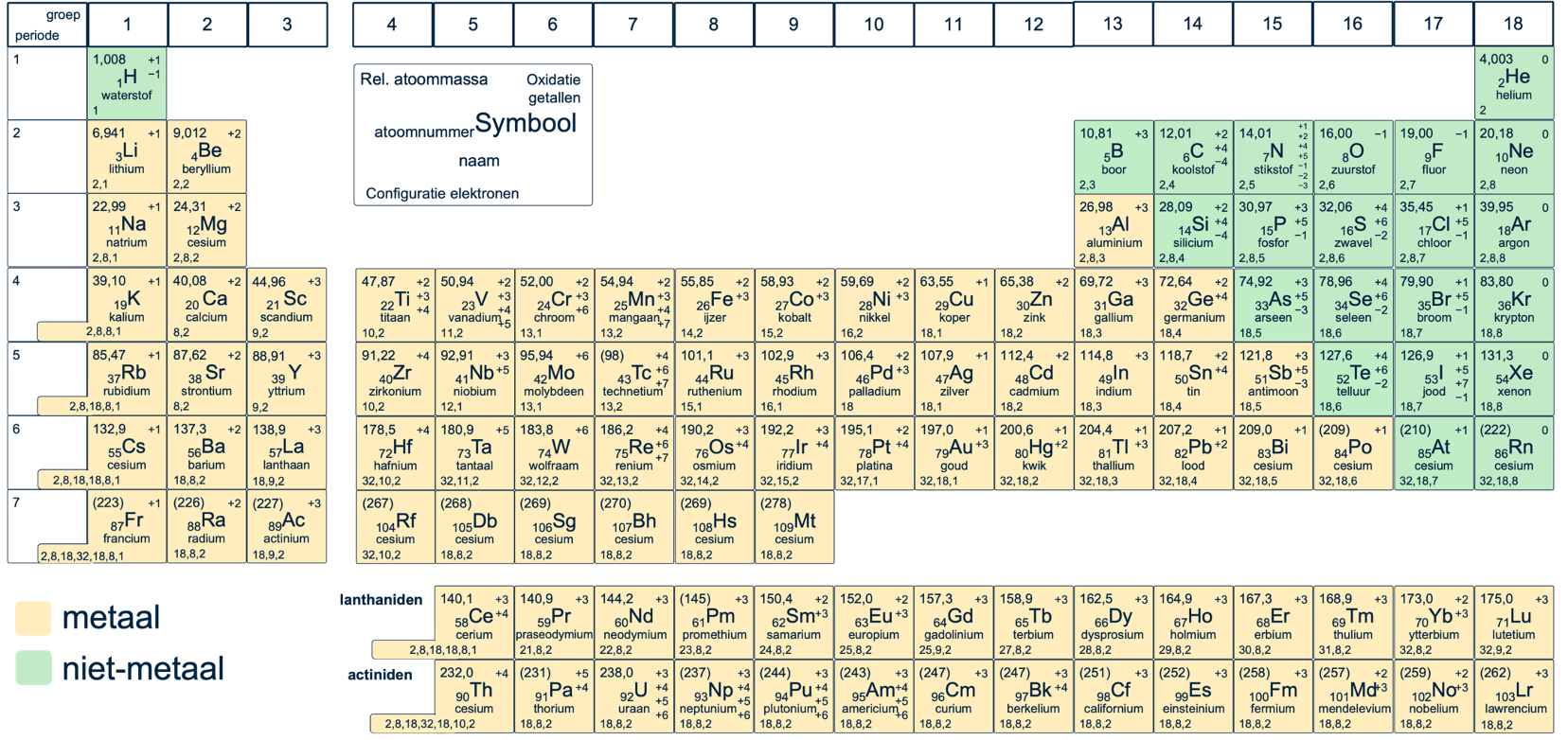
De covalentie van een atoom is het aantal elektronen dat het atoom nodig heeft om een edelgasconfiguratie te bereiken. Dit is tevens het aantal atoombindingen dat het atoom aangaat. Je kunt de covalentie afleiden uit het periodiek systeem:
•Atomen in groep 17 (halogenen) hebben 7 elektronen in hun buitenste schil en willen er 1 bij. Hun covalentie is 1.
•Atomen in groep 16 (zoals zuurstof) hebben 6 elektronen in hun buitenste schil en willen er 2 bij. Hun covalentie is 2.
•Atomen in groep 15 (zoals stikstof) hebben 5 elektronen in hun buitenste schil en willen er 3 bij. Hun covalentie is 3.
•Atomen in groep 14 (zoals koolstof) hebben 4 elektronen in hun buitenste schil en willen er 4 bij. Hun covalentie is 4.
•Waterstof (H) heeft 1 elektron en wil er 1 bij (om op helium te lijken). Zijn covalentie is 1.
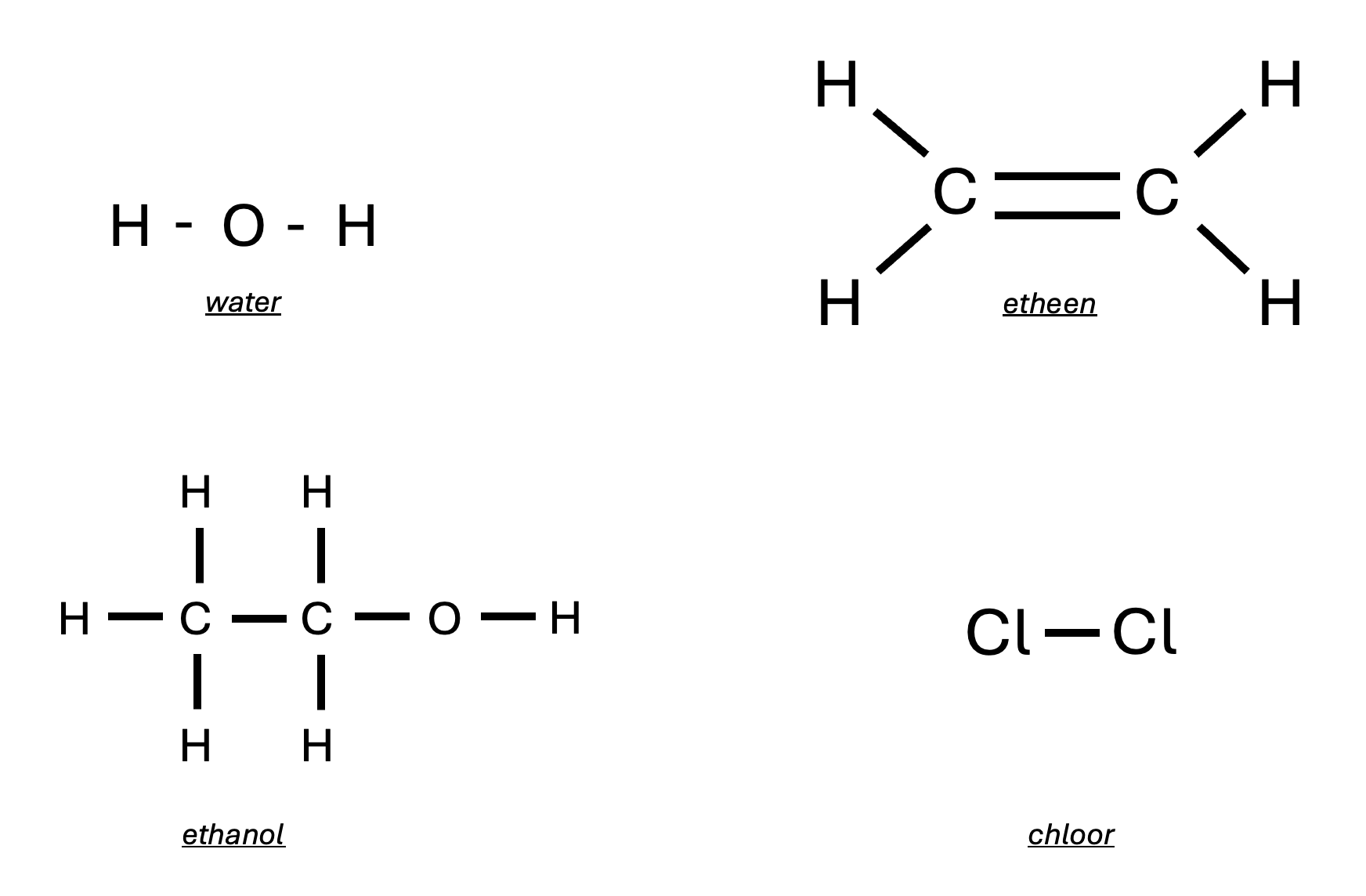
Laten we kijken naar enkele voorbeelden:
•Water (H₂O): Zuurstof heeft een covalentie van 2 (wil 2 elektronen erbij), waterstof heeft een covalentie van 1 (wil 1 elektron erbij). Zuurstof gaat twee bindingen aan, elk met een waterstofatoom. Zo heeft zuurstof 8 elektronen in zijn buitenste schil (2 van zichzelf + 2 x 1 van waterstof) en elk waterstofatoom 2 elektronen (1 van zichzelf + 1 van zuurstof).
•Etheen (C₂H₄): Koolstof heeft een covalentie van 4, waterstof van 1. In etheen vormen de twee koolstofatomen een dubbele binding met elkaar, en elk koolstofatoom vormt twee enkele bindingen met waterstofatomen. Alle atomen voldoen aan hun covalentie.
•Ethanol (C₂H₆OH): Koolstof heeft covalentie 4, waterstof 1, zuurstof 2. Koolstof bindt aan drie waterstofatomen en één zuurstofatoom. Het zuurstofatoom bindt op zijn beurt aan één waterstofatoom.
•Chloor (Cl₂): Chloor heeft een covalentie van 1. Twee chlooratomen delen elk één elektron, waardoor ze een enkele binding vormen en beide 8 elektronen in hun buitenste schil hebben.
In al deze voorbeelden delen de atomen elektronen op zo'n manier dat ze allemaal een gevulde buitenste schil krijgen en daarmee op een edelgas lijken.
Niet alle atomen trekken even hard aan de gedeelde elektronen in een atoombinding. De mate waarin een atoom aan een gemeenschappelijk elektronenpaar trekt, noemen we de elektronegativiteit (EN). Hoe hoger de elektronegativiteit, hoe harder een atoom trekt. Dit heeft invloed op de verdeling van de lading in een molecuul en daarmee op de oplosbaarheid van stoffen: polaire stoffen lossen op in polaire stoffen, en apolaire stoffen in apolaire stoffen (dus niet in elkaar). De elektronegativiteitswaarden van atomen zijn te vinden in tabellen, bijvoorbeeld in Binas tabel 40A.
Om te bepalen of een binding polair of apolair is, kijken we naar het verschil in elektronegativiteit (ΔEN) tussen de twee gebonden atomen. We berekenen dit door de grootste EN-waarde min de kleinste EN-waarde te doen.
Op basis van dit verschil maken we de volgende indeling:
•Apolair: Als het verschil in elektronegativiteit (ΔEN) kleiner is dan of gelijk is aan 0,4. De elektronen worden vrijwel gelijkmatig gedeeld.
•Polair: Als het verschil in elektronegativiteit (ΔEN) groter is dan 0,4, maar kleiner dan of gelijk is aan 1,7. De elektronen worden ongelijkmatig gedeeld, waardoor er een lichte positieve (δ+) en een lichte negatieve (δ-) lading ontstaat aan de uiteinden van de binding.
•Ionbinding: Als het verschil in elektronegativiteit (ΔEN) groter is dan 1,7. In dit geval is het verschil zo groot dat het ene atoom de elektronen volledig naar zich toetrekt en er ionen ontstaan. Dit is kenmerkend voor zouten.
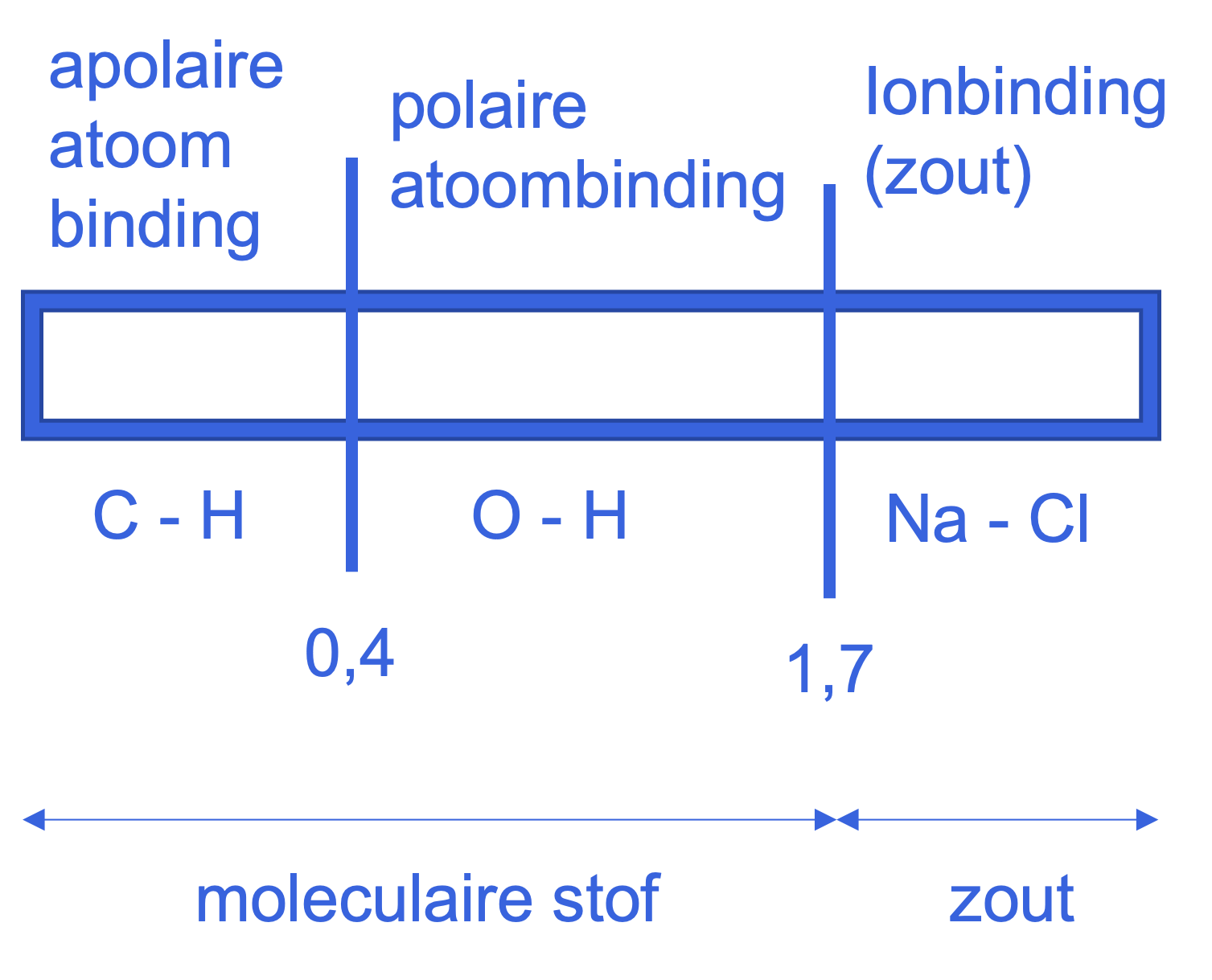
Laten we de EN-waarden gebruiken om het bindingstype te bepalen:
•C-H binding:
•EN(C) = 2,5
•EN(H) = 2,1
•ΔEN = 2,5 - 2,1 = 0,4
•Conclusie: De C-H binding is apolair.
•O-H binding:
•EN(O) = 3,5
•EN(H) = 2,1
•ΔEN = 3,5 - 2,1 = 1,4
•Conclusie: De O-H binding is polair.
•Na-Cl binding (in NaCl):
•EN(Cl) = 3,2
•EN(Na) = 0,9
•ΔEN = 3,2 - 0,9 = 2,3
•Conclusie: De Na-Cl binding is een ionbinding (en NaCl is dus een zout). Dit klopt, want het is een verbinding tussen een metaal (Na) en een niet-metaal (Cl).
De centrale vraag is: wat is de overeenkomst tussen een mens en een atoom? Net zoals mensen streven naar geluk, tevredenheid en stabiliteit, streven atomen ook naar een stabiele toestand. Voor atomen betekent dit het bereiken van een gevulde buitenste elektronenschil, de edelgasconfiguratie. Door atoombindingen aan te gaan en elektronen te delen, bereiken atomen deze "gelukkige" en stabiele toestand. Ze worden als het ware "blij" van gevulde schillen, net zoals mensen gelukkig willen zijn.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







