Noem de toestandsaanduidingen van stoffen en geef een korte uitleg bij elke aanduiding.
Leerdoelen
•Je kunt de fase en faseveranderingen van stoffen benoemen.
•Je kunt graden Celsius omzetten naar Kelvin en andersom.
•Je kunt het verschil tussen een mengsel en een zuivere stof aantonen.
De drie fasen van water
Water kan in drie fasen voorkomen:
•IJs (vast): Moleculen trillen op een vaste plek en bewegen niet langs elkaar heen.
•Water (vloeibaar): Moleculen kunnen vrij bewegen en blijven elkaar aanraken.
•Waterdamp (gas): Moleculen hebben geen contact meer met elkaar, nemen meer ruimte in en hebben een lagere dichtheid.
Toestandsaanduidingen
In de scheikunde worden stoffen aangeduid met toestandsaanduidingen:
•s voor solid (vast)
•l voor liquid (vloeibaar)
•g voor gas
•aq voor opgelost (aqua)
De fase van een stof wordt bepaald door de temperatuur. Een stof is vast als de temperatuur lager is dan het smeltpunt. Bij water is het smeltpunt 0 graden Celsius en het kookpunt is 100 graden Celsius.
Faseveranderingen
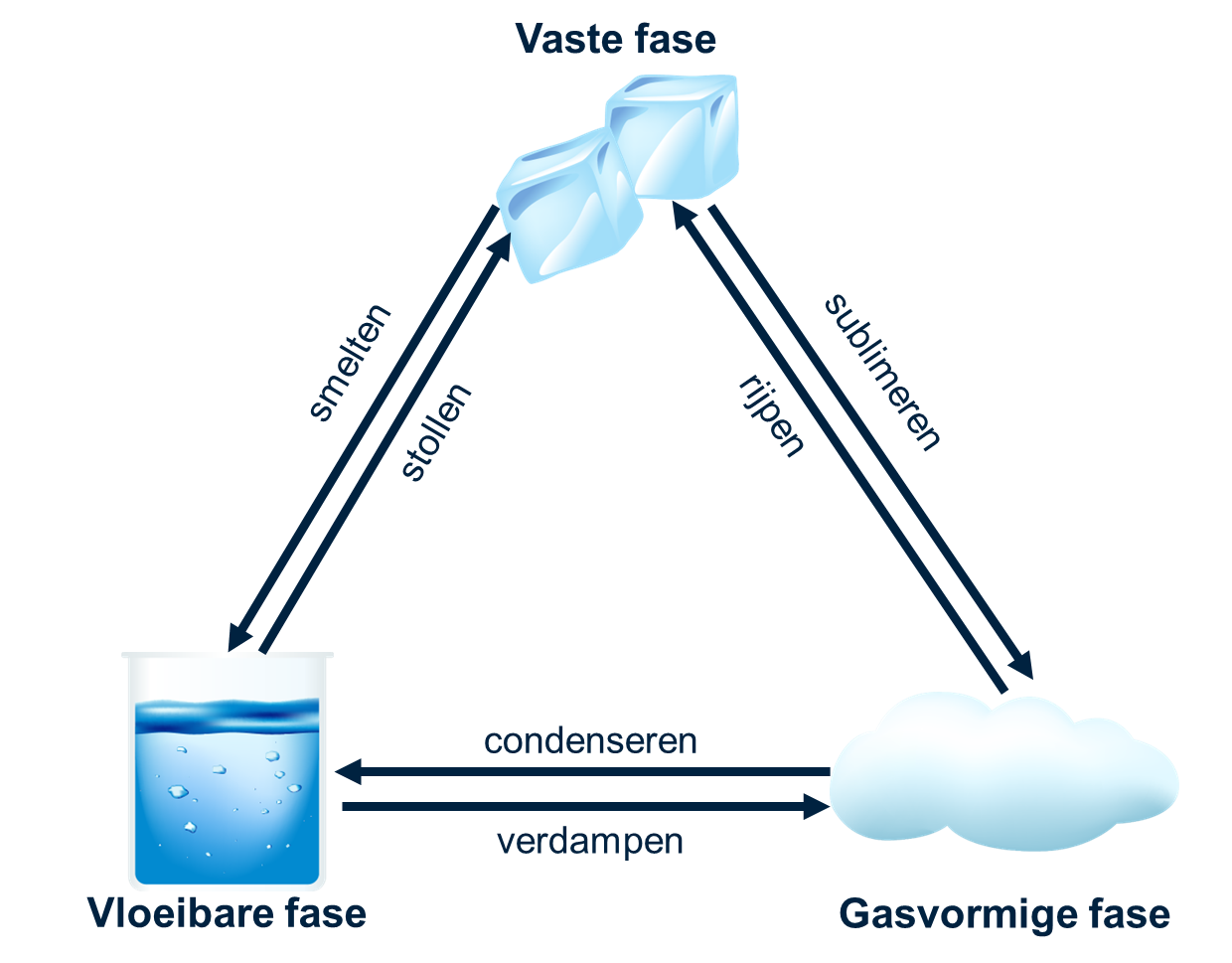
Faseveranderingen zijn de processen waarbij een stof van de ene fase naar de andere verandert. Belangrijke faseveranderingen zijn:
•Verdampen: Van vloeibaar naar gas.
•Condenseren: Van gas naar vloeibaar.
•Smelten: Van vast naar vloeibaar.
•Stollen: Van vloeibaar naar vast.
•Sublimeren: Van vast naar gas zonder vloeibare fase.
•Rijpen: Van gas naar vast (bijvoorbeeld ijsvorming op gras).
Temperatuurschalen
Graden Celsius en Kelvin
Er zijn verschillende temperatuurschalen, de meest bekende zijn celsiusschaal en de kelvinschaal.
•Celsius: Water kookt bij 100 graden en bevriest bij 0 graden.
•Kelvin: Deze schaal begint bij 0 Kelvin, wat het absolute nulpunt is waarbij alle moleculaire beweging stopt.
0 graden Celsius is dus niet het absolute nulpunt, dat is −273 °C.
Omrekeningen
De omrekenformule van Celsius naar Kelvin is:
Bijvoorbeeld:
20 graden Celsius is gelijk aan (20 + 273 = 293 K).
De omrekenformule van Kelvin naar Celsius is:
Bijvoorbeeld:
373 K is gelijk aan (373 − 273 = 100 °C).
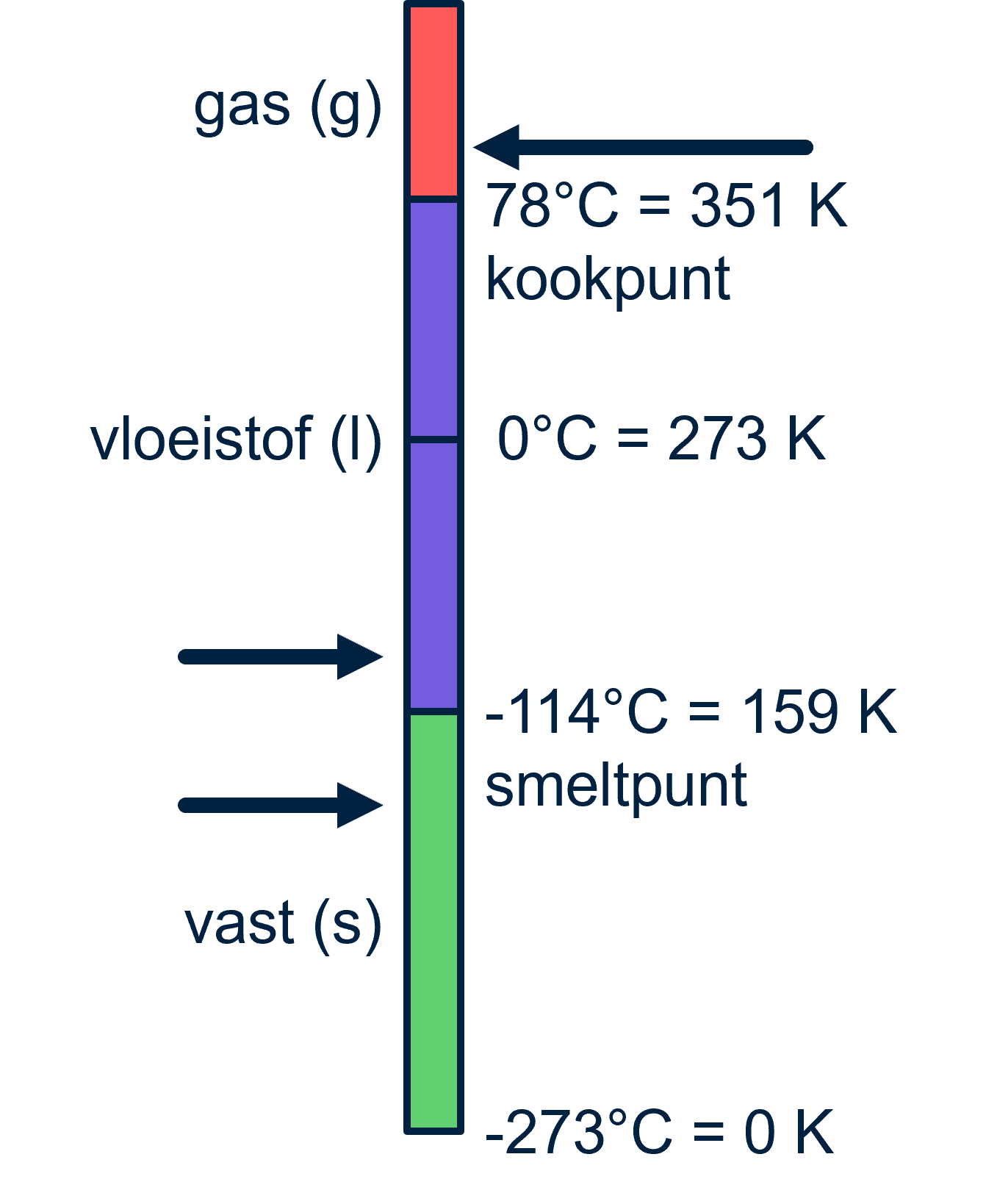
Temperatuurlijn
Een temperatuurlijn laat zien bij welke temperaturen een stof van fase verandert, bijvoorbeeld van vast naar vloeibaar of van vloeibaar naar gas. Op de temperatuurlijn kan je het smeltpunt en het kookpunt van een stof aflezen.
Verschil tussen mengsels en zuivere stoffen
Een zuivere stof bestaat uit één soort molecuul, terwijl een mengsel uit meerdere soorten moleculen bestaat. Bijvoorbeeld:
Water () is een zuivere stof.
Een oplossing van zout in water is een mengsel, omdat het uit verschillende soorten moleculen bestaat.

Zuivere stoffen en mengsels herkennen
Temperatuurverloop bij zuivere stoffen
Bij een zuivere stof blijft de temperatuur constant tijdens het smelt- of kookproces. Wanneer je bijvoorbeeld ijs verwarmt, gebeurt er het volgende:
•Smeltpunt: Bij 0 graden Celsius begint het ijs te smelten. De temperatuur blijft 0 graden totdat het hele ijsblok volledig is gesmolten. Op dat moment wordt het water (vloeistof) verder verwarmd en de temperatuur begint te stijgen.
•Kookpunt: Bij 100 graden Celsius begint het water te koken. De temperatuur blijft 100 graden totdat alle vloeistof in gasvorm (waterdamp) is omgezet. Daarna kan de temperatuur verder stijgen als je de waterdamp verder verwarmt.
Temperatuurverloop bij mengsels
Bij een mengsel verandert de temperatuur geleidelijk tijdens het smelt- en kookproces. Dit komt doordat een mengsel verschillende componenten bevat die bij verschillende temperaturen smelten of koken.
•Smelttraject: In plaats van een constante temperatuur het smeltpunt, zie je een smelttraject. Terwijl een mengsel zoals bijvoorbeeld boter wordt verwarmd, smelten de verschillende vetten niet allemaal tegelijk. Sommige vetten beginnen al te smelten bij een lagere temperatuur, andere pas later. Daardoor verandert de temperatuur geleidelijk tijdens het smelten en blijft deze niet constant gedurende het hele proces.
•Kooktraject: Bij het koken van een mengsel begint niet alles tegelijk te verdampen. De verschillende stoffen in het mengsel hebben elk hun eigen kookpunt. Daardoor stijgt de temperatuur geleidelijk tijdens het koken, in plaats van constant te blijven zoals bij een zuivere stof. Dit geleidelijke temperatuurverloop noemen we het kooktraject.















