Papierchromatografie scheidt stoffen op basis van:
Leerdoelen
•Je kunt beschrijven wat je met papierchromatografie kunt onderzoeken.
•Je kunt het principe van de scheiding bij chromatografie uitleggen aan de hand van het verdelingsevenwicht.
•Je kunt de-waarde van een stof berekenen en op basis daarvan een stof identificeren.
•Je kunt de mobiele en stationaire fase bij papierchromatografie benoemen.
Papierchromatografie
Met papierchromatografie kun je mengsels van kleurstoffen scheiden. De scheiding van de stoffen in het mengsel vindt plaats op basis van het verschil in hun oplosbaarheid in de loopvloeistof en hun aanhechtingsvermogen aan het papier. Hoe beter de oplosbaarheid, hoe hoger de kleurstof op het papier komt. Als het aanhechtingsvermogen hoog is, dan komt de kleurstof juist lager op het papier.
Een toepassing van chromatografie is het controleren of bier een ongewenste stof bevat, zoals diacetyl (geeft een botersmaak). Je brengt een stip bier en een stip zuiver diacetyl aan op dezelfde startlijn. Als in het chromatogram een vlek uit het bier op dezelfde hoogte zit (en dus dezelfde-waarde heeft) als diacetyl, dan bevat het bier diacetyl.
Begrippen
•Mobiele fase: De fase die beweegt. Bij papierchromatografie is dit de loopvloeistof.
•Stationaire fase: De fase die stilstaat. Bij papierchromatografie is dit het papier.
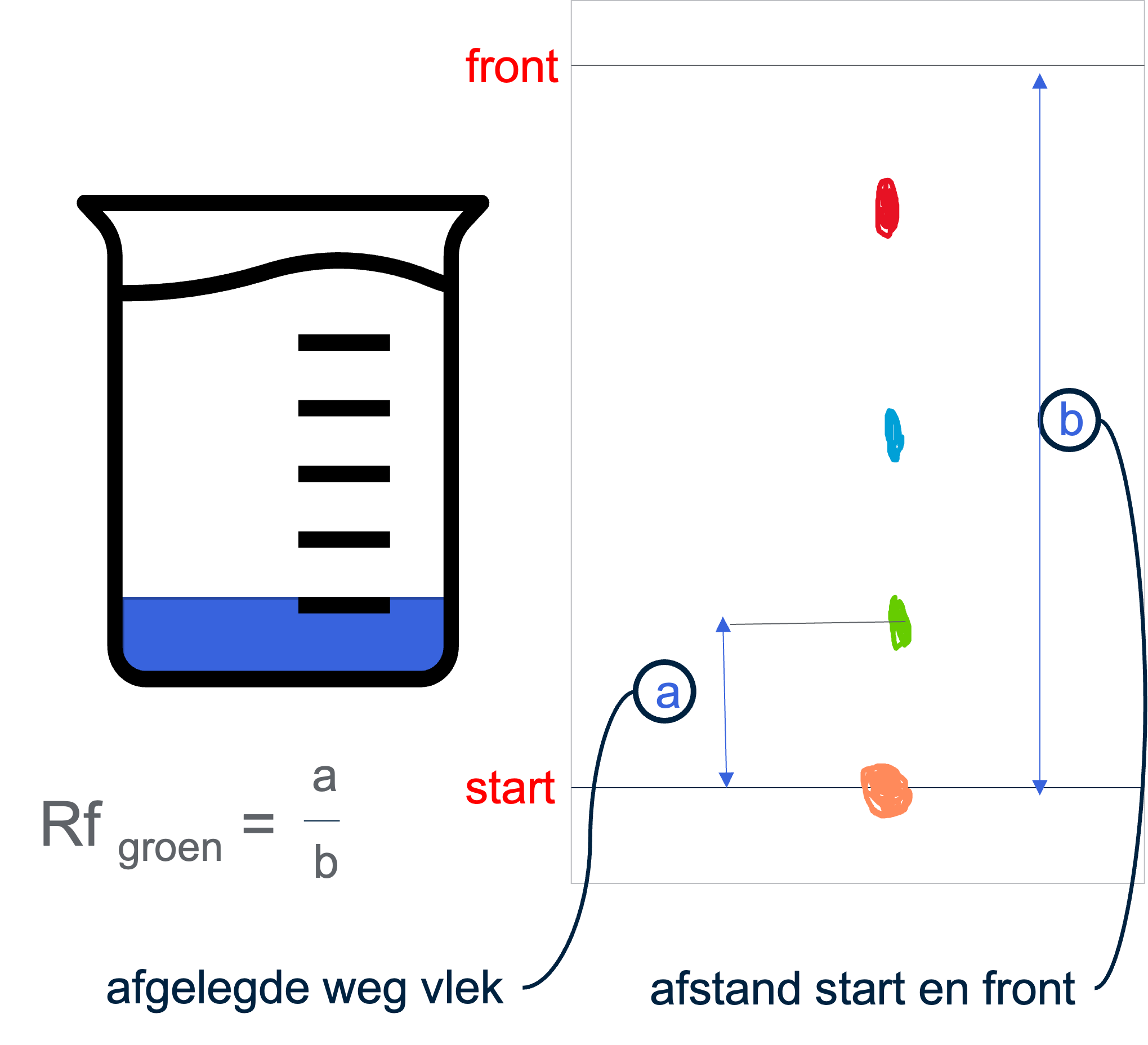
•-waarde: De verhouding tussen de afstand die de stof aflegt en de afstand die de loopvloeistof aflegt.waarbij:
•= afstand van de startlijn tot het midden van de vlek
•= afstand van de startlijn tot het vloeistoffront
Principe van de scheiding
Naast papierchromatografie zijn er andere technieken die op hetzelfde principe berusten, zoals TLC (Thin Layer Chromatography, ook wel dunnelaagchromatografie). Hierbij wordt een laagje silica op plastic gebruikt in plaats van papier. Net als bij papierchromatografie is TLC gebaseerd op het verdelingsevenwicht tussen de mobiele en stationaire fase.
Verdelingsevenwicht
Alle vormen van chromatografie maken gebruik van het verdelingsevenwicht tussen de mobiele en stationaire fase. Dit is een evenwicht waarbij deeltjes van de mobiele fase naar de stationaire fase gaan en andersom. Vandaar de dubbele pijl in de onderstaande vergelijking:
Hierbij isstof A in de mobiele fase enstof A in de stationaire fase. Bij dit evenwicht hoort een verdelingsconstante, die aangeeft hoe de stof verdeeld is over beide fasen:K_{v}=\frac{\left[A_{s}\right]}{\left[A_{m}\right]}
Een hogegeeft aan dat een stof sterk hecht aan de stationaire fase. De stof zal daardoor minder ver meelopen, wat resulteert in een lage-waarde. Omgekeerd betekent een lagedat de stof goed oplost in de mobiele fase, ver meeloopt en dus een hoge-waarde heeft.














