Er zijn zes faseovergangen. Welke van de volgende combinaties beschrijft correct een overgang van een gas naar een vaste stof en van een vaste stof naar een gas?
Leerdoelen
•Je kunt uitleggen wat deeltjesmodellen zijn en relevante deeltjesmodellen benoemen.
•Je kunt de drie fasen en zes faseovergangen uitleggen.
•Je kunt fysische eigenschappen van gassen, vloeistoffen en materialen beschrijven en kunt deze eigenschappen verklaren en analyseren aan de hand van deeltjesmodellen.
•Je kunt uitleggen wat smeltwarmte, verdampingswarmte en het absolute nulpunt zijn.
•Je weet welke BINAS tabellen relevant zijn.
Deeltjesmodellen en fase overgangen
Wat zijn deeltjesmodellen?
Een deeltjesmodel stelt dat stoffen bestaan uit kleine deeltjes. Een Griekse filosoof noemde deze deeltjes atomen (ondeelbaar). Tegenwoordig weten we dat materie uit moleculen bestaat, die weer opgebouwd zijn uit atomen. Atomen bestaan uit een kern met daaromheen elektronen. Een voorbeeld van een deeltjesmodel is het molecuulmodel.
Begrippen van het molecuulmodel
•Toestanden: De fase waarin een stof zich bevindt.
•Chemische verbindingen: Hoe atomen binnen moleculen verbonden zijn.
•Van der Waals krachten: Krachten tussen deeltjes, vooral belangrijk in de vaste en de vloeibare fase.
Fasen van materie
Stoffen kunnen zich in drie toestanden bevinden: vast, vloeibaar of gasvormig.

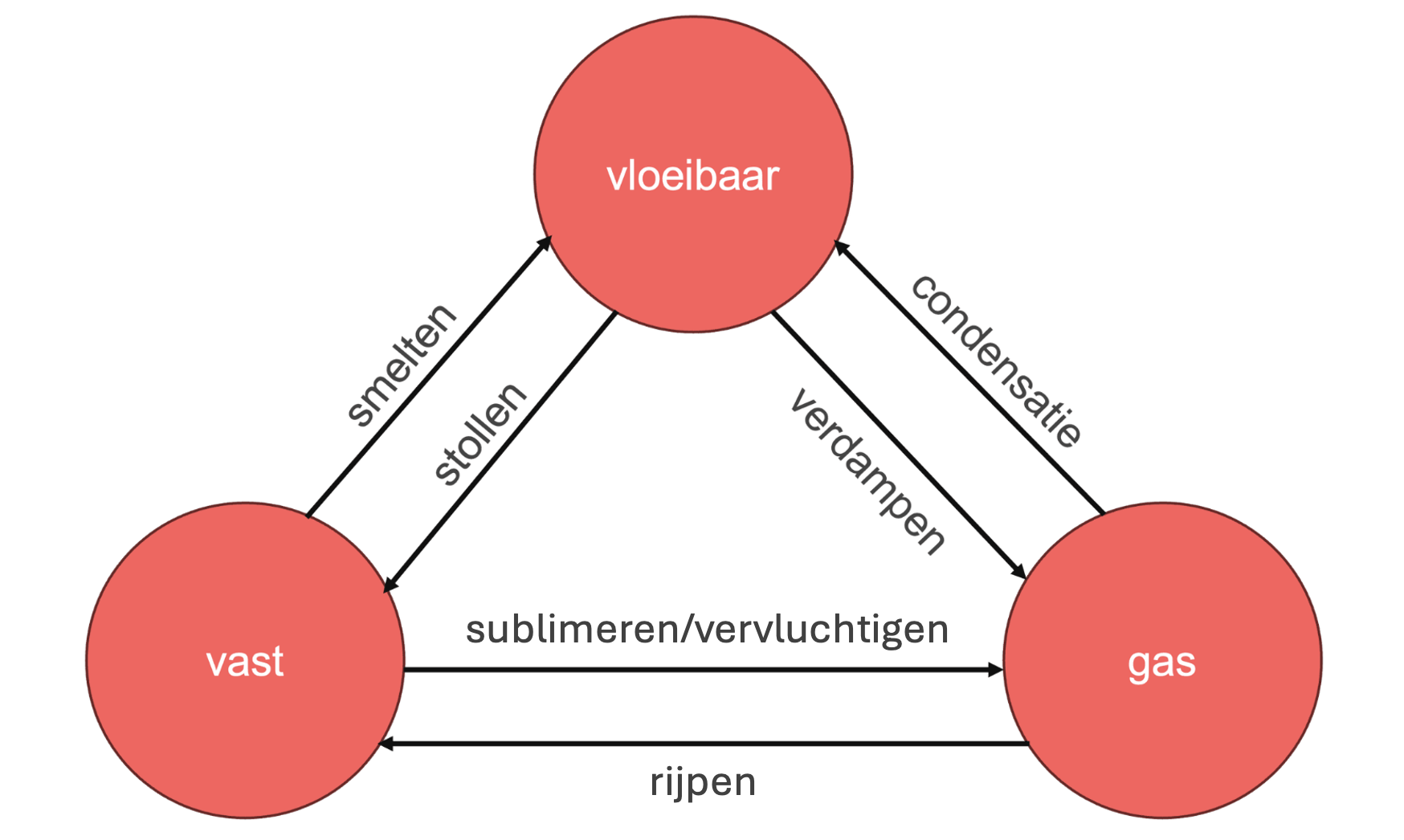
Drie fasen en zes fase overgangen
Er zijn zes mogelijke fase overgangen:
•Smelten (vast naar vloeibaar)
•Stollen (vloeibaar naar vast)
•Verdampen (vloeibaar naar gasvormig)
•Condenseren (gasvormig naar vloeibaar)
•Rijpen (gasvormig naar vast)
•Sublimeren/vervluchtigen (vast naar gasvormig)
Kenmerken van moleculen
•Beweging: Moleculen bewegen altijd en hun snelheid hangt af van de temperatuur.
•Afstand: De afstand tussen deeltjes verschilt per fase en hangt samen met de potentiële energie.
•Aantrekking: Moleculen trekken elkaar aan door bijvoorbeeld Van der Waals krachten.
Smeltwarmte en verdampingswarmte
Smeltwarmte: De energie nodig om een kilogram van een stof op het smeltpunt van vast naar vloeibaar te brengen.
Verdampingswarmte: De energie nodig om een kilogram van een stof op het kookpunt te verdampen.
BINAS Tips: Zie tabel 8 voor smeltwarmte van zilver en tabel 9 voor verdampingswarmte van water.
Temperatuur en het absolute nulpunt
Temperatuur is een maat voor de kinetische energie van de deeltjes. Het absolute nulpunt is -273 graden Celsius, ook wel 0 Kelvin. Hier bewegen de deeltjes niet meer.
Celsius naar Kelvin
Omrekenen naar Kelvin: °C + 273,15 = K
Omrekenen naar Celsius: K - 273,15 = °C
Relevante BINAS-tabellen
De belangrijkste tabellen die je moet kennen:
•Tabel 8: Gegevens van metalen
•Tabel 9: Gegevens van vaste stoffen
•Tabel 10: Gegevens van vloeistoffen
•Tabel 11: Gegevens van gassen
•Tabel 12: Gegevens van dampen













