Noem 3 factoren die de reactiesnelheid kunnen beïnvloeden.
Leerdoelen
•Je kunt uitleggen welke vijf factoren invloed hebben op de reactiesnelheid.
Wat is reactiesnelheid?
Reactiesnelheid betekent letterlijk de snelheid waarmee een reactie plaatsvindt. Dit houdt in hoe snel de beginstoffen worden omgezet tot de eindproducten. Sommige reacties gaan heel snel, zoals een explosie, terwijl andere reacties, zoals het roesten van ijzer, juist heel lang duren.
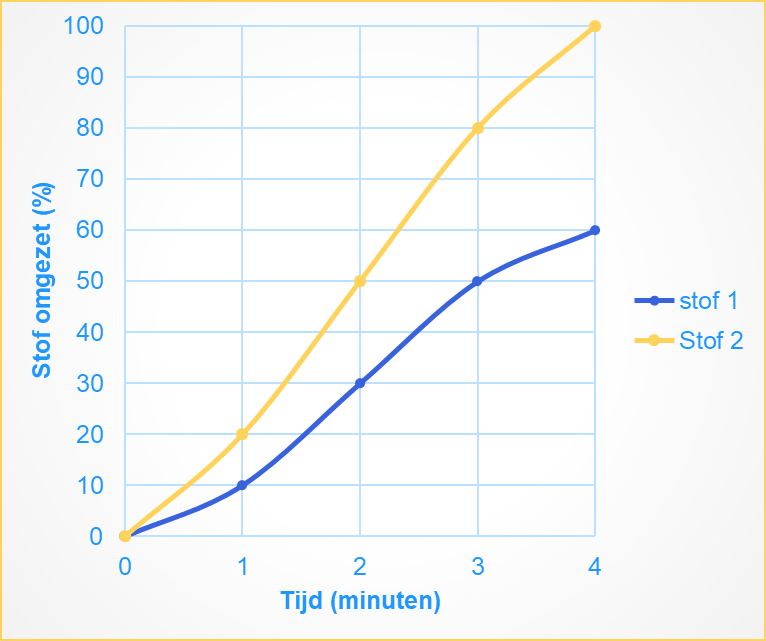
Om de reactiesnelheid te vergelijken, kun je kijken naar hoe snel een bepaalde stof wordt omgezet. Stel, je hebt twee stoffen die een reactie ondergaan: stof één en stof twee. Na vier minuten is stof één pas zestig procent omgezet, terwijl stof twee al voor honderd procent is omgezet. Stof twee heeft dan een hogere reactiesnelheid dan stof één, omdat de omzetting veel sneller is gegaan.
Vijf factoren die de reactiesnelheid beïnvloeden
De snelheid waarmee een stof wordt omgezet, is afhankelijk van verschillende factoren. Deze factoren bepalen hoe snel of langzaam een chemische reactie verloopt. Hieronder staan de vijf belangrijkste factoren beschreven.
1. Soort stof
Niet alle stoffen reageren even snel. Het is net als met mensen: de ene persoon is van nature sneller dan de andere. Sommige stoffen hebben een chemische structuur die ze reactiever maakt, waardoor ze sneller reageren dan andere stoffen. Dit is een eigenschap van de stof zelf.
2. Concentratie
De concentratie van een stof geeft aan hoeveel van die stof er in een bepaalde ruimte aanwezig is. Als er heel veel deeltjes van een stof in een kleine ruimte zitten (hoge concentratie), is de kans groter dat deze deeltjes met elkaar botsen en reageren. Denk maar aan een druk plein: hoe meer mensen er zijn, hoe groter de kans dat je tegen iemand aanbotst. Een hogere concentratie leidt dus vaak tot een snellere reactie.
3. Verdelingsgraad
De verdelingsgraad heeft te maken met hoe goed de beginstoffen met elkaar gemengd zijn, of hoe groot het oppervlak is waar ze met elkaar in contact kunnen komen. Als de beginstoffen goed door elkaar zitten, kunnen de deeltjes elkaar sneller vinden en met elkaar reageren. Bijvoorbeeld, bij een verbranding is het belangrijk dat de brandstof en de zuurstof goed gemengd zijn. Als ze door elkaar heen zitten, kunnen ze sneller met elkaar reageren dan wanneer de brandstof aan de ene kant zit en de zuurstof aan de andere kant. Een goede menging zorgt voor een snelle reactie.
4. Temperatuur
De temperatuur speelt een belangrijke rol bij de reactiesnelheid. Een hogere temperatuur zorgt voor een snellere reactie. Waarom is dat? Bij een hogere temperatuur hebben de deeltjes meer energie. Hierdoor bewegen ze sneller en botsen ze vaker en harder tegen elkaar aan. Net als bij gym: als je hard rent, bots je sneller tegen anderen. Meer botsingen met voldoende energie leiden tot meer succesvolle reacties.
Dit principe zie je vaak in het dagelijks leven. Denk aan groente en fruit. Waarom rot groente en fruit sneller als je het niet in de koelkast legt? In de koelkast is het koud, dus de temperatuur is laag. Buiten de koelkast is de temperatuur hoger. Omdat een hogere temperatuur zorgt voor een sneller proces, verloopt de rotting van groente en fruit sneller bij hogere temperaturen. Als je je appel of peer lang goed wilt houden, kun je hem dus het beste in de koelkast bewaren.
5. Katalysator
Een katalysator is een bijzonder stofje dat je aan een reactie kunt toevoegen. Het zorgt ervoor dat de reactiesnelheid verhoogd wordt, maar het stofje zelf wordt tijdens de reactie niet verbruikt. Het is een soort hulpstof die de reactie sneller laat verlopen zonder zelf te veranderen.
Je kunt een katalysator vergelijken met een coach bij een schaatswedstrijd. De coach staat aan de zijlijn en roept aanmoedigingen of tips: "Je moet harder!" of "Nog zoveel rondjes!". Hierdoor gaat de schaatser sneller schaatsen, maar de coach zelf hoeft niet mee te schaatsen en verbruikt geen energie aan de wedstrijd. Zo werkt een katalysator ook: het zorgt ervoor dat de reactie sneller gaat, zonder zelf deel te nemen aan de reactie.
Voorbeelden katalysatoren
Een bekend voorbeeld van katalysatoren zijn enzymen in je lichaam. Onze enzymen zorgen ervoor dat wij voedsel beter kunnen verteren. Ze helpen de reactie voor vertering te versnellen, maar ze worden niet opgebruikt. Daardoor kunnen we de volgende keer gewoon weer ons eten verteren. Een ander voorbeeld is lactasepillen voor mensen die lactose-intolerant zijn. Deze pillen bevatten het enzym lactase, dat helpt bij het afbreken van lactose, waardoor mensen met lactose-intolerantie melkproducten beter kunnen verdragen.














