In de avond heeft het gesneeuwd. Op de oprit ligt een dikke laag sneeuw. Terwijl het overdag vriest wordt de laag toch steeds minder dik. Welke faseovergang zorgt ervoor dat de laag steeds dunner wordt?
Heb je je ooit afgevraagd hoe het komt dat water kan veranderen van ijs naar vloeistof en vervolgens naar damp? Dit boeiende proces staat bekend als faseovergang.
Wat zijn Faseovergangen?
Om bij het begin te beginnen: stoffen kunnen in drie hoofdfases voorkomen: de vaste fase, de vloeibare fase, en de gasfase. Een faseovergang vindt plaats wanneer een stof van de ene fase naar een andere overgaat. Dit kan gebeuren door veranderingen in de temperatuur. Er zijn in totaal zes verschillende soorten faseovergangen die we gaan bespreken.
Soorten Faseovergangen
Smelten en Stollen
Eerst kijken we naar smelten en stollen (of bevriezen), de overgangen tussen de vaste en de vloeibare fase. Wanneer iets smelt, verandert het van vast naar vloeibaar. Als je aan de winter denkt, smelten de ijspegels aan de dakrand tot water. Stollen, aan de andere kant, is het proces waarbij een vloeistof verandert in een vaste stof. Denk maar aan water dat verandert in ijs in je vriezer.

Vervluchtigen en Rijpen
Dan hebben we vervluchtigen en rijpen, deze gaan over de overgang tussen de vaste stof en een gas. Bij vervluchtigen verandert een vaste stof direct in een gas, zonder eerst vloeibaar te worden. Een voorbeeld hiervan is droogijs (bevroren koolstofdioxide) dat direct verdampt naar gas. Rijpen is het tegenovergestelde waarbij gas direct verandert in een vaste stof, zoals rijp op bladeren tijdens een koude winterochtend.

Verdampen en Condenseren
Tot slot het paar verdampen en condenseren, de veranderingen tussen vloeistof en gas. Wanneer je ademt op een koude ruit en je ziet damp, dat is een voorbeeld van condenseren - gas verandert in vloeistof. Verdampen gebeurt wanneer vloeistof verandert in gas, zoals water dat opwarmt in een pan en verdampt.

Het Belang van Faseovergangen
Faseovergangen zijn niet alleen fascinerend, maar ze spelen ook een cruciale rol in veel weersverschijnselen en in ons dagelijks leven. Van het koken van je eten tot het bevriezen van ijsjes in de zomer, overal om je heen vind je voorbeelden van faseovergangen.
Overzicht
Hieronder staat een overzich van de zes faseovergangen. Probeer deze later ook zelf uit je hoofd te maken om goed te oefenen!
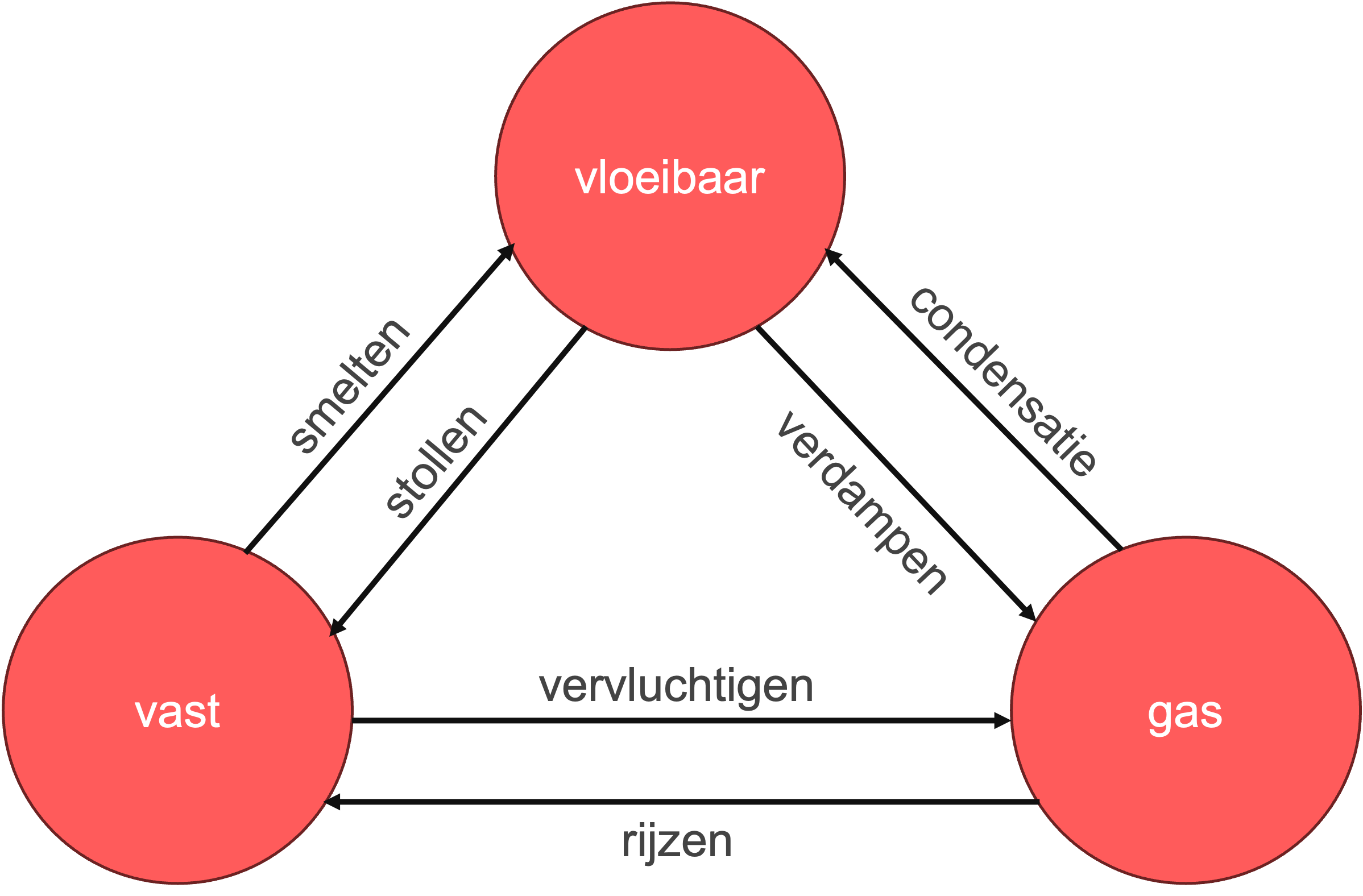
Dus, de volgende keer dat je een glas water ziet condenseren, of je je afvraagt waarom sneeuw verdwijnt zelfs als het vriest, herinner je dan de fascinerende wereld van faseovergangen. En vergeet niet je piramide te maken, het is een geweldige manier om te leren en te onthouden hoe de wondere wereld van natuurkunde en scheikunde werkt!
Bedankt voor het lezen, en veel succes met het experimenteren met faseovergangen in je dagelijks leven en het maken van de vragen!











