Sorteer de volgende bindingen van minst sterk naar sterkst.
Leerdoelen
•Je kunt eigenschappen van zouten noemen.
•Je kunt uitleggen hoe een ion tot stand komt uit een atoom.
•Je kunt uitleggen hoe de oplossing van een zout in water werkt.
Het ionrooster
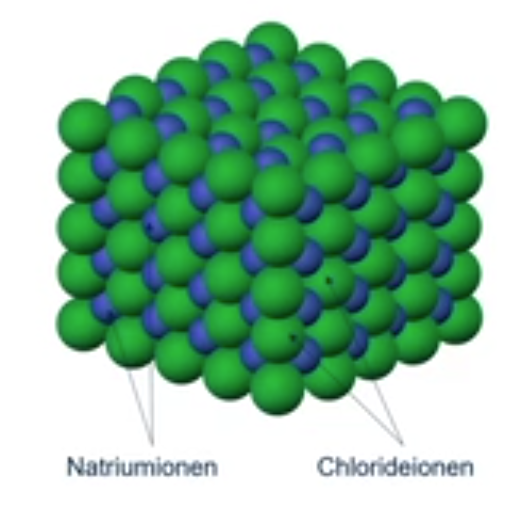
Zouten bestaan uit een ionrooster waarin positief geladen ionen en negatief geladen ionen regelmatig zijn gerangschikt. Dit zorgt voor orde in de structuur. De ionbinding tussen deze deeltjes is vaak sterker dan andere bindingen, zoals de vanderwaalsbinding of de waterstofbrug.
Op macroniveau zijn zouten zoals natriumchloride zichtbaar als kubische kristallen. Dit komt doordat het ionrooster van natriumchloride dezelfde vorm heeft als de kristallen die je met het blote oog kunt zien.
Indeling van stoffen
Om beter te begrijpen wat zouten zijn, is het handig om naar de algemene indeling van stoffen te kijken. Er zijn drie belangrijke categorieën:
•Metalen – Bestaan uit metaalatomen en hebben een metaalrooster.
•Moleculaire stoffen – Bestaan alleen uit niet-metaalatomen en hebben een molecuulrooster.
•Zouten – Bestaan uit een metaal en een niet-metaal en vormen een ionrooster.
Kenmerken van zouten
Zouten hebben een aantal belangrijke kenmerken:
•Ze bevatten een metaal en een niet-metaal.
•Ze bestaan uit geladen deeltjes (ionen).
•Ionen kunnen bewegen als een zout is gesmolten of opgelost in water, waardoor een oplossing stroom kan geleiden.
•Zouten hebben een hoog smeltpunt en hoog kookpunt door de sterke ionbindingen.
Hoe ontstaan ionen?
Atomen streven ernaar om een stabiele elektronenverdeling te krijgen, net als edelgassen. Dit doen ze door elektronen af te staan of op te nemen.
Het natriumion (Na⁺)
Natrium (Na) heeft atoomnummer 11 en dus 11 elektronen.
De elektronenverdeling is 2,8,1 (twee in de eerste schil, acht in de tweede en één in de derde).
Natrium kan stabiliteit bereiken door één elektron af te staan.
Hierdoor ontstaat Na⁺, een positief ion met één elektron minder dan het oorspronkelijke atoom.

Het chloride-ion (Cl⁻)
Chloor (Cl) heeft atoomnummer 17 en dus 17 elektronen.
De elektronenverdeling is 2, 8, 7.
Chloor kan stabiliteit bereiken door één elektron op te nemen.
Hierdoor ontstaat Cl⁻, een negatief ion met één elektron meer dan het oorspronkelijke atoom.
Wanneer Na⁺ en Cl⁻ elkaar aantrekken, ontstaat een sterke ionbinding en vormen ze natriumchloride (NaCl), beter bekend als keukenzout.

Oplossen van zouten in water
Wanneer keukenzout in water wordt opgelost, gebeurt het volgende:
De ionen in het ionrooster worden omringd door watermoleculen. Hierdoor worden de ionen uit elkaar getrokken en zweven ze los door de oplossing. De oplossing kan nu elektrische stroom geleiden. Als het water weer verdampt, blijven de zoutkristallen achter.
Waarom zie je in Twente speciale huisjes?
In Twente zijn huisjes te zien die te maken hebben met zoutwinning. Dit komt doordat in deze regio vroeger een zee lag. Het natriumchloride uit die zee is in de grond achtergebleven.
Zoutwinning gebeurt door stoom de grond in te pompen. Dit lost het zout op, waarna het via buizen naar boven wordt gehaald. In fabrieken wordt het water verdampt, zodat het zout wordt teruggewonnen. Dit proces levert onder andere het keukenzout op dat je gebruikt bij het koken!













