Geef de oplosvergelijking inclusief toestandsaanduidingen voor het oplossen van aluminiumnitraat in water (controleer in BINAS tabel 45A of aluminiumnitraat oplost in water).
Leerdoelen
•Je kunt hydratatie van zouten beschrijven.
•Je kunt uitleggen waarom de toestand van ionen in water (aq) wordt genoemd.
•Je kunt de oplosbaarheidstabel 45A uit Binas gebruiken om de oplosbaarheid van zouten te bepalen.
•Je kunt oplos- en indampvergelijkingen opstellen.
•Je kunt het verschil tussen een onverzadigde en een verzadigde zoutoplossing uitleggen.
•Je kunt de reactie van metaaloxiden met water beschrijven en de producten benoemen.
Water
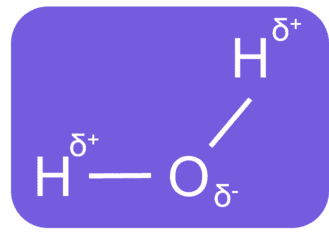
Water is een polaire stof. Dit komt doordat de zuurstof- en waterstofatomen een verschillende elektronegativiteit hebben, wat resulteert in polaire O-H-bindingen. Het zuurstofatoom trekt harder aan het gemeenschappelijke elektronenpaar en krijgt eenlading, terwijl het waterstofatoom zwakker trekt, waardoor het eenlading krijgt.
Hydratatie
Wanneer je een zout, zoals keukenzout, in water doet en roert, zul je opmerken dat de vaste stof verdwijnt. Dat wil zeggen dat de vaste structuur van het zout (het ionrooster) op dat moment wordt afgebroken. Tegelijkertijd worden de vrijgekomen ionen omringd door watermoleculen. Dit komt doordat water een polaire stof is: de negatieve kant van het watermolecuul richt zich naar positieve ionen en de positieve kant naar negatieve ionen. Dit proces heet hydratatie en zorgt ervoor dat de ionen in oplossing blijven.
De betekenis van (aq)
De toestand (aq) wordt gebruikt om aan te geven dat een stof is opgelost in water. De afkorting (aq) komt van het Latijnse woord aqua, wat water betekent.
Dit betekent dat de ionen in oplossing omringd zijn door watermoleculen. Deze watermoleculen vormen een hydratatieschil rondom de ionen.
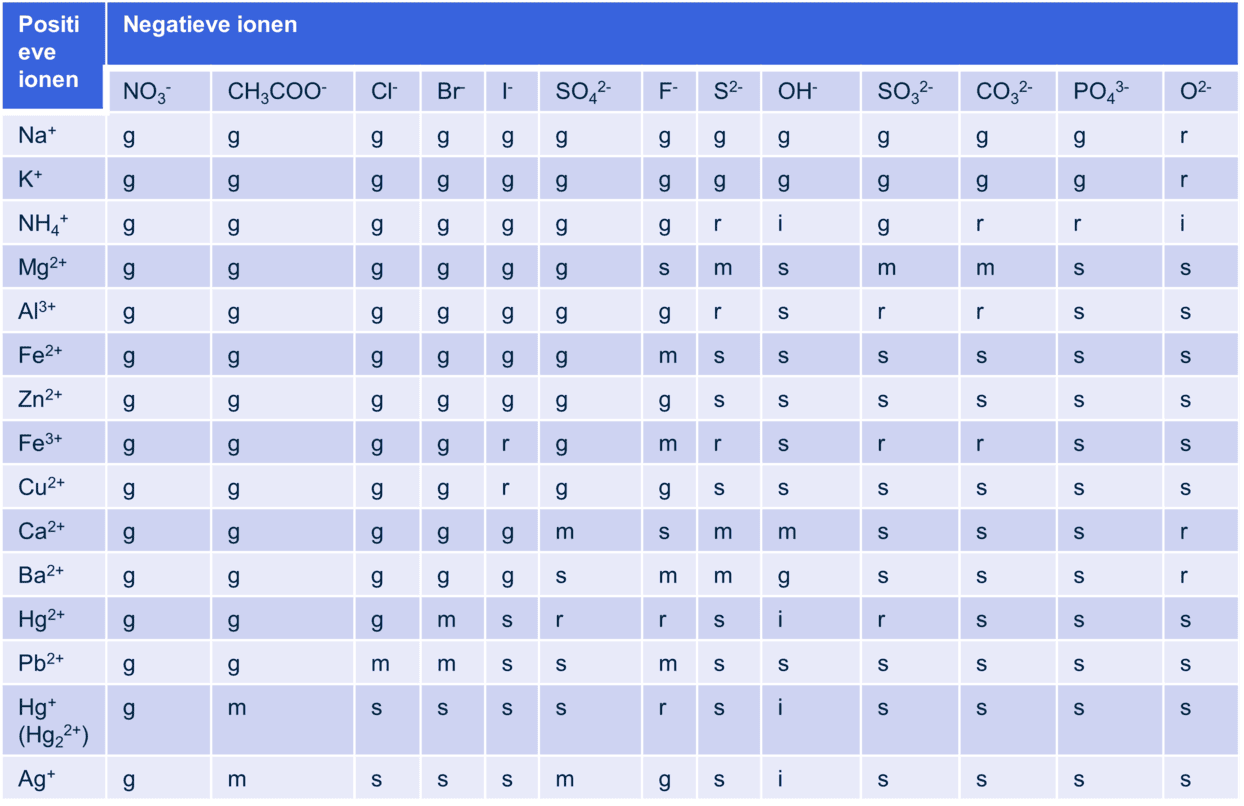
Het gebruik van oplosbaarheidstabel 45A
De oplosbaarheid van verschillende soorten zouten kan worden vastgesteld met behulp van de oplosbaarheidstabel 45A uit Binas. Door een positief ion met een negatief ion te kruisen, vind je de oplosbaarheid. De combinatie van en is bijvoorbeeld goed oplosbaar (g), maar de combinatie van en is slecht oplosbaar (s). De oplosbaarheid kan ook kwantitatief worden bepaald. Vaak is de oplosbaarheid gegeven in gram per liter. Door deze waarde te delen door de molaire massa van het zout, kun je de oplosbaarheid omrekenen naar mol per liter. Met deze waarde kun je vervolgens in tabel 45A bepalen of een stof goed, matig of slecht oplosbaar is. Een stof is goed oplosbaar bij meer dan 0,1 mol/L, matig oplosbaar tussen 0,01 en 0,1 mol/L en slecht oplosbaar bij minder dan 0,01 mol/L.
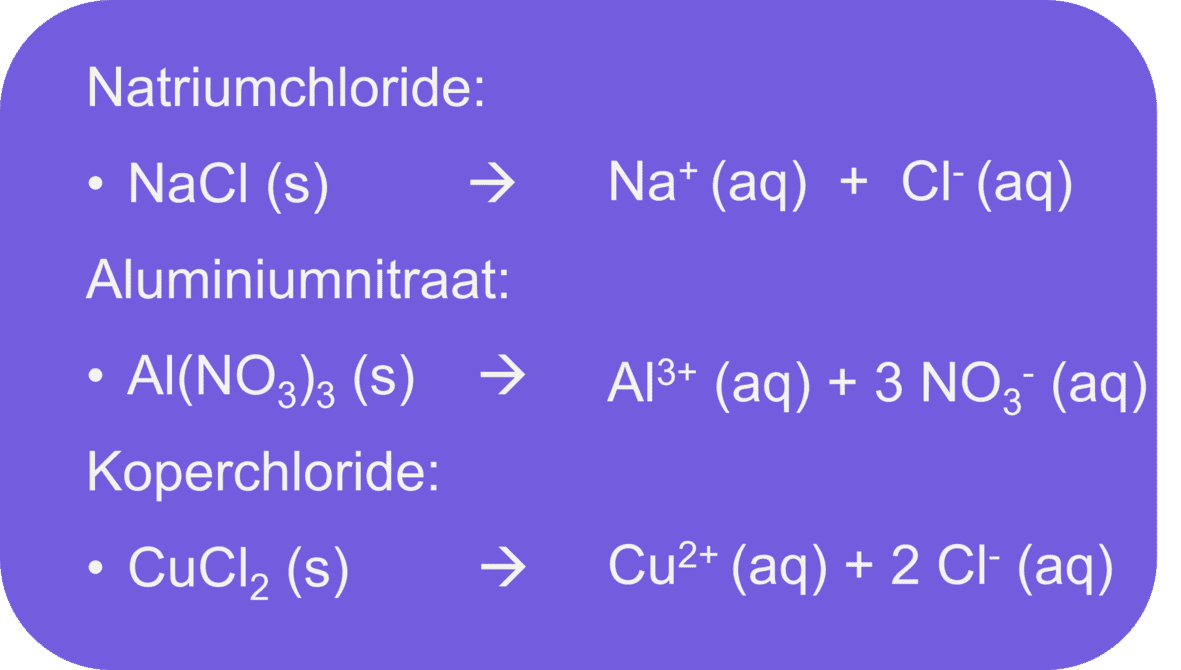
Het opstellen van oplos- en indampvergelijkingen
Voor het oplossen van zouten in water kunnen oplosvergelijkingen opgesteld worden. Daarbij is het belangrijk om eerst de verhoudingsformule van het zout correct op te stellen. Dit doe je door de ladingen van de positieve en negatieve ionen zo te combineren dat het geheel neutraal is. Bijvoorbeeld: aluminiumnitraat bestaat uit en . Om de totale lading nul te maken, zijn drie nitraationen nodig voor één aluminiumion. De formule wordt dus.
Tegelijkertijd kunnen we ook indampvergelijkingen opstellen die het proces van verdampen van water uit een zoutoplossing tot het overblijven van vast zout beschrijven.

Onverzadigde en verzadigde zoutoplossingen
Het verschil tussen een onverzadigde en een verzadigde zoutoplossing zit in de hoeveelheid opgelost zout. Is de maximale hoeveelheid zout opgelost, dan spreken we van een verzadigde oplossing. Kan er nog meer zout oplossen, dan hebben we te maken met een onverzadigde oplossing.
De reactie van metaaloxiden met water
Sommige metaaloxiden reageren met water in plaats van enkel op te lossen, een fenomeen dat je kunt observeren bij bepaalde verbindingen zoals natriumoxide () en kaliumoxide (). Deze metaaloxiden lossen niet simpelweg op, maar er vindt een chemische reactie met water plaats. In Binas tabel 45A wordt dit aangegeven met de letter r (reageert).

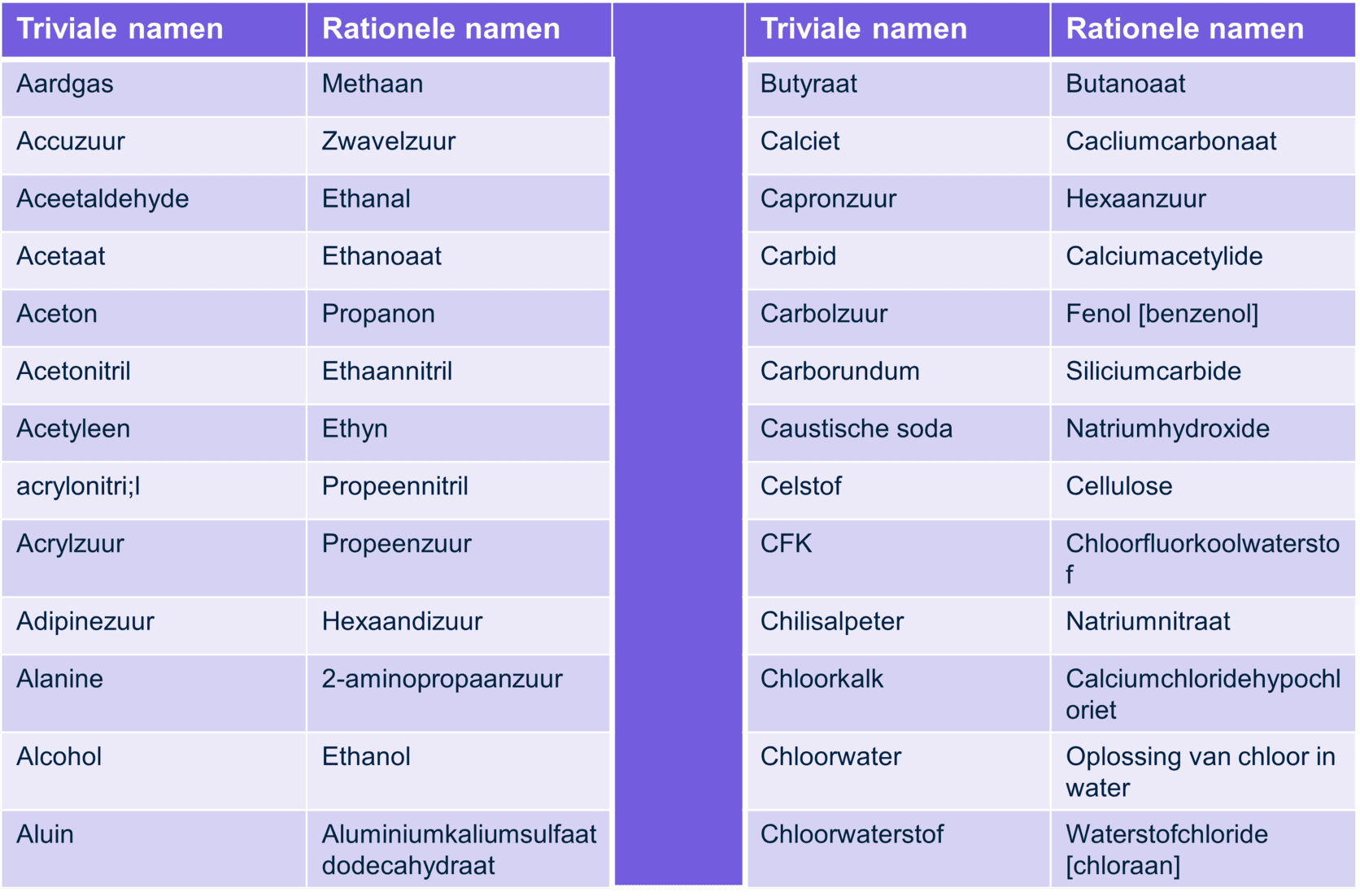
Triviale namen
Triviale namen zijn alledaagse of gangbare namen die we gebruiken voor chemische stoffen. Deze namen zijn meestal geen weergave van de chemische structuur van de stof, maar zijn vaak gebaseerd op historische, culturele of praktische redenen.
Bijvoorbeeld wordt er vaak "keukenzout" gezegd in plaats van natriumchloride of "aardgas" in plaats van methaan. Deze triviale namen maken het makkelijker om over deze stoffen te praten in dagelijkse gesprekken.
In Binas-tabel 66A vind je een overzicht van veelgebruikte triviale namen. Dit is handig als je een naam tegenkomt waarvan je de chemische aanduiding niet direct weet.