Waarom kan ethanol wel goed oplossen in water en ethaan niet?
Leerdoelen
•Je kunt uitleggen wat elektronegativiteit is.
•Je kunt uitleggen wanneer iets een polaire of een apolaire binding is.
•Je kunt uitleggen wat een waterstofbrug is.
Elektronegativiteit
Elektronegativiteit is een getal dat de aantrekkingskracht weergeeft die een atoom uitoefent op de elektronen die het deelt in een atoombinding. Elk element heeft een specifieke elektronegativiteitswaarde. Je kunt deze waarden vinden in Binas-tabel 40A. Pak je Binas er maar eens bij en zoek de kolom 'elektronegativiteit' op. Hierin zie je bijvoorbeeld dat waterstof (H) een elektronegativiteit heeft van 2,1 en zuurstof (O) een waarde van 3,5.

Wanneer twee atomen een atoombinding vormen, delen ze elektronen. Maar als het ene atoom een hogere elektronegativiteit heeft dan het andere, trekt het harder aan deze gedeelde elektronen. Dit heeft belangrijke gevolgen voor de ladingsverdeling binnen een molecuul.
Polaire en apolaire atoombindingen
Het verschil in elektronegativiteit (ΔEN) tussen twee gebonden atomen bepaalt het type atoombinding:
•Apolaire atoombinding: Als het verschil in elektronegativiteit (ΔEN) kleiner of gelijk is aan 0,4, dan is de binding apolair. De elektronen worden vrijwel gelijkmatig verdeeld tussen de atomen.
•Polaire atoombinding: Als het verschil in elektronegativiteit (ΔEN) groter is dan 0,4, maar kleiner of gelijk aan 1,7, dan is de binding polair. De elektronen worden ongelijkmatig verdeeld, waardoor het atoom met de hogere elektronegativiteit een beetje negatief wordt en het andere atoom een beetje positief.
•Ionbinding: Als het verschil in elektronegativiteit (ΔEN) groter is dan 1,7, dan is de aantrekkingskracht zo groot dat het elektron volledig overspringt naar het atoom met de hogere elektronegativiteit. Er ontstaan dan ionen, en de binding is een ionbinding. Dit gebeurt bijvoorbeeld bij natriumchloride (NaCl), waar het verschil in elektronegativiteit tussen Na en Cl groter is dan 1,7, waardoor Na een Na⁺-ion wordt en Cl een Cl⁻-ion.
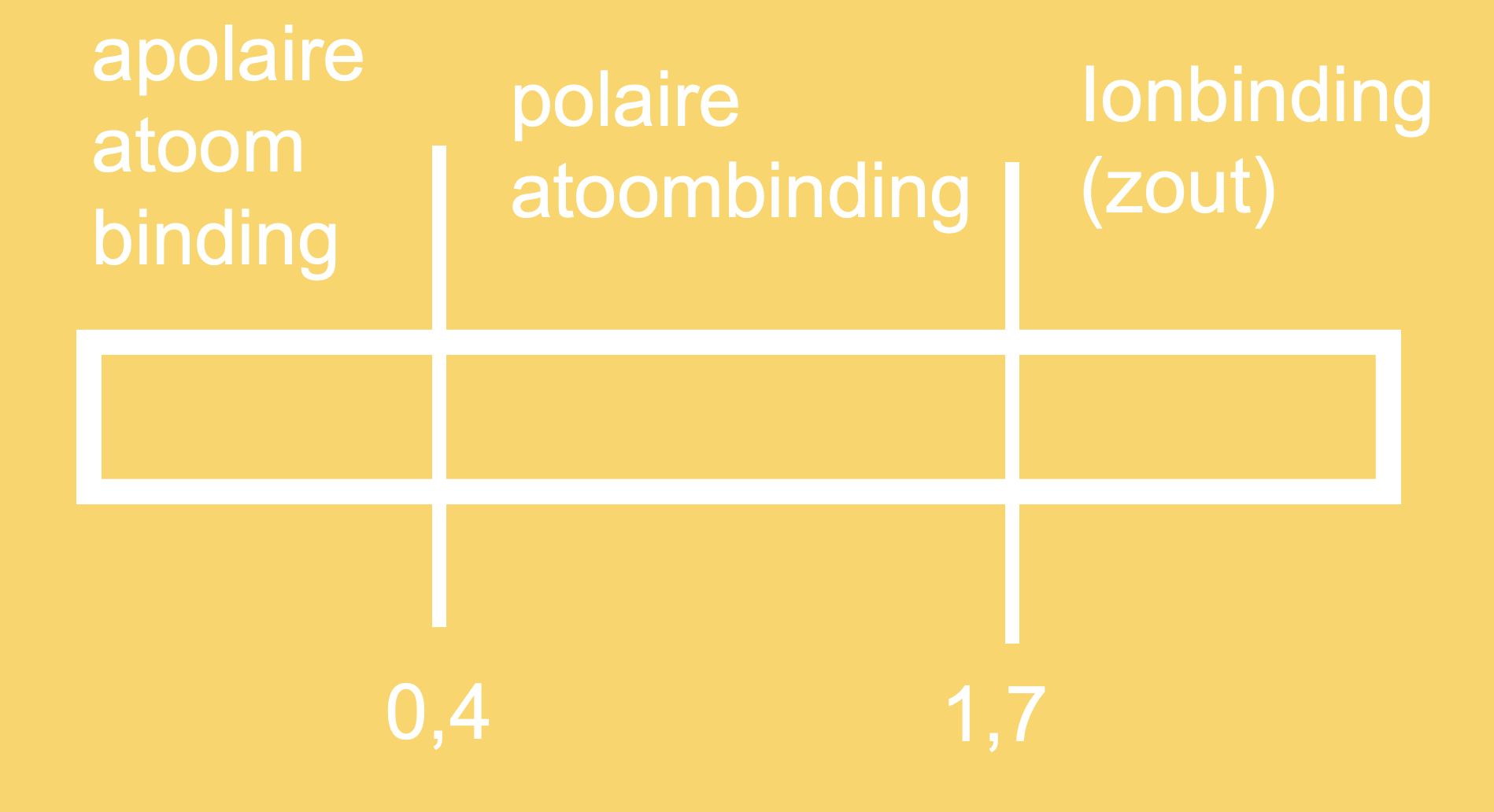
Toepassing: watermolecuul
We kijken naar de O-H binding:
•Elektronegativiteit O = 3,5
•Elektronegativiteit H = 2,1
•ΔEN = 3,5 - 2,1 = 1,4
Omdat 1,4 tussen 0,4 en 1,7 ligt, is de O-H binding een polaire atoombinding. Dit betekent dat de zuurstof harder aan de elektronen trekt dan de waterstof. Hierdoor krijgt zuurstof een beetje negatieve lading, aangeduid als partiële lading delta min (δ⁻), en waterstof krijgt een beetje positieve lading, delta plus (δ⁺).
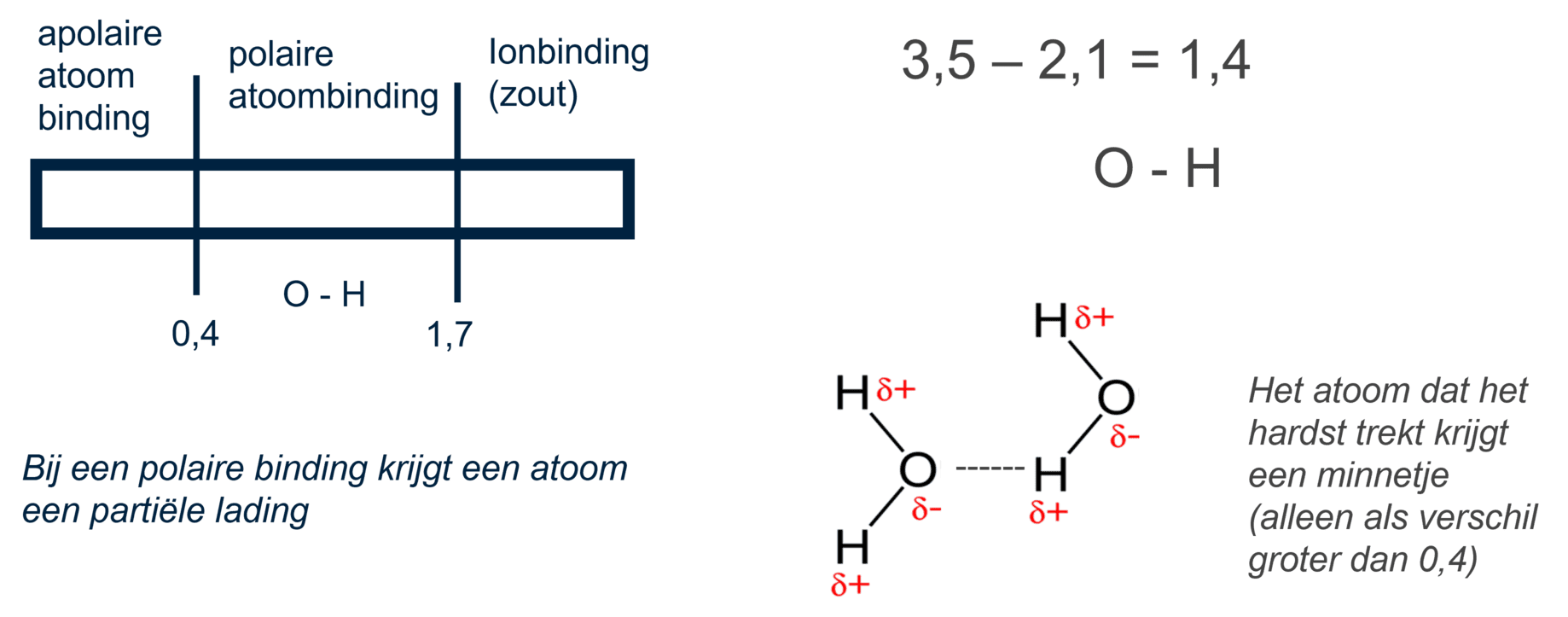
Toepassing: C-H-binding
Een ander voorbeeld is de C-H-binding:
•Elektronegativiteit C = 2,5
•Elektronegativiteit H = 2,1
•ΔEN = 2,5 - 2,1 = 0,4
Omdat 0,4 precies op de grens ligt van een apolaire binding, wordt de C-H-binding als apolair beschouwd. Er is geen significant verschil in aantrekkingskracht, dus er ontstaan geen partiële ladingen. Moleculen die voornamelijk uit C-H-bindingen bestaan, zoals veel koolwaterstoffen, zijn daarom apolair. Ze lossen slecht op in water, maar goed in andere apolaire stoffen zoals olie.
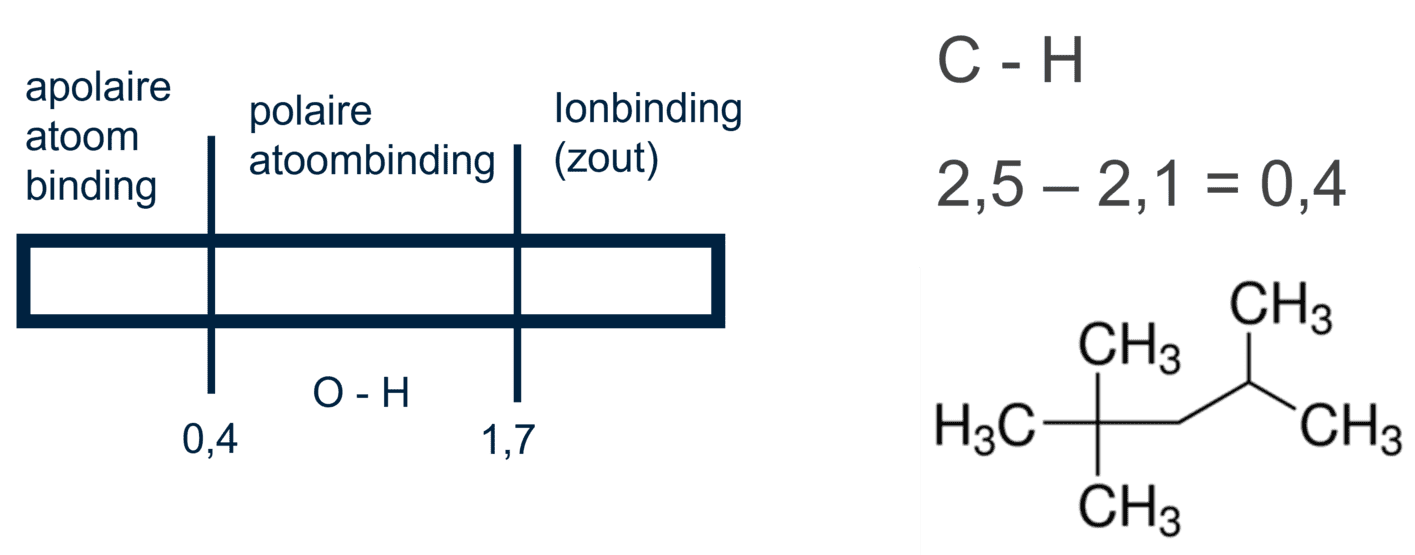
Waterstofbruggen
De partiële ladingen in polaire moleculen leiden tot een speciale soort intermoleculaire kracht: de waterstofbrug. Een waterstofbrug ontstaat wanneer de partiële negatieve lading (δ⁻) op een zuurstof- of stikstofatoom van het ene molecuul wordt aangetrokken door de partiële positieve lading (δ⁺) op een waterstofatoom van een ander molecuul. Dit waterstofatoom moet dan wel gebonden zijn aan een zuurstof- of stikstofatoom (OH- of NH-groep).
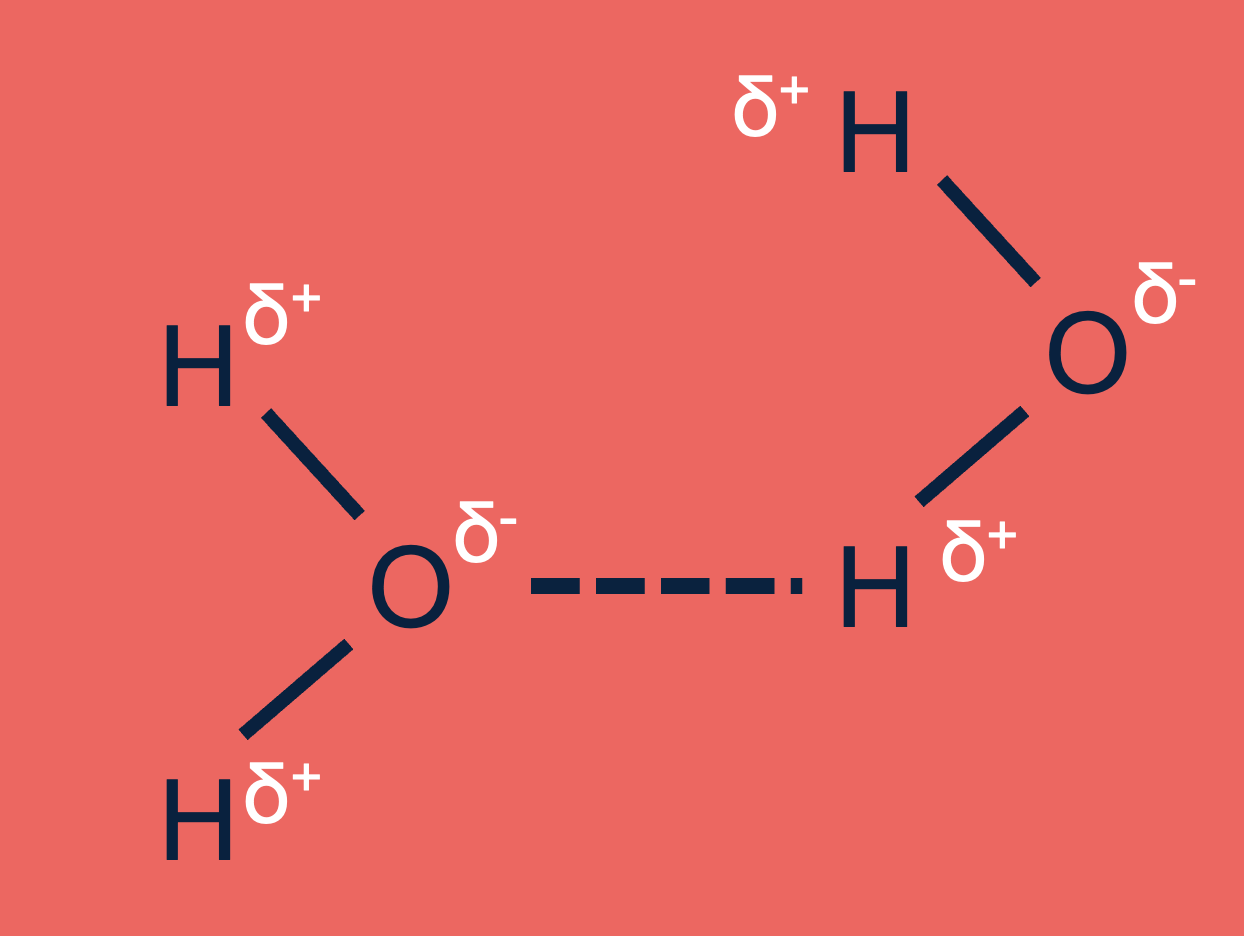
Waterstofbruggen zijn sterker dan andere intermoleculaire krachten zoals vanderwaalskrachten, maar zwakker dan atoombindingen. Ze zijn cruciaal voor veel eigenschappen van stoffen, vooral water.
De algemene regel is: als een stof OH- en/of NH-groepen heeft, kan deze waterstofbruggen vormen tussen de moleculen. Dit geldt niet alleen voor watermoleculen onderling, maar ook tussen water en andere moleculen met deze groepen.
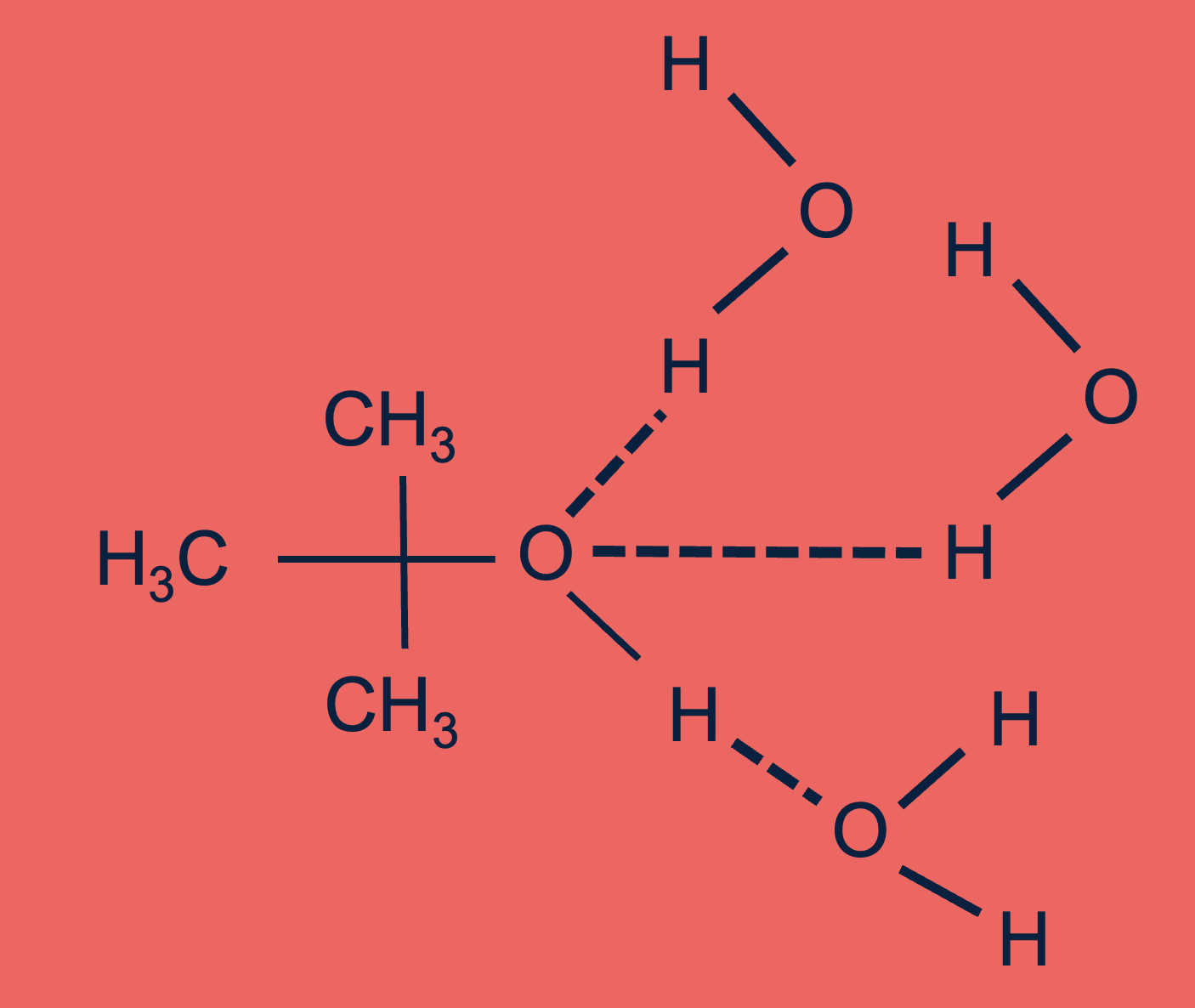
Denk bijvoorbeeld aan een alcoholmolecuul (zoals ethanol, CH₃CH₂OH). Dit molecuul heeft een OH-groep. De zuurstof in deze OH-groep krijgt een δ⁻ en de waterstof een δ⁺. Hierdoor kan het alcoholmolecuul waterstofbruggen vormen met watermoleculen. De δ⁻ van de zuurstof in het alcoholmolecuul kan een waterstofbrug vormen met de δ⁺ van een waterstofatoom van een watermolecuul. Tegelijkertijd kan de δ⁺ van de waterstof in de OH-groep van het alcoholmolecuul een waterstofbrug vormen met de δ⁻ van een zuurstofatoom van een watermolecuul. Dit verklaart waarom alcohol goed oplost in water.
Oppervlaktespanning
Hoe kunnen insecten op water blijven staan? Watermoleculen vormen onderling talloze waterstofbruggen. Deze bruggen zorgen voor een sterke aantrekkingskracht tussen de moleculen, vooral aan het oppervlak van het water. De watermoleculen aan het oppervlak worden naar binnen getrokken door de waterstofbruggen met de moleculen eronder en ernaast. Dit creëert een soort 'huid' of vlies op het wateroppervlak, wat we oppervlaktespanning noemen. De oppervlaktespanning is sterk genoeg om kleine, lichte objecten, zoals insecten, te dragen zonder dat ze zinken.














