Welke van bovenstaande stoffen lost het beste op in water (ethanol of propan-1-ol)? Licht je antwoord toe.
Leerdoelen
•Je kunt uitleggen dat moleculen een apolair en een polair deel kunnen hebben.
•Je kunt beschrijven hoe hydrofobe stoffen oplossen in hydrofobe stoffen en hydrofiele stoffen in hydrofiele stoffen.
•Je kunt het ontstaan van een verdelingsevenwicht tussen twee oplosmiddelen uitleggen wanneer een stof hierin wordt geplaatst.
Polaire en apolaire moleculen
Bij moleculaire stoffen houden atoombindingen de atomen bij elkaar. Tussen moleculen werken zwakkere krachten, zoals vanderwaalsbinding en, indien OH- of NH-groepen aanwezig zijn, waterstofbruggen.
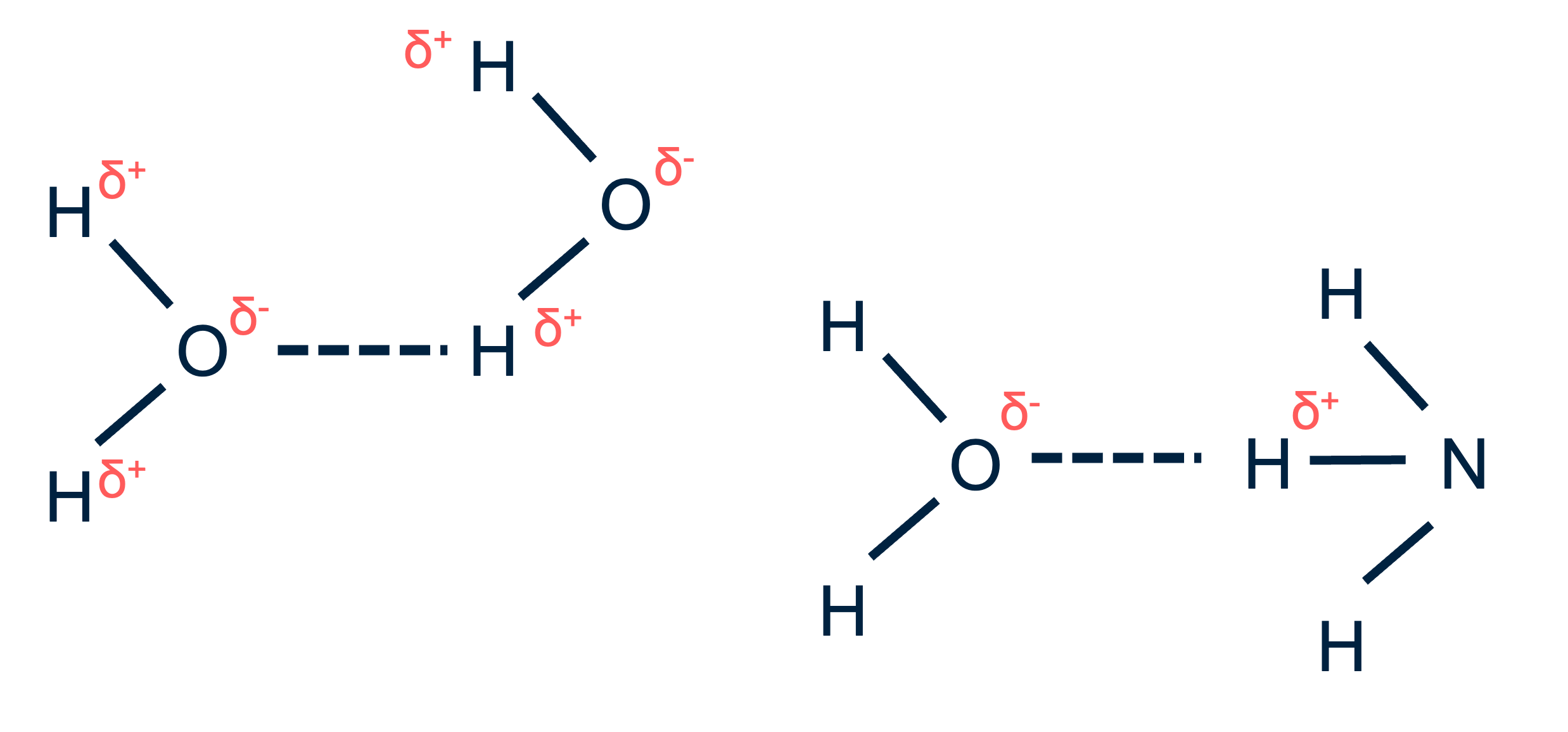
Een molecuul kan zowel een polair als een apolair deel bevatten. Bij polaire bindingen ontstaat een ladingsverschil, waarbij het ene atoom een gedeeltelijk negatieve lading (δ⁻) krijgt en het andere een gedeeltelijk positieve lading (δ⁺). Dit ladingsverschil ontstaat doordat het ene atoom harder aan de gemeenschappelijke elektronen trekt dan het andere, een eigenschap die elektronegativiteit wordt genoemd. Groepen zoals OH en NH zorgen daardoor voor polaire eigenschappen, terwijl koolwaterstofdelen met vooral C- en H-atomen apolair zijn.
De intermoleculaire krachten zijn een gevolg van deze ladingsverschillen en bepalen hoe moleculen met elkaar mengen en oplossen.
Voorbeelden
•Methanol: bevat een polaire OH-groep en een apolair -deel.
•Methanamine: bevat een polaire -groep en een apolair -deel.
Hydrofiele en hydrofobe stoffen
Hydrofiele stoffen (waterliefhebbers) lossen goed op in water en in andere hydrofiele stoffen, terwijl hydrofobe stoffen (watervrezers) dat niet doen. Polaire moleculen, zoals water, kunnen waterstofbruggen vormen, waardoor ze goed mengen met andere polaire stoffen.
Hydrofobe stoffen, die dus apolair zijn, kunnen niet goed oplossen in water. Daarom lost olie bijvoorbeeld niet goed op in water.

Apolaire stoffen, zoals oliën, lossen daarentegen goed op in andere apolaire stoffen.
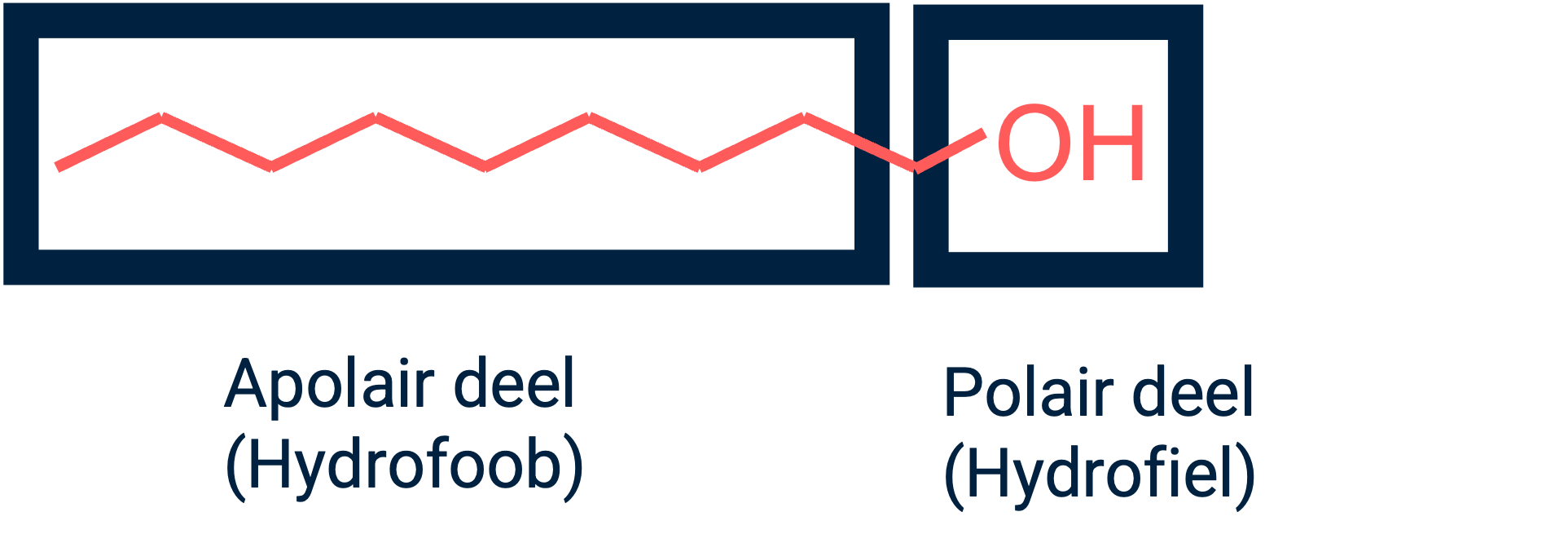
Een molecuul zoals pentan-1-ol heeft een lange apolaire koolstofketen en een polaire OH-groep. De OH-groep is hydrofiel en kan in principe goed met water mengen, maar het apolaire deel van het molecuul is te groot. Daardoor lost pentan-1-ol niet goed op in water.
Dynamisch evenwicht en verdelingsevenwicht
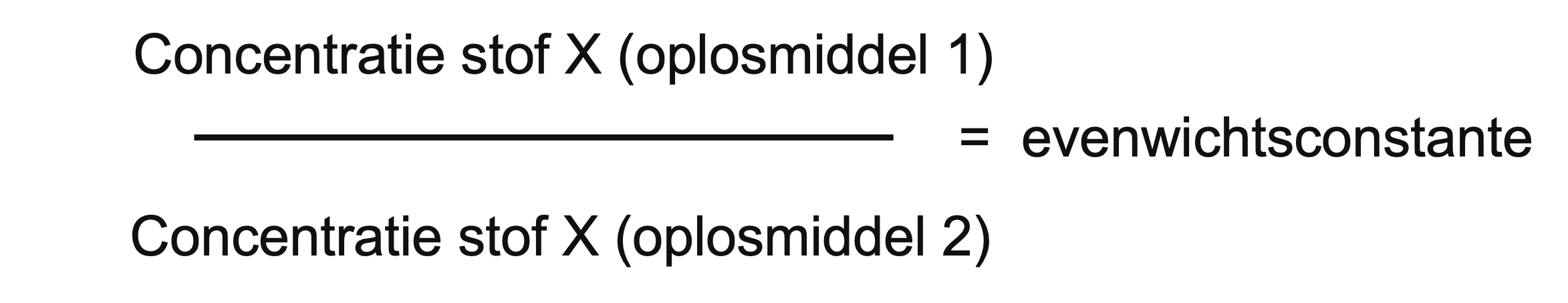
Wanneer een stof in twee verschillende oplosmiddelen wordt geplaatst, kan er een verdelingsevenwicht ontstaan. Dit evenwicht betekent dat de stof zich verdeelt over de twee oplosmiddelen totdat de concentraties niet meer veranderen, hoewel er nog steeds moleculen tussen de fasen bewegen. De evenwichtsconstante (K) beschrijft de verhouding van de concentraties van een stof in de twee fasen bij evenwicht. De concentratie van een stof wordt weergegeven met rechte haken, bijvoorbeeld []. De verhouding van de concentraties bij evenwicht wordt gegeven door de evenwichtsconstante K: K = [ (aq)] / [ (wasbenzine)].
Voorbeeld
Jood verdeelt zich over zowel wasbenzine als water, wat resulteert in een dynamisch evenwicht.













