Vul de ontbrekende woorden in de volgende zinnen in:
Een dipoolmolecuul wordt bepaald door zijn bouw. Een klassiek voorbeeld is het watermolecuul (H₂O). In dit molecuul vertoont zuurstof (O) een partiële negatieve lading (δ-) en waterstof (H) een partiële positieve lading (δ+). Deze ladingen ontstaan door verschillen in elektronegativiteit.
Bijvoorbeeld, zuurstof heeft een elektronegativiteit van 3,5 en waterstof 2,1, waardoor zuurstof sterker aan het gemeenschappelijke elektronenpaar trekt.

Elektronegativiteit en polaire bindingen
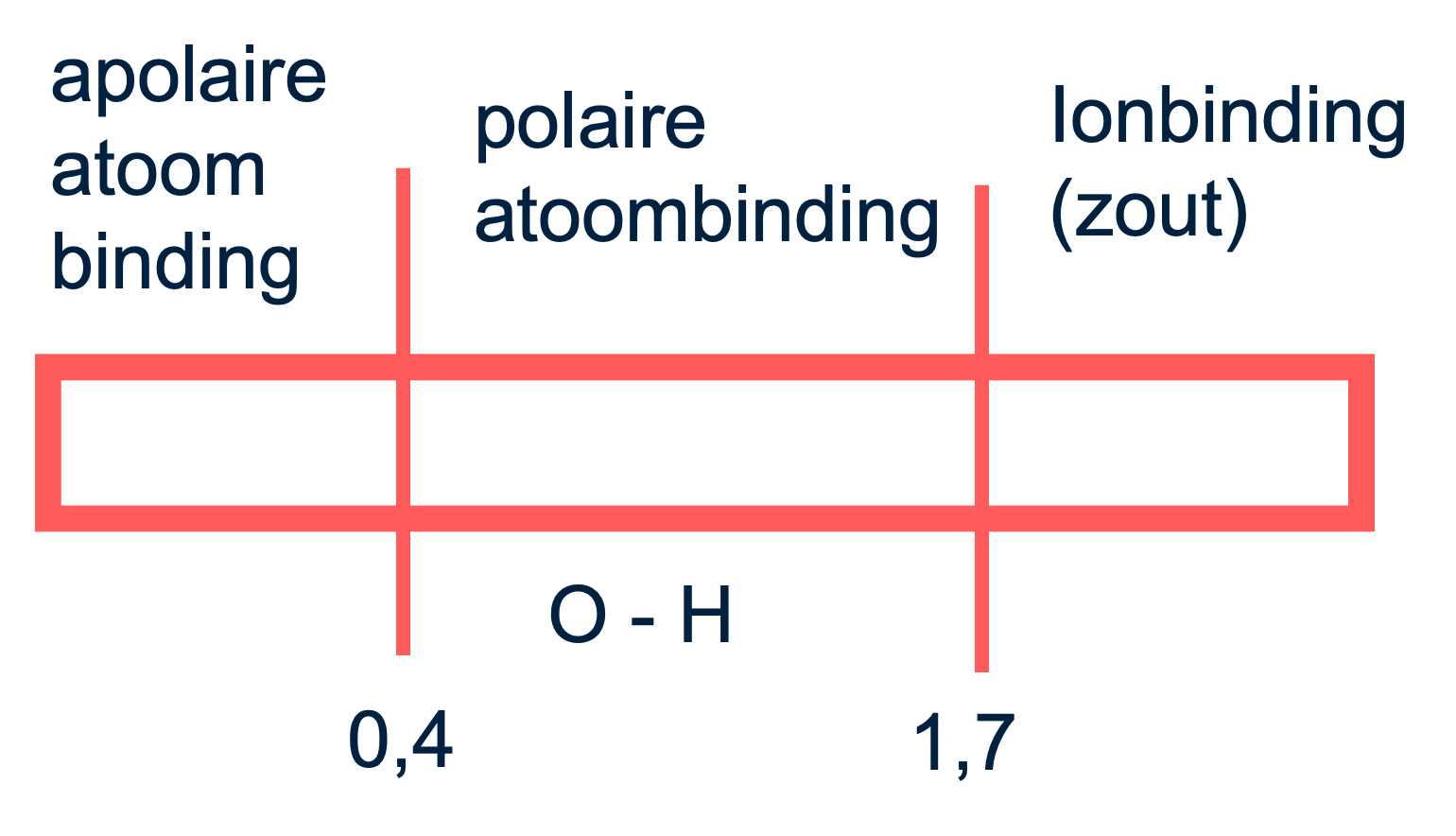
Bindingen zijn polair bij een elektronegativiteitsverschil tussen 0,4 en 1,7. Bij een verschil groter dan 1,7 ontstaan ionische bindingen. In water (verschil van 1,4 = 3,5 - 2,1) is de binding dus polair. Moleculen met een ongelijke ladingverdeling die elkaar niet opheffen, vormen dipoolmoleculen.
VSEPR-model: Ruimtelijke structuur van moleculen
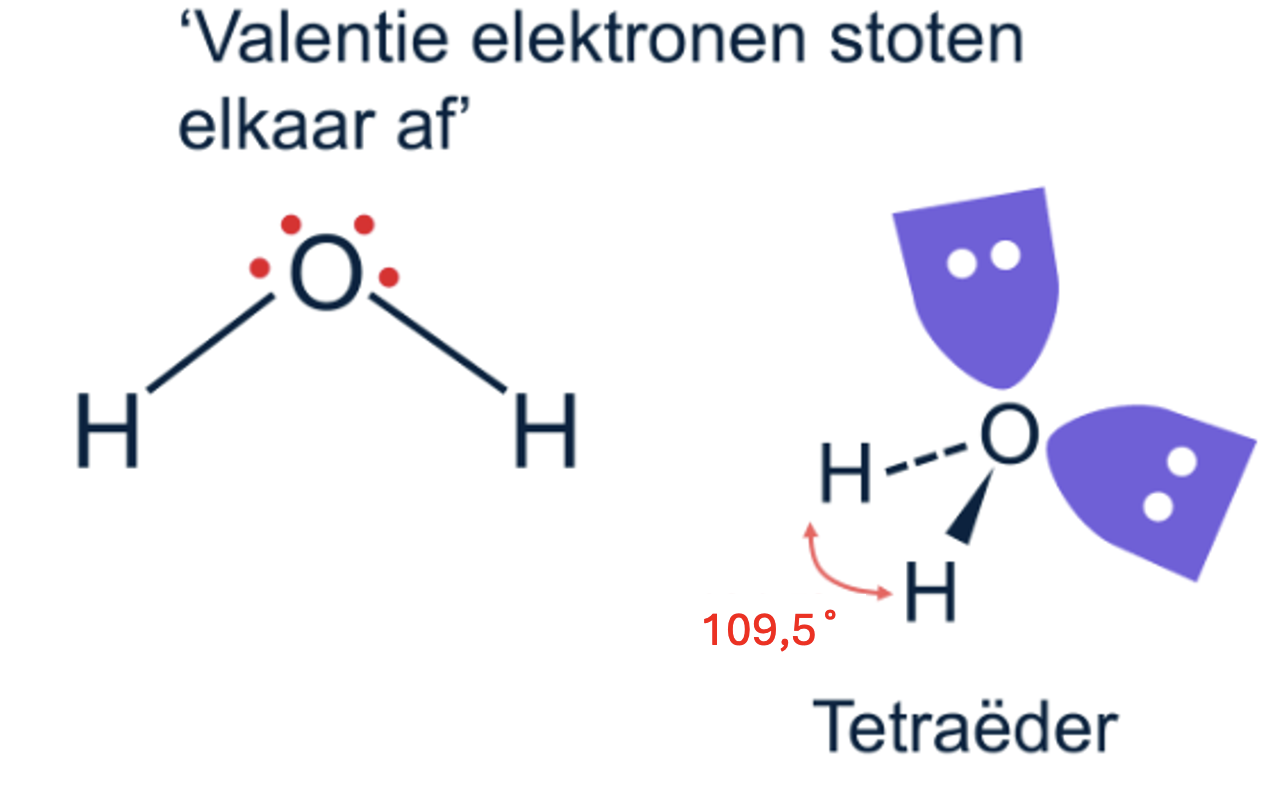
De structuur van water volgens VSEPR
Het Valence Shell Electron Pair Repulsion (VSEPR) model legt uit hoe elektronenparen rond een centraal atoom hun positie kiezen om elkaar maximaal af te stoten. Dit bepaalt de ruimtelijke structuur van een molecuul.
In het geval van water draagt zowel de bindingselektronen als de niet-bindende elektronenparen bij aan zijn tetraëdrische vorm.
Het omringingsgetal en moleculaire structuren
Het omringingsgetal bepaalt de moleculaire structuur. Het wordt berekend door het aantal atomen plus het aantal niet-bindende elektronenparen rond het centrale atoom op te tellen.
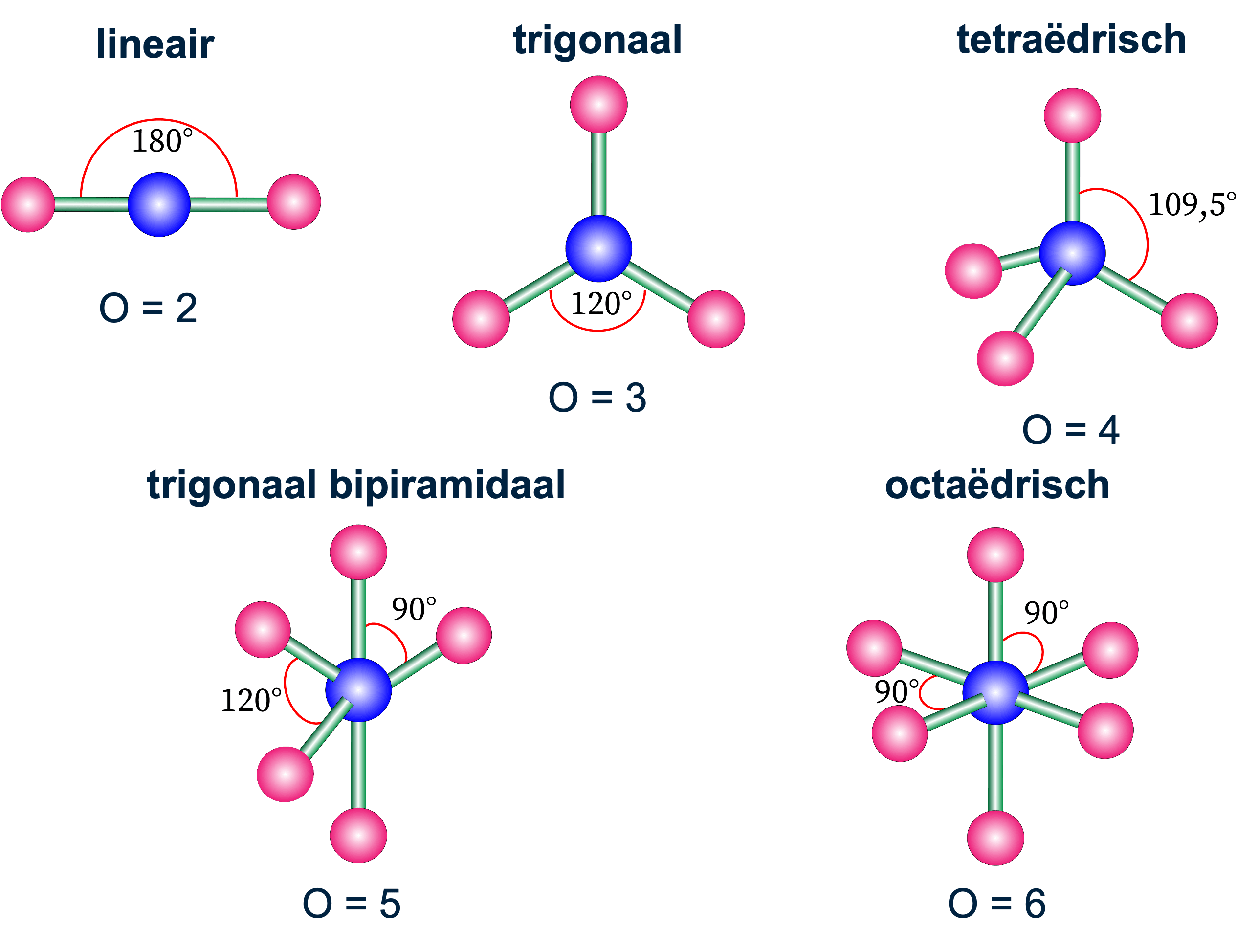
Voorbeelden van structuren
•Lineair (Omringingsgetal = 2): Bijvoorbeeld CO₂, dat geen dipoolmolecuul is ondanks het hebben van polaire atoombindingen.
•Trigonaal (Omringingsgetal = 3): Moleculen met drie atomen of elektronenparen in een plat vlak.
•Tetraëdrisch (Omringingsgetal = 4): Zoals water.
•Trigonaal Bipyramidaal (Omringingsgetal = 5): Met atomen in een plat vlak en een boven en onder.
•Octaëdrisch (Omringingsgetal = 6): Met hoeken van 90 graden tussen de dichtstbijzijnde componenten.
De oplosbaarheid van SO₂ vs CO₂ in water
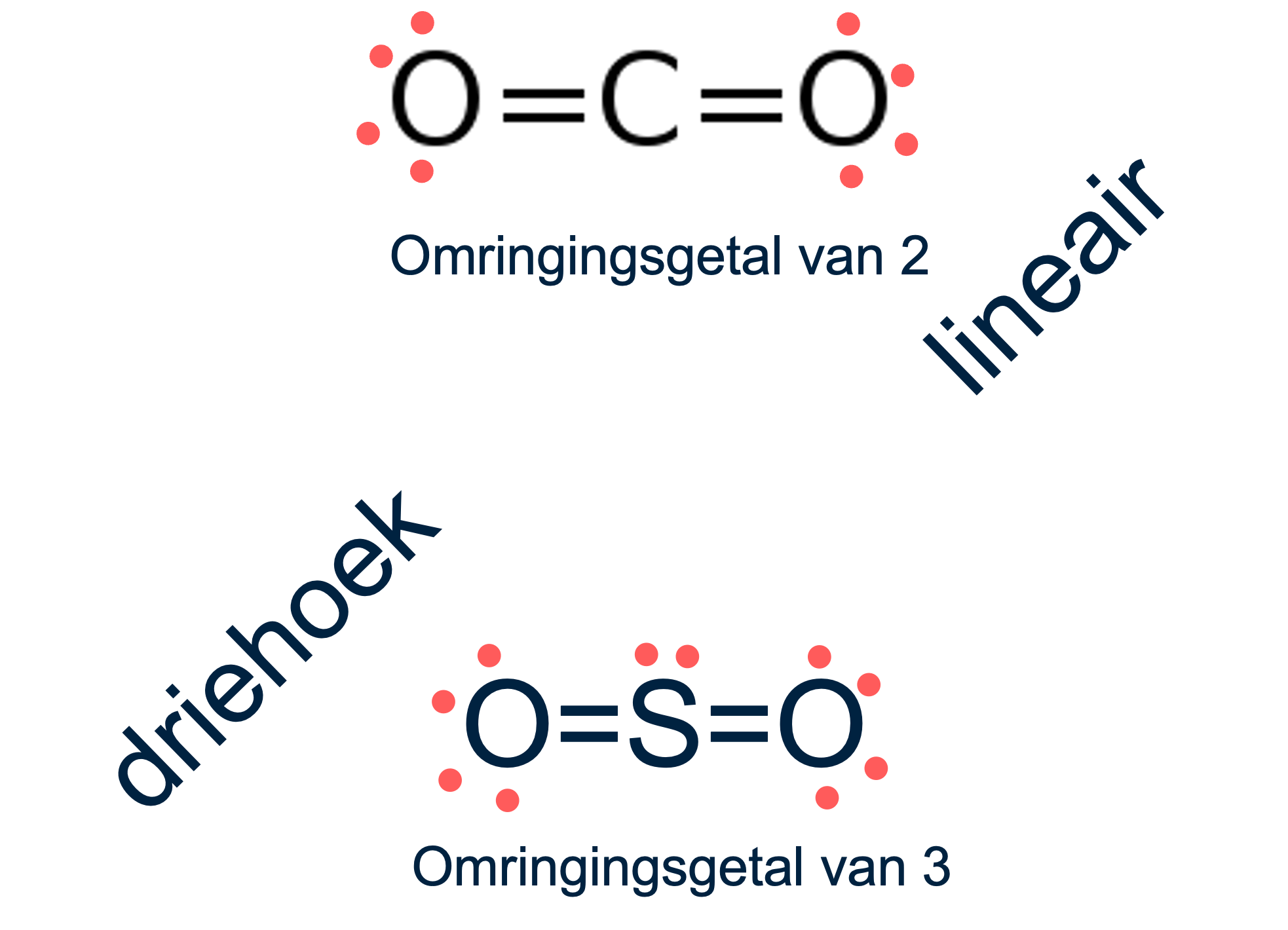
Lewisstructuren Vergelijking:
•CO₂ heeft een lineaire structuur zonder ongebonden elektronenparen.
•SO₂ heeft een trigonale structuur met één ongebonden elektronenpaar op het zwavelatoom.
Omringingsgetal:
•CO₂ heeft een omringingsgetal van 2 (geen ongebonden elektronenparen, alleen twee atomen gebonden).
•SO₂ heeft een omringingsgetal van 3 (twee atomen gebonden en één ongebonden elektronenpaar).
Dipoolkarakter:
•In CO₂ heffen de polaire bindingen elkaar op vanwege de lineaire structuur, waardoor het geen permanente dipool heeft.
•In SO₂ kunnen de polaire bindingen van zwavel naar zuurstof niet volledig tegen elkaar worden weggestreept vanwege de trigonale structuur, wat resulteert in een permanente dipool.
Oplosbaarheid in Water:
Water is een polaire stof en heeft de neiging om andere polaire stoffen op te lossen.
•Omdat CO₂ niet polair is, lost het niet goed op in water.
•SO₂ is polair en kan daarom sterke dipool-dipoolbindingen vormen met watermoleculen, wat leidt tot een betere oplosbaarheid.













