De ontledingsreactie van kaliumchloride
Geef de reactievergelijking van de ontledingsreactie van kaliumchloride.


 Thijs Brouwer
Thijs BrouwerTest je kennis met de 8 examenvragen die aan dit onderwerp zijn gekoppeld.
Geef de reactievergelijking van de ontledingsreactie van kaliumchloride.
In een reactievergelijking komen twee cruciale elementen altijd naar voren: de massabalans en de ladingbalans. De massabalans betekent dat het aantal deeltjes van een bepaalde soort links en rechts gelijk moeten zijn in de vergelijking. De ladingbalans houdt in dat de lading links van de pijl gelijk moet zijn aan de lading rechts van de pijl.
Bij het opstellen een reactievergelijking moet er ook rekening gehouden worden met de toestandsaanduidingen. Dit kan worden aangeduid met 'G' voor gas, 'L' voor vloeistof (liquid), 'S' voor vast (solid) en 'AQ' voor een opgeloste deeltje (aqua). In tabel 10A van Binas kun je de gegevens van vaste stoffen vinden, in tabel 11 de gegevens van vloeistoffen en in tabel 12 de gegevens van gassen en dampen.
Bovendien zijn er een aantal tweeatomige elementen waar rekening mee gehouden moet worden. Deze elementen komen altijd in paren van twee voor in stoffen. Het ezelsbruggetje "Claire fietst naar haar oma in Brussel" kan helpen om te onthouden welke zeven elementen dit zijn: chloor (Cl2), fluor (F2), stikstof (N2), waterstof (H2), zuurstof (O2), jood (I2) en broom (Br2).
Nu de basis begrepen is, is het tijd om aan de hand van een voorbeeld een reactievergelijking op te stellen. Laten we als voorbeeld de vorming van ammoniak (NH3) uit waterstof (H2) en stikstof (N2) nemen.
De reactievergelijking wordt dan H2 + N2 wordt NH3. Hierbij maken we gebruik van de molecuulformules en de massabalans om de correcte verhoudingen van de deeltjes te vinden.
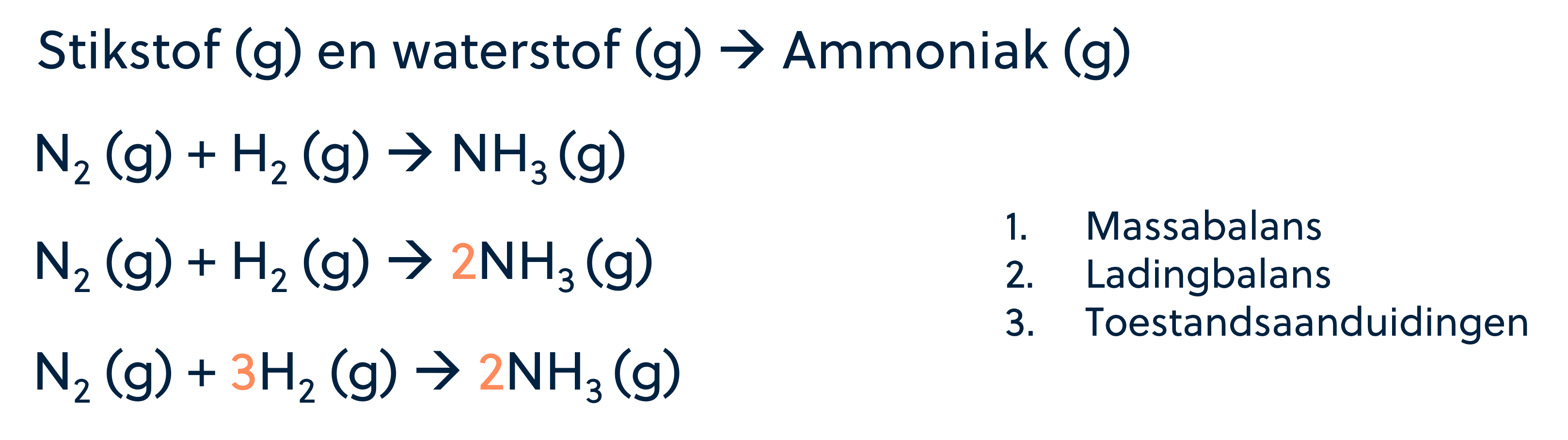
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







