Wat wordt bedoeld met een reactiemechanisme?
Leerdoelen
•Je kunt uitleggen wat een reactiemechanisme is.
•Je kunt het radicaalmechanisme van een substitutiereactie beschrijven.
•Je kunt het ionaire mechanisme van een substitutiereactie beschrijven.
Wat is een reactiemechanisme?
In de kern van elke chemische transformatie ligt een reeks opeenvolgende stappen die samen het reactiemechanisme vormen. Dit mechanisme kan ons vertellen welke atoombindingen worden verbroken en gevormd, en in welke volgorde. Verder worden soms tussenproducten gevormd die cruciaal zijn voor het uiteindelijke reactieproduct. Er zijn twee hoofdtypen mechanismen: het radicaalmechanisme en het ionaire mechanisme, onderscheiden door het gebruik van radicalen (ongepaarde elektronen) of ionen (geladen deeltjes).
De basis van substitutiereacties opgefrist
Bij een substitutiereactie vervangt een atoom of atoomgroep een ander in een koolwaterstof. Een klassiek voorbeeld is de vorming van broommethaan uit broom en methaan, waarbij een waterstofatoom in methaan wordt vervangen door een broomatoom, resulterend in broommethaan en waterstofbromide.
Het radicaalmechanisme uitgelegd
Bij blootstelling aan UV-licht valt een broommolecuul in twee broomradicalen uiteen. Dit proces, bekend als de initiatiefase, start de reactie. Zonder UV-licht kan deze stap niet plaatsvinden, waardoor de reactie niet in het donker kan verlopen.
Vervolgens reageert een broomradicaal in de propagatiefase met een methaanmolecuul door een waterstofatoom van methaan af te splitsen. Daarbij vormt zich waterstofbromide (HBrHBH) en blijft er een methylradicaal (CH_3\cdotCH_3CH_{\placeholder{}}CH) over. Dit methylradicaal reageert verder met een broommolecuul (Br_2Br_{\placeholder{}}Br) om broommethaan (CH_3BrCH_{\placeholder{}}BrCHBr) te vormen en een nieuw broomradicaal te genereren. Op deze manier kan de kettingreactie doorgaan.
De terminatiefase treedt op wanneer twee radicalen met elkaar reageren en zo een stabiel molecuul vormen. Hierbij stopt de kettingreactie. Tijdens de propagatiefase worden de eindproducten van de totaalreactie gevormd, namelijk waterstofbromide () en broommethaan (CH_3BrCH_{\placeholder{}}BrCHBr).
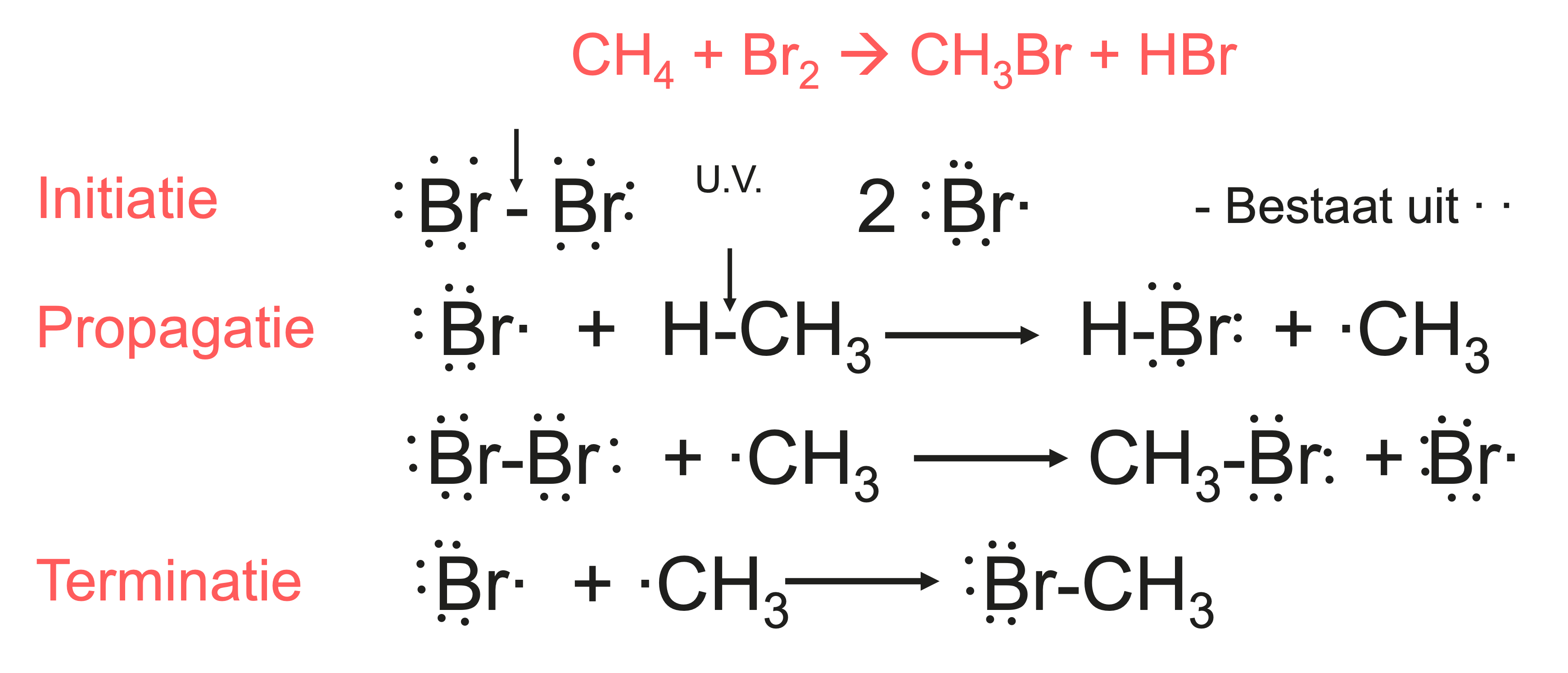
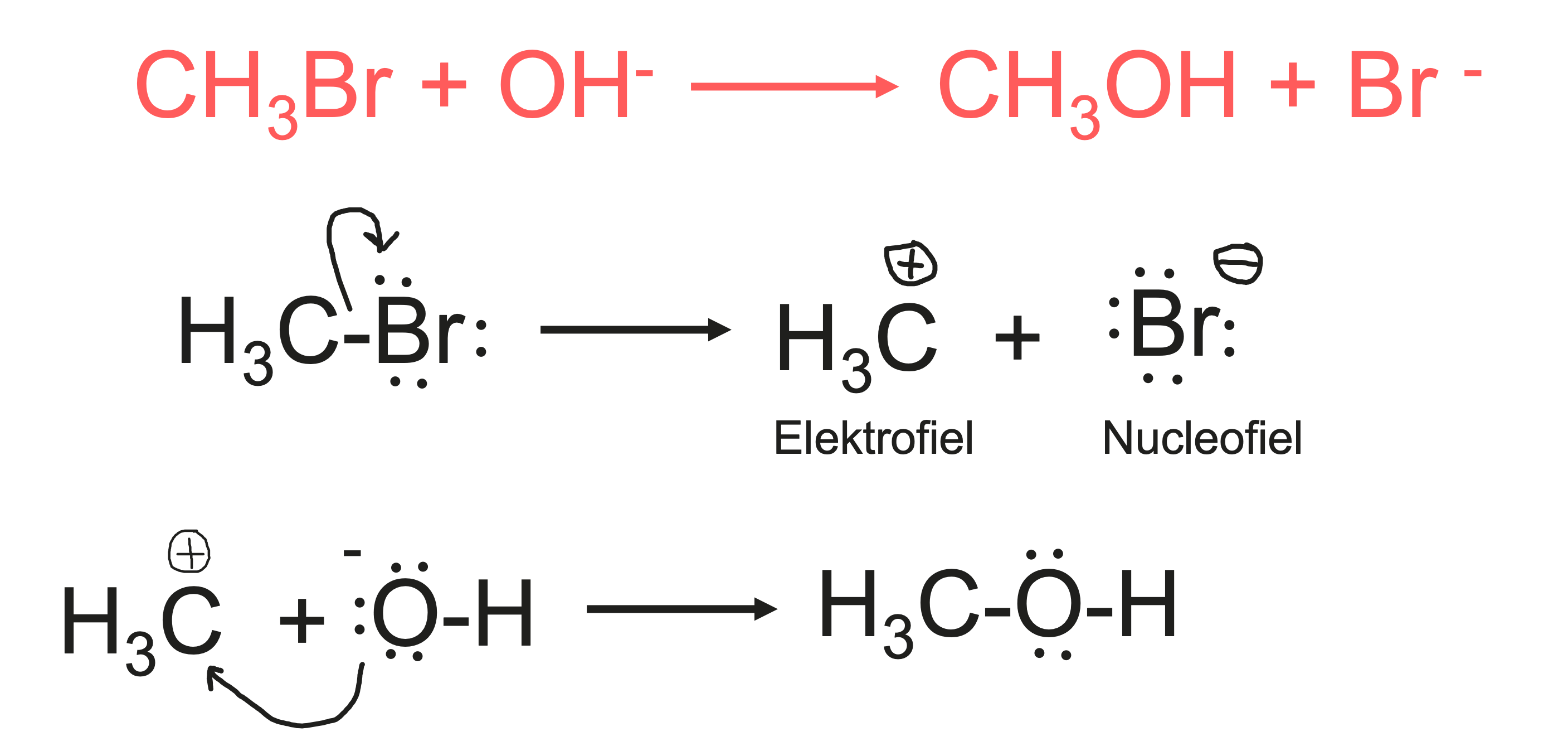
Het ionaire mechanisme verklaard
Een andere manier waarop substitutiereacties kunnen verlopen, is via het ionaire mechanisme. Hierin reageert een geladen deeltje, zoals , met een molecuul om een nieuwe binding te vormen.
In het geval van broommethaan (CH_3BrCH_{\placeholder{}}BrCHBr) vindt de reactie plaats in twee stappen:
•Splitsing van broommethaan
De polaire binding tussen koolstof en broom () kan uiteenvallen doordat broom elektronegatiever is dan koolstof. Hierdoor trekt broom het bindende elektronenpaar naar zich toe, waardoor het molecuul uiteenvalt in een carbokation () en een bromide-ion (Br^{-}Br^{\placeholder{}}Br).
•Vorming van methanol
Het positief geladen carbokation (CH_3^{+}CH_3^{+}CH_3^{\placeholder{}}CH_3CH_{\placeholder{}}CHCH3CH3^{}CH3^{+}CH3^{\placeholder{}}CH3) reageert vervolgens met het negatief geladen hydroxide-ion (OH^{-}OH^{\placeholder{}}OH). Het elektronenpaar van de zuurstof in OH^{-}OH^{\placeholder{}}OH wordt gedeeld met de koolstof, waardoor een nieuwe binding ontstaat en methanol (CH_3OHCH_{\placeholder{}}OHCHOH) wordt gevormd.
Deze reactie laat de wisselwerking zien tussen elektrofiele (deeltjes die elektronen willen aantrekken, zoals ) en nucleofielen (deeltjes die elektronen willen afstaan, zoalsOH^{-}OH^{\placeholder{}}OH ).