Sommige atomen maken soms een uitzondering de octetregel waardoor ze een uitgebreid octet hebben. Welke atomen kunnen dit doen? Kruis ze allemaal aan.
Leerdoelen
•Je kunt de lewisstructuur van eenvoudige moleculen zoals koolstofdioxide opstellen.
•Je kunt met behulp van een stappenplan de lewisstructuur van complexere moleculen zoals methanol opstellen.
•Je kunt het concept van een uitgebreid octet toepassen bij het opstellen van lewisstructuren, zoals bij zwavelzuur, en herkennen wanneer dit van toepassing is.
•Je kunt de lewisstructuur van een radicaal tekenen, de reactiviteit ervan verklaren en de formele lading bepalen.
•Je kunt de lewisstructuur van een samengesteld ion, zoals carbonaation, opstellen en de formele ladingen op de atomen bepalen.
•Je kunt de lewisstructuur van ozon opstellen en de rol ervan in het absorberen van UV-B-straling verklaren.
De basis: Koolstofdioxide en methanol
Koolstofdioxide (CO₂)
Bij het tekenen van de lewisstructuur voorzien we dat koolstof (C) voldoet aan de octetregel doordat het omringd is door acht elektronen: twee dubbele bindingen van elk vier elektronen. Elke zuurstof heeft, naast deze bindingen, nog vier ongebonden elektronen, wat resulteert in een stabiele edelgasconfiguratie voor alle betrokken atomen.
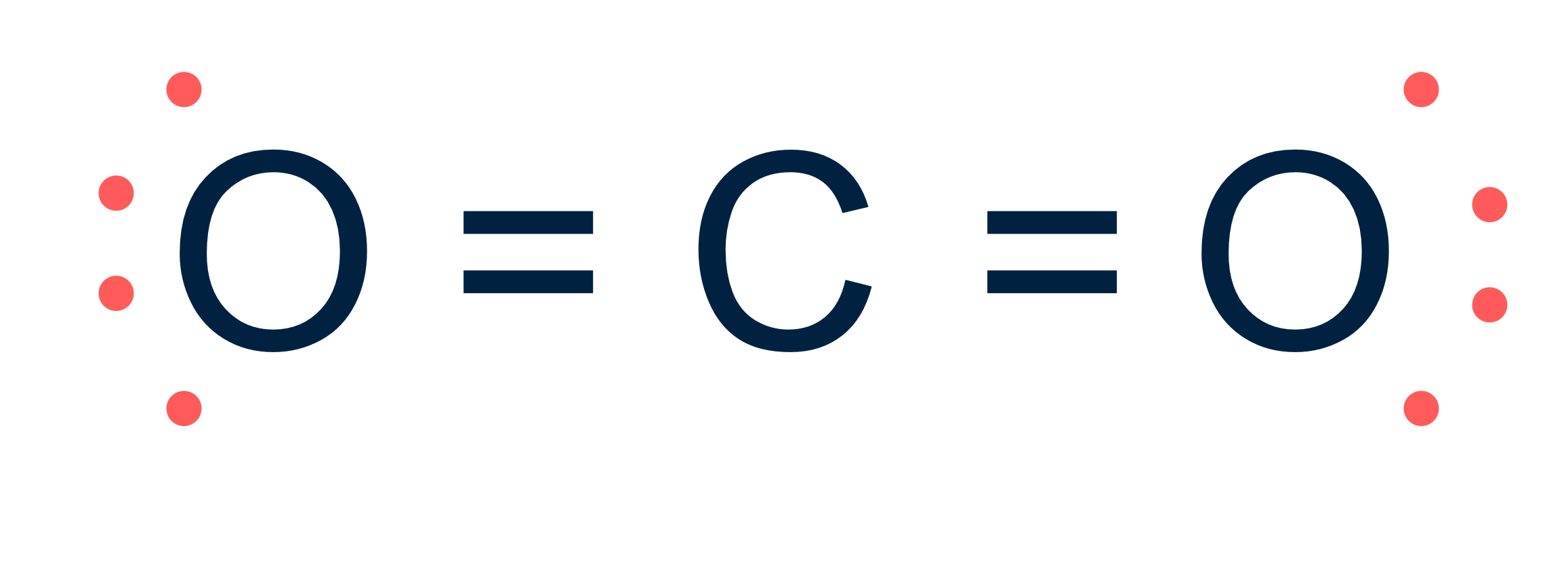
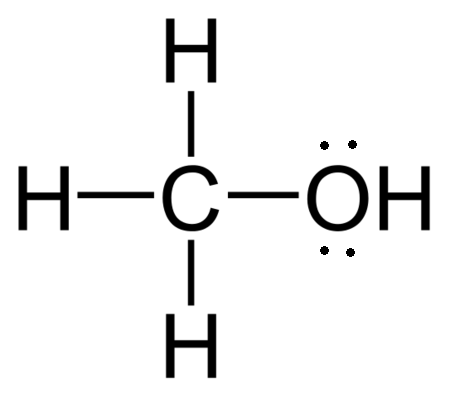
Methanol ()
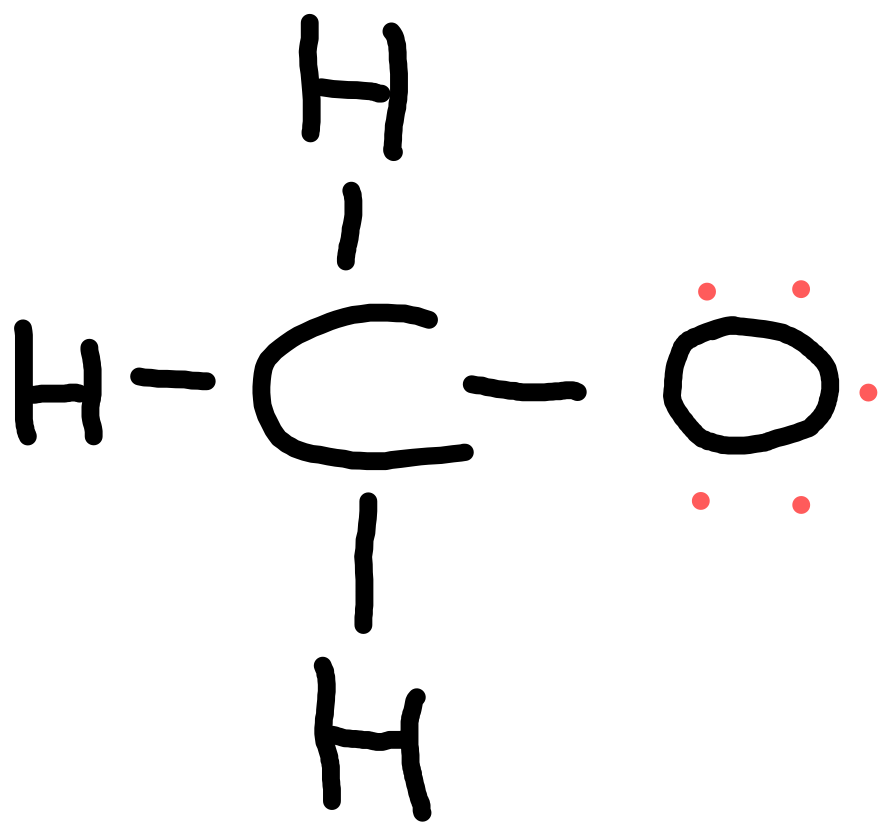
Bij methanol kijken we naar het stappenplan om de lewisstructuur op te stellen. Met in totaal 14 valentie-elektronen en een behoefte aan 24 elektronen voor een volledig octet voor koolstof en zuurstof (en twee voor waterstof), zien we dat er 5 paren gebonden elektronen nodig zijn voor de bindingsstructuur. Dit aantal volgt uit de berekening: (24 benodigde elektronen - 14 valentie-elektronen)/2 = 5 bindingsparen.
Deze gebonden paren zijn drie C-H-bindingen, één C-O-binding en één O-H-binding. De overige 4 valentie-elektronen (14 totaal - 10 voor de bindingen) worden als twee vrije elektronenparen op het zuurstofatoom geplaatst, zodat ook dit atoom aan de octetregel voldoet.
Uitzonderingen en speciale gevallen
Zwavelzuur ()
Zwavel in zwavelzuur demonstreert het uitgebreid octet, met zes bindingen rondom, wat resulteert in 12 gebonden elektronen. Dit toont aan dat zwavel meer dan 8 elektronen kan accommoderen, wat cruciaal is in de structuur van zwavelzuur.

Een uitgebreid octet wordt meestal in een opgave aangegeven, bijvoorbeeld doordat vermeld wordt dat een atoom een covalentie van 5 of 6 heeft. In zulke gevallen weet je dat het element meer dan acht elektronen kan dragen.
Radicaal
Een radicaal is een molecuul dat graag reageert vanwege een ongepaard elektron. Dit ongepaarde elektron maakt het molecuul uiterst reactief. We zien dit bij een zuurstofatoom met een ongepaard elektron, waardoor het geen octet heeft en zeer reactief is. Het zuurstofradicaal heeft daarbij een formele lading van 0, omdat het totaal aantal elektronen dat aan zuurstof wordt toegeschreven gelijk is aan zijn zes valentie-elektronen.
Ion
Bij het tekenen van een lewisstructuur voor een ion, zoals het carbonaation (CO_3^{2-}CO_3^2CO_3^{\placeholder{}}CO_3CO_3^), wordt de lading van het ion meegenomen in de berekening van de valentie-elektronen. Dit resulteert erin dat de negatieve lading terechtkomt als formele ladingen op specifieke atomen, zoals bij het carbonaation waar twee zuurstofatomen elk een formele lading van -1 dragen.
Dit komt doordat deze zuurstofatomen zeven elektronen toegewezen krijgen, één elektron van de atoombinding met koolstof en zes als ongebonden elektronen, terwijl zuurstof van nature zes valantie-elektronen heeft. Daardoor hebben deze zuurstofatomen één elektron te veel, wat leidt tot hun formele lading van -1.
Ozon () en UV-B-absorptie
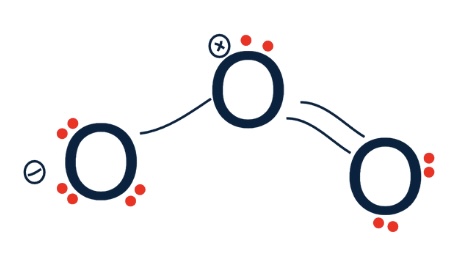
Bij het opstellen van de lewisstructuur van ozon () teken je drie zuurstofatomen op een rij. Deze drie zuurstofatomen zijn met elkaar verbonden via één enkele binding en één dubbele binding, precies zoals zichtbaar wordt in de lewisstructuur van ozon. Daarbij ontstaat een structuur met verschillende formele ladingen.
•Het centrale zuurstofatoom heeft 5 elektronen (2 ongebonden + 3 uit de bindingen), wat één minder is dan zijn 6 valentie-elektronen. Het krijgt een formele lading van +1.
•Het enkelgebonden zuurstofatoom heeft 7 elektronen (6 ongebonden + 1 uit de binding), wat één meer is dan 6 valentie-elektronen. Het krijgt een formele lading van -1.
•Het dubbelgebonden zuurstofatoom heeft precies 6 elektronen, wat overeenkomt met het aantal valentie-elektronen. Het krijgt een formele lading van 0.
Hoewel alle atomen in ozon aan de octetregel voldoen, heeft het molecuul formele ladingen: het middelste atoom is positief geladen en een van de buitenste atomen is negatief geladen.
Wanneer UV-B-straling op het ozonmolecuul valt, wordt de energie van deze straling geabsorbeerd door de binding tussen twee zuurstofatomen. Die binding breekt, waardoor ozon uiteenvalt in zuurstofgas () en een zuurstofradicaal. Omdat de UV-B-energie volledig wordt opgenomen bij het verbreken van die binding, bereikt deze straling de aarde niet. De ozonlaag houdt daarom UV-B-straling tegen, terwijl zuurstofgas dat niet doet.













