Wat is de massa van 1 mol van stof X? En wat is de molaire massa van stof X?
Leerdoelen
•Je kunt vertellen hoeveel deeltjes in een mol zitten.
•Je kunt uitleggen waarom de mol handig is.
•Je kunt uitleggen hoe je de molecuulmassa bepaalt én dat het getal gelijk is aan de molaire massa.
•Je kunt het molrekenschema gebruiken.
•Je kunt rekenen met eenheden.
De mol en het getal van Avogadro
In de scheikunde werken we vaak met extreem kleine deeltjes, zoals atomen, moleculen en ionen. Het is onmogelijk om deze individueel te tellen. Daarom is het concept van de mol bedacht. De mol is een eenheid voor de hoeveelheid stof.
De Italiaanse wetenschapper Amedeo Avogadro bedacht dat één mol altijd hetzelfde aantal deeltjes bevat. Dit aantal staat bekend als het getal van Avogadro (NA) en is gelijk aan 6,02 x 10²³ deeltjes. Deze deeltjes kunnen, afhankelijk van de stof waar je mee werkt, atomen, moleculen of ionen zijn. Of je nu een mol ijzeratomen, een mol watermoleculen of een mol chloride-ionen hebt, het zijn altijd 6,02 x 10²³ deeltjes.
Het verband tussen u en gram: mol
Waarom is juist dit enorme getal, 6,02 x 10²³, gekozen? Het antwoord ligt in het verband tussen de massa van een enkel deeltje en de massa van een mol van die deeltjes.
Een enkel molecuul is ongelooflijk licht. De massa van zo'n klein deeltje wordt uitgedrukt in de atomaire massa-eenheid (u). Het is onpraktisch om deze massa's in kilogrammen uit te drukken, omdat je dan met heel veel nullen achter de komma zou werken.
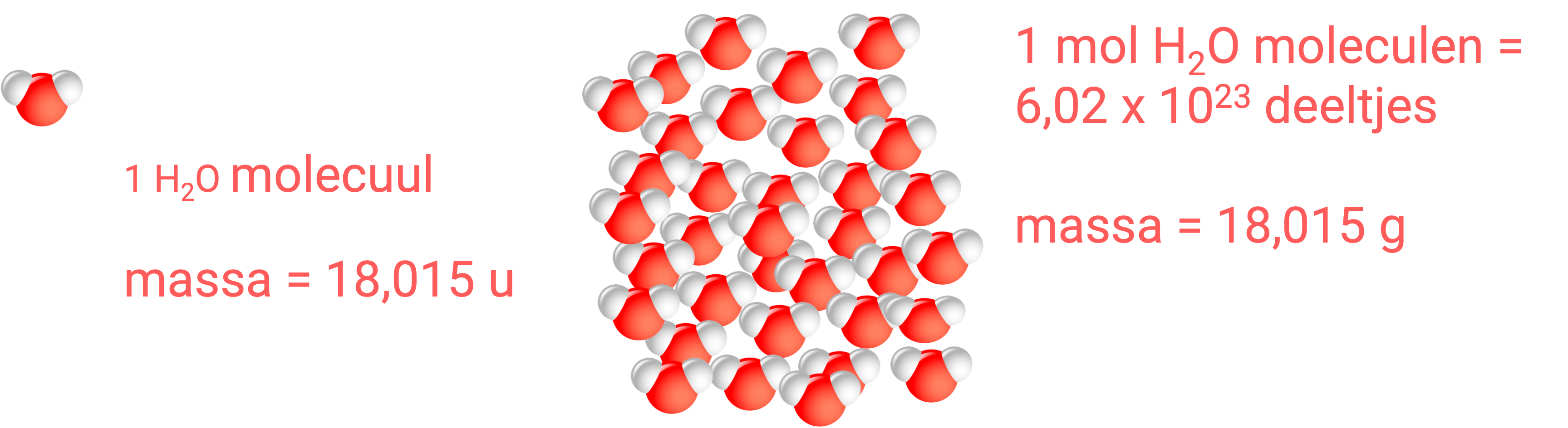
Laten we water (H₂O) als voorbeeld nemen. Een watermolecuul bestaat uit twee waterstofatomen (H) en één zuurstofatoom (O). Als je de massa's van deze atomen bij elkaar optelt (H heeft een massa van ongeveer 1,01 u en O van ongeveer 16,00 u), kom je uit op: 2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (voor O)}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (voor O}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (voor }=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (voor}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (voo}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (vo}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (v}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ (}=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u\text{ }=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(v=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(vo=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(voo=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(voor=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(voorO=18,02u.2\cdot1,01u\text{ (voor H)}+1\cdot16,00u(voorO)=18,02u.2\cdot1,01u\text{ (voor H)}+116,00u(voorO)=18,02u.2\cdot1,01u\text{ (voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01u\text{ (voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01u\text{(voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{(voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u(voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor H)}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor H}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor }+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor h}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor }+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voor}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (voo}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (vo}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (v}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u (}+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u }+1x16,00u(voorO)=18,02u.2\cdot1,01\text{u}+1x16,00u(voorO)=18,02u.2\cdot1,01+1x16,00u(voorO)=18,02u.2\cdot1,01u+1x16,00u(voorO)=18,02u.2\cdot1,01u(+1x16,00u(voorO)=18,02u.2\cdot1,01u(v+1x16,00u(voorO)=18,02u.2\cdot1,01u(vo+1x16,00u(voorO)=18,02u.2\cdot1,01u(voo+1x16,00u(voorO)=18,02u.2\cdot1,01u(voor+1x16,00u(voorO)=18,02u.2\cdot1,01u(voorH+1x16,00u(voorO)=18,02u.2\cdot1,01u(voorH)+1x16,00u(voorO)=18,02u.21,01u(voorH)+1x16,00u(voorO)=18,02u. Dus, één H₂O-molecuul weegt 18,02 u.
Het bijzondere is nu: als je niet één watermolecuul neemt, maar precies één mol watermoleculen (dus 6,02 x 10²³ moleculen), dan wegen deze samen precies 18,02 gram!
Dit is de kern van waarom de mol zo handig is:
•Eén H₂O-molecuul weegt 18,02 u.
•Eén mol H₂O-moleculen weegt 18,02 gram.
Het getal blijft hetzelfde, alleen de eenheid verandert van u naar gram. Dit maakt het veel eenvoudiger om in het laboratorium met meetbare hoeveelheden (grammen) te werken en toch te weten hoeveel deeltjes je hebt.
De molaire massa bepalen
De massa van één mol van een stof noemen we de molaire massa (M). De eenheid van de molaire massa is gram per mol (g/mol). Je kunt de molaire massa van een stof berekenen door de atoommassa's van alle atomen in de molecuulformule bij elkaar op te tellen.
Rekenvoorbeeld: molaire massa van difosforpentoxide (P₂O₅)
1.Zoek de atoommassa's op in het periodiek systeem (of Binas-tabel 99):
1.Fosfor (P): ongeveer 31,0 u
2.Zuurstof (O): ongeveer 16,0 u
2.Bereken de totale massa van de P-atomen:
1.2\cdot31,0u=62,0u231,0u=62,0u2x31,0u=62,0u231,0u=62,0u
3.Bereken de totale massa van de O-atomen:
1.5\cdot16,0u=80,0u516,0u=80,0u
4.Tel de massa's bij elkaar op voor de molecuulmassa:
1.
5.De molecuulmassa is 142,0 u. Dit betekent dat de molaire massa 142,0 gram per mol is.
1.M(P₂O₅) = 142,0 g/mol.
Voor veelgebruikte stoffen hoef je de atoommassa's niet altijd zelf op te tellen; hun molaire massa's zijn vaak te vinden in Binas-tabel 98.
Het molrekenschema
Het molrekenschema is een essentieel hulpmiddel om omrekeningen te maken tussen de massa van een stof (in gram), de hoeveelheid stof (in mol) en het aantal deeltjes. Dit schema is cruciaal voor het oplossen van veel scheikundige vraagstukken, bijvoorbeeld bij het berekenen van hoeveel reactieproduct ontstaat uit een bepaalde hoeveelheid beginstof.
Het schema werkt als volgt:
•Van massa (gram) naar hoeveelheid stof (mol): Je deelt de massa door de molaire massa (M).
•Formule: n = m / M (waarbij n = aantal mol, m = massa in gram, M = molaire massa in g/mol)
•Van hoeveelheid stof (mol) naar aantal deeltjes: Je vermenigvuldigt het aantal mol met het getal van Avogadro (NA).
•Formule:\text{aantal deeltjes}=n\cdot\text{N}_{\text{A}}\text{aantal deeltjes}=n\cdot\text{N}_{\placeholder{}}\text{aantal deeltjes}=n\cdot\text{N}\text{aantal deeltjes}=n\cdot\text{NA}\text{aantal deeltjes}=n\cdot\text{N}\text{aantal deeltjes}=n\cdot\text{Na}\text{aantal deeltjes}=n\cdot\text{N}\text{aantal deeltjes}=n\cdot\text{aantal deeltjes}=n\cdot N\text{aantal deeltjes}=n\cdot NA\text{aantal deeltjes}=nNA\text{aantal deeltjes}=n*NA\text{aantal deeltjes }=n*NA\text{aantal deeltjes}=n*NA\text{aantal deeltje}=n*NA\text{aantal deeltj}=n*NA\text{aantal deelt}=n*NA\text{aantal deel}=n*NA\text{aantal dee}=n*NA\text{aantal deet}=n*NA\text{aantal dee}=n*NA\text{aantal de}=n*NA\text{aantal d}=n*NA\text{aantal }=n*NA\text{aantal}=n*NA\text{aanta}=n*NA\text{aant}=n*NA\text{aan}=n*NA\text{aa}=n*NA\text{a}=n*NA=n*NA
•Van aantal deeltjes naar hoeveelheid stof (mol): Je deelt het aantal deeltjes door het getal van Avogadro (NA).
•Van hoeveelheid stof (mol) naar massa (gram): Je vermenigvuldigt het aantal mol met de molaire massa (M).
•Formule: m=n\cdot Mm=nM
Het is belangrijk om bij elke stap te bedenken waar je bent en waar je naartoe wilt in het schema.

Rekenen met eenheden
Soms kan het lastig zijn om te onthouden of je nu moet vermenigvuldigen of delen. Een handige methode om dit te controleren of af te leiden, is door te 'rekenen met eenheden'. Het principe is simpel: de eenheden aan de linkerkant van een vergelijking moeten overeenkomen met de eenheden aan de rechterkant.
Laten we als voorbeeld kijken hoe je van massa (gram) naar hoeveelheid stof (mol) komt. Je hebt een massa in gram (g) en je wilt een hoeveelheid stof in mol (mol) krijgen. Stel je voor dat je een formule hebt: g\cdot X=molgX=mol. Wat moet X zijn?
1.Je wilt van de eenheid 'gram' af. Om dit te doen, moet 'gram' in de noemer van X staan, zodat de grammen tegen elkaar wegvallen.
1.g\cdot(iets/g)=molg(iets/g)=mol
2.Je wilt de eenheid 'mol' overhouden. Dus 'mol' moet in de teller van X staan.
1.g\cdot(mol/g)=molg(mol/g)=mol
De eenheid van X moet dus 'mol/g' zijn. De molaire massa (M) heeft de eenheid 'g/mol'. Dit is precies het omgekeerde van 'mol/g'. Dus, als je de massa (g) vermenigvuldigt met (mol/g), is dat hetzelfde als de massa (g) delen door de molaire massa (g/mol).
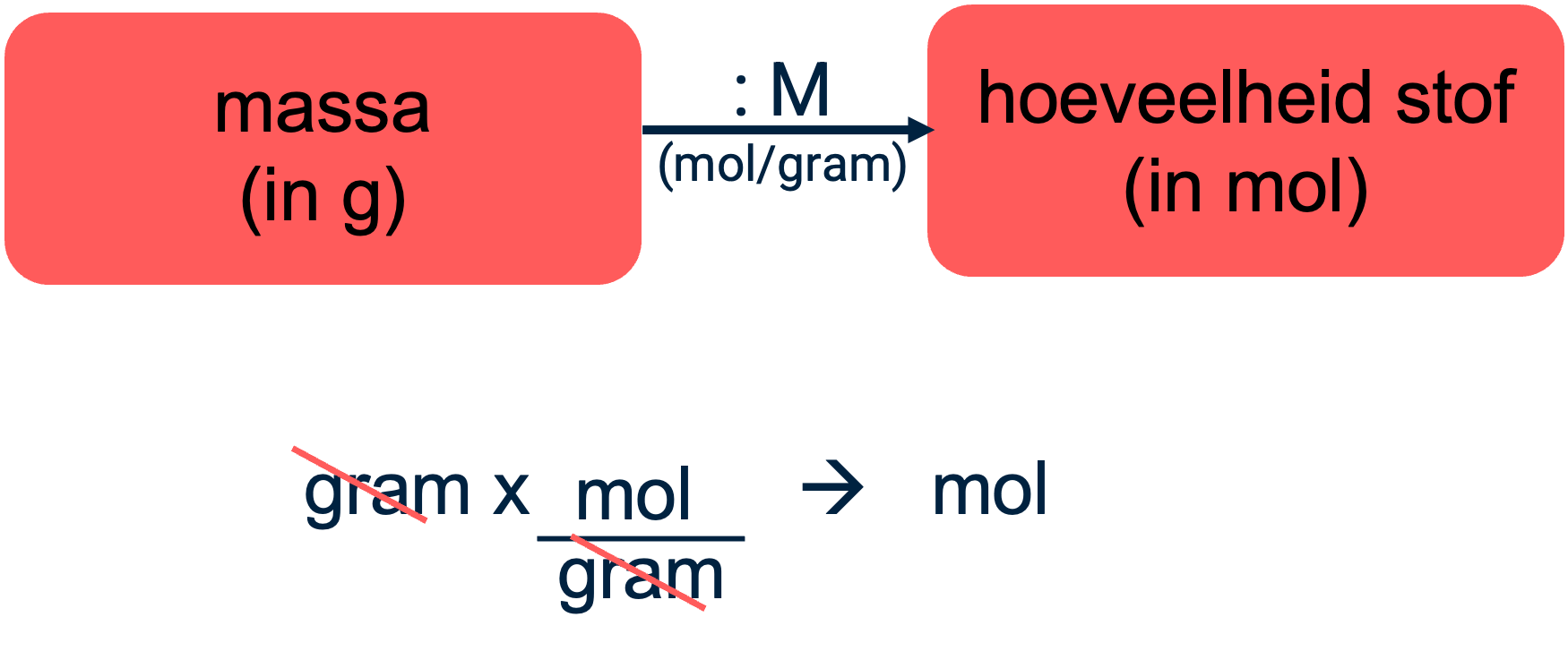
Conclusie: om van gram naar mol te gaan, moet je delen door de molaire massa (M). Deze methode van rekenen met eenheden kan je helpen om formules af te leiden en te controleren, en is vooral nuttig bij complexere berekeningen in hogere klassen of vervolgopleidingen.
Rekenvoorbeeld: hoeveel watermoleculen in een glas water?
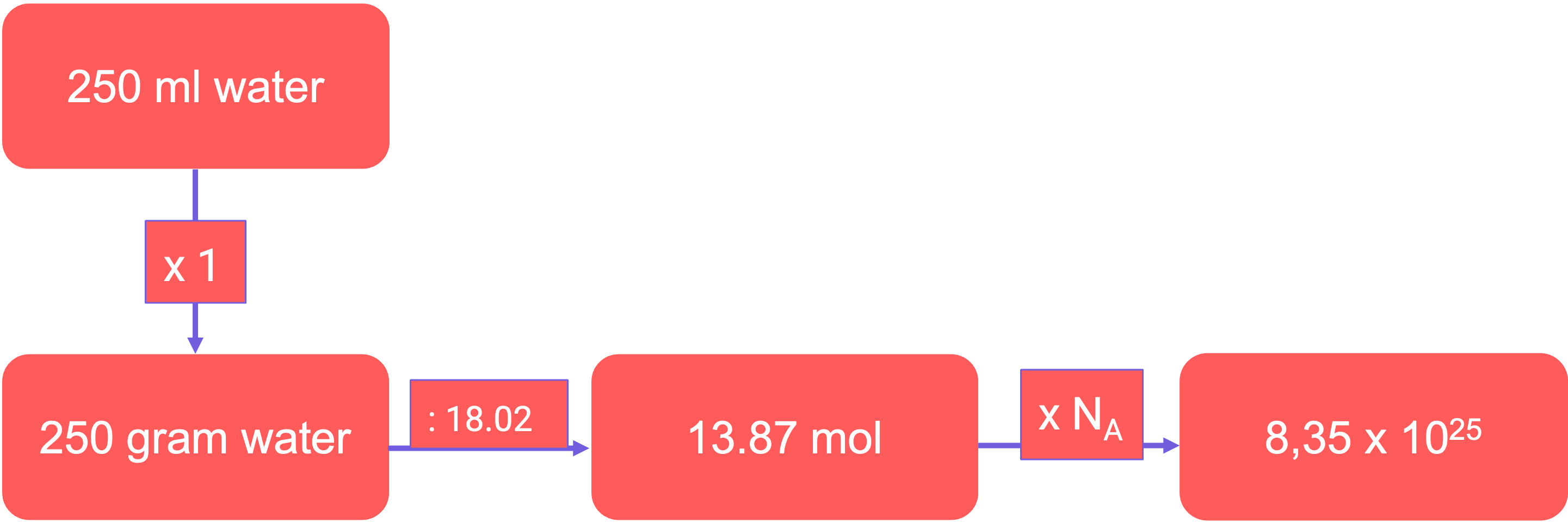
Laten we de centrale vraag beantwoorden: hoeveel watermoleculen zitten er in een glas water van 250 milliliter?
Om dit te berekenen, breiden we het molrekenschema uit met het volume en de dichtheid.
Stap 1: Volume omzetten naar massa We hebben het volume van water (250 ml). Om dit om te zetten naar massa (gram), gebruiken we de dichtheid van water. De dichtheid van water is ongeveer 1 gram per milliliter (1 g/ml).
•\text{massa = volume }\cdot\text{ dichtheid}\text{massa = volume }\cdot\text{ dichthei}\text{massa = volume }\cdot\text{ dichthe}\text{massa = volume }\cdot\text{ dichth}\text{massa = volume }\cdot\text{ dicht}\text{massa = volume }\cdot\text{ dich}\text{massa = volume }\cdot\text{ dic}\text{massa = volume }\cdot\text{ di}\text{massa = volume }\cdot\text{ d}\text{massa = volume }\cdot\text{ }\text{massa = volume }\cdot\text{massa = volume}\cdot\text{massa = volume}\text{massa = volume }\text{massa = volume \textasteriskcentered}\text{massa = volume \textasteriskcentered }\text{massa = volume \textasteriskcentered d}\text{massa = volume \textasteriskcentered dc}\text{massa = volume \textasteriskcentered d}\text{massa = volume \textasteriskcentered }\text{massa = volume \textasteriskcentered}\text{massa = volume }\text{massa = volume x}\text{massa = volume }\text{massa = volume}\text{massa = volum}\text{massa = volu}\text{massa = vol}\text{massa = vo}\text{massa = v}\text{massa = }\text{massa =}\text{massa }\text{massa}\text{mass}\text{mas}\text{ma}\text{m}Massa=Volume*Dchtheid
•\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{ gram}\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{ gra}\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{ gr}\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{ g}\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{ }\text{massa }=250\text{mL}\cdot1\text{g/mL}=250\text{massa }=250\text{mL}\cdot1\text{g/mL}=250g\text{massa }=250\text{mL}\cdot1\text{g/mL}=250ga\text{massa }=250\text{mL}\cdot1\text{g/mL}=250gam\text{massa }=250\text{mL}\cdot1\text{g/mL}=250gram\text{massa}=250\text{mL}\cdot1\text{g/mL}=250gram\text{mass}=250\text{mL}\cdot1\text{g/mL}=250gram\text{mas}=250\text{mL}\cdot1\text{g/mL}=250gram\text{ma}=250\text{mL}\cdot1\text{g/mL}=250gram\text{m}=250\text{mL}\cdot1\text{g/mL}=250gram=250\text{mL}\cdot1\text{g/mL}=250gramMassa=250\text{mL}\cdot1\text{g/mL}=250gramMassa=250\text{mL}\cdot1\text{g/m}=250gramMassa=250\text{mL}\cdot1\text{g/}=250gramMassa=250\text{mL}\cdot1\text{g}=250gramMassa=250\text{mL}\cdot1=250gramMassa=250\text{mL}\cdot1g=250gramMassa=250\text{mL}\cdot1g/=250gramMassa=250\text{mL}\cdot1g/m=250gramMassa=250\text{mL}\cdot1g/ml=250gramMassa=250\text{m}\cdot1g/ml=250gramMassa=250\cdot1g/ml=250gramMassa=250m\cdot1g/ml=250gramMassa=250ml\cdot1g/ml=250gramMassa=250ml1g/ml=250gram
Stap 2: Massa omzetten naar hoeveelheid stof (mol) Nu we de massa in gram hebben (250 g), kunnen we deze omzetten naar mol. Hiervoor hebben we de molaire massa van water (H₂O) nodig.
•\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ g/mol}.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ g/mo}.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ g/m}.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ g/}.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ g}.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02\text{ }.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02g.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02g/.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02g/m.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02g/mo.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O)}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor O}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor }=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voor}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (voo}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (vo}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (v}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol (}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol }=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mol}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/mo}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/m}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g/}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ g}=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00\text{ }=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00g=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1\cdot16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+116,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H)}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor H}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor }+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voor}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (voo}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (vo}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (v}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol (}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol }+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mol}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/mo}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/m}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g/}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ g}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{ }+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01\text{g}+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2\cdot1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=21,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_2O)=2*1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H_{\placeholder{}}O)=2*1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(HO)=2*1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.\text{M}(H2O)=2*1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.(H2O)=2*1,01g/mol(voorH)+1*16,00g/mol(voorO)=18,02g/mol.
•\text{Aantal mol }=\text{ massa / molaire massa}\text{Aantal mol }=\text{ massa / molaire mass}\text{Aantal mol }=\text{ massa / molaire mas}\text{Aantal mol }=\text{ massa / molaire ma}\text{Aantal mol }=\text{ massa / molaire m}\text{Aantal mol }=\text{ massa / molaire }\text{Aantal mol }=\text{ massa / molaire}\text{Aantal mol }=\text{ massa / molair}\text{Aantal mol }=\text{ massa / molai}\text{Aantal mol }=\text{ massa / mola}\text{Aantal mol }=\text{ massa / mol}\text{Aantal mol }=\text{ massa / mo}\text{Aantal mol }=\text{ massa / m}\text{Aantal mol }=\text{ massa / }\text{Aantal mol }=\text{ massa /}\text{Aantal mol }=\text{ massa }\text{Aantal mol }=\text{ massa}\text{Aantal mol }=\text{ mass}\text{Aantal mol }=\text{ mas}\text{Aantal mol }=\text{ ma}\text{Aantal mol }=\text{ m}\text{Aantal mol }=\text{ }\text{Aantal mol }=\text{ }\text{Aantal mol }=\text{Aantal mol }=\text{m}\text{Aantal mol }=\text{ma}\text{Aantal mol }=\text{m}\text{Aantal mol }=\text{Aantal mol }=M\text{Aantal mol }=Ma\text{Aantal mol }=Mas\text{Aantal mol }=Mass\text{Aantal mol }=Massa/Molairemassa\text{Aantal mol}=Massa/Molairemassa\text{Aantal mo}=Massa/Molairemassa\text{Aantal moo}=Massa/Molairemassa\text{Aantal mool}=Massa/Molairemassa\text{Aantal moo}=Massa/Molairemassa\text{Aantal mo}=Massa/Molairemassa\text{Aantal m}=Massa/Molairemassa\text{Aantal }=Massa/Molairemassa\text{Aantal}=Massa/Molairemassa\text{Aanta}=Massa/Molairemassa\text{Aant}=Massa/Molairemassa\text{Aan}=Massa/Molairemassa\text{Aa}=Massa/Molairemassa\text{A}=Massa/Molairemassa=Massa/MolairemassaA=Massa/MolairemassaAa=Massa/MolairemassaAan=Massa/MolairemassaAant=Massa/MolairemassaAanta=Massa/MolairemassaAantal=Massa/MolairemassaAantalm=Massa/MolairemassaAantalmo=Massa/MolairemassaAantalmol=Massa/MolairemassaAantalmol(=Massa/MolairemassaAantalmol(n=Massa/Molairemassa
•n=\frac{250\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{25\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{2\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{3\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{35\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{350\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{35\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{3\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{3\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=2\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=25\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mol}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ mo}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ m}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ }n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ ,}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ ,o}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ ,}n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ }n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87\text{ }n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87n=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87mn=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87mon=250\frac{\text{ g }}{18,02\text{ g/mol}}=13,87moln=250\frac{\text{ g }}{18,02\text{ g/mo}}=13,87moln=250\frac{\text{ g }}{18,02\text{ g/m}}=13,87moln=250\frac{\text{ g }}{18,02\text{ g/}}=13,87moln=250\frac{\text{ g }}{18,02\text{ g}}=13,87moln=250\frac{\text{ g }}{18,02\text{ }}=13,87moln=250\frac{\text{ g }}{18,02}=13,87moln=250\frac{\text{ g }}{18,02}g=13,87moln=250\frac{\text{ g }}{18,02}g/=13,87moln=250\frac{\text{ g }}{18,02}g/m=13,87moln=250\frac{\text{ g }}{18,02}g/mo=13,87moln=250\frac{\text{ g }}{18,02}g/mol=13,87moln=250\frac{\text{ g }}{\placeholder{}}g/mol=13,87moln=250\frac{\text{ g }}{\placeholder{}}18,02g/mol=13,87moln=250\text{ g }18,02g/mol=13,87moln=250\text{ g}18,02g/mol=13,87moln=250\text{ }18,02g/mol=13,87moln=25018,02g/mol=13,87moln=250g18,02g/mol=13,87moln=25018,02g/mol=13,87moln=250\text{g}18,02g/mol=13,87moln=25018,02g/mol=13,87moln=250g18,02g/mol=13,87mol
Stap 3: Hoeveelheid stof (mol) omzetten naar aantal deeltjes Tot slot zetten we het aantal mol om naar het aantal watermoleculen met behulp van het getal van Avogadro (NA = 6,02 x 10²³ deeltjes/mol).
•\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avogadro}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avogadr}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avogad}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avoga}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avog}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Avo}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van Av}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van A}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van }\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van a}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van }\text{Aantal deeltjes = aantal mol }\cdot\text{ getal van}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal va}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal v}\text{Aantal deeltjes = aantal mol }\cdot\text{ getal }\text{Aantal deeltjes = aantal mol }\cdot\text{ getal}\text{Aantal deeltjes = aantal mol }\cdot\text{ geta}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao }\text{Aantal deeltjes = aantal mol }\cdot\text{ getao v}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao va}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao vaj}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao va}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao v}\text{Aantal deeltjes = aantal mol }\cdot\text{ getao }\text{Aantal deeltjes = aantal mol }\cdot\text{ getao}\text{Aantal deeltjes = aantal mol }\cdot\text{ geta}\text{Aantal deeltjes = aantal mol }\cdot\text{ get}\text{Aantal deeltjes = aantal mol }\cdot\text{ ge}\text{Aantal deeltjes = aantal mol }\cdot\text{ g}\text{Aantal deeltjes = aantal mol }\cdot\text{ }\text{Aantal deeltjes = aantal mol }\cdot\text{ }\text{Aantal deeltjes = aantal mol }\cdot\text{ }g\text{Aantal deeltjes = aantal mol }\cdot\text{ }ge\text{Aantal deeltjes = aantal mol }\cdot\text{ }get\text{Aantal deeltjes = aantal mol }\cdot\text{ }geta\text{Aantal deeltjes = aantal mol }\cdot\text{ }get\text{Aantal deeltjes = aantal mol }\cdot\text{ }ge\text{Aantal deeltjes = aantal mol }\cdot\text{ }g\text{Aantal deeltjes = aantal mol }\cdot\text{ }\text{Aantal deeltjes = aantal mol }\cdot\text{ }\text{Aantal deeltjes = aantal mol }\cdot\text{Aantal deeltjes = aantal mol }\text{Aantal deeltjes = aantal mol}\text{Aantal deeltjes = aantal mol }\text{Aantal deeltjes = aantal mol}\text{Aantal deeltjes = aantal mo}\text{Aantal deeltjes = aantal m}\text{Aantal deeltjes = aantal }\text{Aantal deeltjes = aantal}\text{Aantal deeltjes = aanta}\text{Aantal deeltjes = aant}\text{Aantal deeltjes = aan}\text{Aantal deeltjes = aa}\text{Aantal deeltjes = a}\text{Aantal deeltjes = }\text{Aantal deeltjes =}\text{Aantal deeltjes }\text{Aantal deeltjes}\text{Aantal deeltje}\text{Aantal deeltj}\text{Aantal deelt}\text{Aantal deel}\text{Aantal dee}\text{Aantal de}\text{Aantal d}\text{Aantal }\text{Aantal}\text{Aanta}\text{Aant}\text{Aan}\text{Aa}\text{A}AAaAanAantAantaAantalAantaldAantaldeAantaldeeAantaldeelAantaldeeltAantaldeeltjAantaldeeltjeAantaldeeltjesAantaldeeltjes=Aantaldeeltjes=AAantaldeeltjes=AaAantaldeeltjes=AanAantaldeeltjes=AantAantaldeeltjes=AantaAantaldeeltjes=AantalAantaldeeltjes=AantalmAantaldeeltjes=AantalmoAantaldeeltjes=AantalmolAantaldeeltjes=Aantalmol*Aantaldeeltjes=Aantalmol*GAantaldeeltjes=Aantalmol*GeAantaldeeltjes=Aantalmol*GetAantaldeeltjes=Aantalmol*GetaAantaldeeltjes=Aantalmol*GetalAantaldeeltjes=Aantalmol*GetalvAantaldeeltjes=Aantalmol*GetalvaAantaldeeltjes=Aantalmol*GetalvanAantaldeeltjes=Aantalmol*GetalvanAAantaldeeltjes=Aantalmol*GetalvanAvAantaldeeltjes=Aantalmol*GetalvanAvoAantaldeeltjes=Aantalmol*GetalvanAvogAantaldeeltjes=Aantalmol*GetalvanAvogaAantaldeeltjes=Aantalmol*GetalvanAvogadAantaldeeltjes=Aantalmol*GetalvanAvogadr
•
Dus, in een glas water van 250 milliliter zitten maar liefst 8,35 x 10²⁵ watermoleculen! Dat is een gigantisch aantal. Om je een idee te geven: als elk van deze moleculen zo groot zou zijn als een knikker, dan zouden we met z'n allen op de hele wereld tot aan onze knieën in de knikkers staan!