Geef van onderstaande stoffen aan of het een metaal is, een zout of een moleculaire stof:
1. CH_4CH
2.
3. CaCO_3CaCO
4.
5. H_2H
6. Fe_2O_3Fe_2OFe_2O3FeO3
7. Brons (een legering van koper en tin)


 Thijs Brouwer
Thijs BrouwerGeef van onderstaande stoffen aan of het een metaal is, een zout of een moleculaire stof:
1. CH_4CH
2.
3. CaCO_3CaCO
4.
5. H_2H
6. Fe_2O_3Fe_2OFe_2O3FeO3
7. Brons (een legering van koper en tin)
•Je kunt uitleggen wat de kapstok van de scheikunde is.
•Je kunt uitleggen welke deeltjes je nodig hebt voor het geleiden van stroom en wat die deeltjes moeten kunnen.
•Je kunt uitleggen welke soorten roosters er allemaal zijn.
•Je kunt uitleggen welke bindingen je hebt binnen die roosters.
In de scheikunde gebruiken we een handige 'kapstok' om stoffen in te delen. Deze kapstok heeft drie haakjes, oftewel drie hoofdcategorieën: metalen, zouten en moleculaire stoffen. Om te bepalen onder welke categorie een stof valt, stel je jezelf de vraag: welke elementen zitten er in de formule van de stof? Zitten er metalen in of niet-metalen?
De samenstelling van de elementen bepaalt de categorie:
•Alleen metalen: Als een stof uitsluitend uit metaalelementen bestaat, is het een metaal.
•Metaal en niet-metaal: Als een stof bestaat uit een combinatie van metaalelementen en niet-metaalelementen, is het een zout.
•Alleen niet-metalen: Als een stof uitsluitend uit niet-metaalelementen bestaat, is het een moleculaire stof.

Om te bepalen of een element een metaal of een niet-metaal is, gebruik je Tabel 99 uit je Binas. Hierin zijn metalen vaak geel gekleurd en niet-metalen groen. Zo is zuurstof (O) een niet-metaal en calcium (Ca) een metaal.
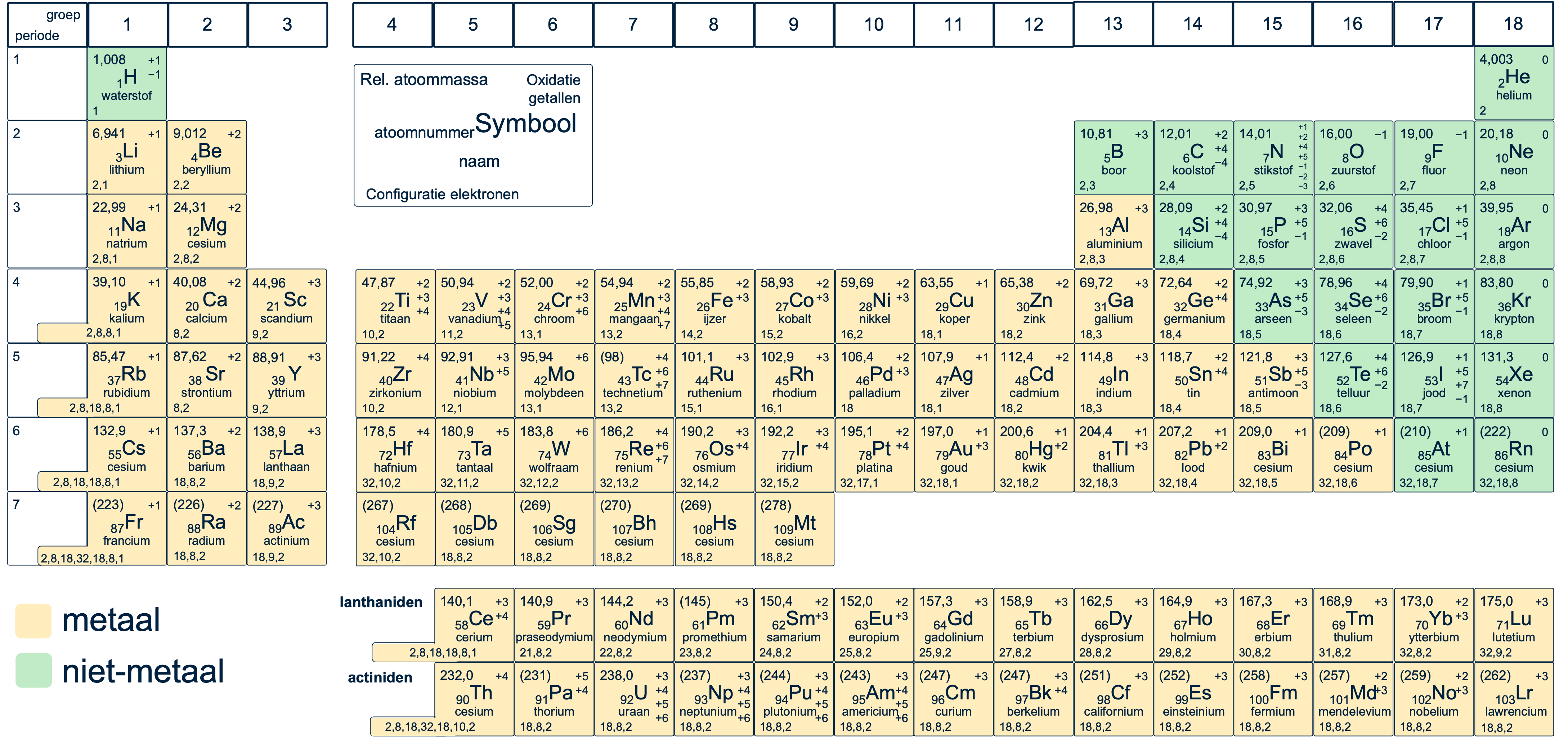
Soms zie je in het periodiek systeem een derde categorie: de overgangsmetalen. Deze elementen bevinden zich op de grens tussen metalen en niet-metalen en hebben vaak een afwijkende kleur. Van deze elementen is niet altijd direct aan te geven of ze onderdeel zijn van een zout of een moleculaire stof; soms kunnen ze beide rollen vervullen. Voor nu richten we ons echter op de duidelijke indeling in metalen, zouten en moleculaire stoffen.
Of een stof stroom kan geleiden, hangt af van twee belangrijke voorwaarden. Deze voorwaarden kun je toepassen op metalen, zouten en moleculaire stoffen om te bepalen of ze geleidend zijn:
1.Er moeten geladen deeltjes aanwezig zijn.
2.Deze geladen deeltjes moeten kunnen bewegen.
Metalen zijn een belangrijke categorie stoffen die we dagelijks tegenkomen, bijvoorbeeld in elektrische kabels of constructies.

•Metalen bestaan uit alleen metaalatomen (of metaalionen met bijbehorende elektronen).
•Ze geleiden altijd stroom, omdat ze vrije elektronen bezitten die kunnen bewegen.
•De atomen/ionen in metalen zijn gerangschikt in een metaalrooster.
•De deeltjes in dit rooster worden bij elkaar gehouden door een metaalbinding.
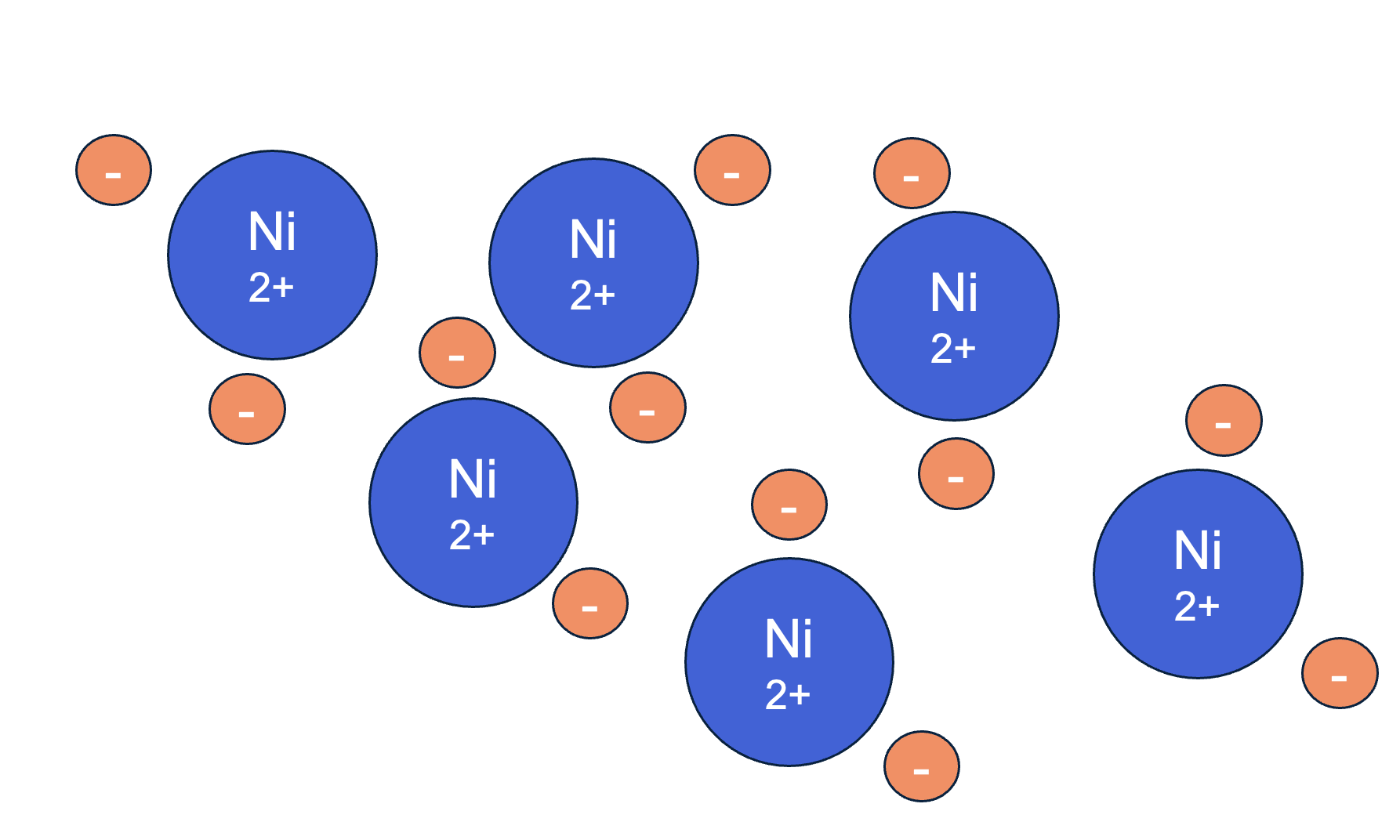
In een metaalrooster staan metaalatomen gerangschikt. Deze atomen staan elektronen af en vormen zo positieve metaalionen. De afgestane elektronen bewegen vrij door het hele metaalrooster en vormen een soort 'elektronenwolk'. Deze vrij bewegende elektronen en de positieve metaalionen trekken elkaar aan door elektrostatische interactie. Dit zorgt ervoor dat de metaalionen bij elkaar blijven en de metaalbinding ontstaat.
Een voorbeeld is een nikkelion (Ni²⁺) met twee vrije valentie-elektronen. Deze elektronen zijn niet gebonden aan één specifiek atoom, maar kunnen vrij door het hele rooster bewegen. Dit is essentieel voor de stroomgeleiding. Als je een stroompje aan de ene kant van een metaal aansluit, kunnen de elektronen door het metaal heen bewegen en aan de andere kant weer uittreden.
Zouten zijn een andere belangrijke categorie stoffen, die we bijvoorbeeld kennen als keukenzout (natriumchloride).

•Zouten bevatten zowel metaalelementen als niet-metaalelementen.
•Ze bestaan uit positieve en negatieve ionen.
•Een zout geleidt alleen stroom als de ionen vrij kunnen bewegen. Dit is het geval wanneer het zout vloeibaar is (gesmolten) of opgelost in een vloeistof (bijvoorbeeld water).
•In de vaste fase geleidt een zout geen stroom, omdat de ionen dan vast op hun plek zitten en alleen trillen. Ze kunnen niet bewegen.
•De ionen in zouten zijn gerangschikt in een ionrooster.
•De deeltjes in dit rooster worden bij elkaar gehouden door een ionbinding.
•Zouten hebben vaak een hoog smeltpunt vanwege de sterke ionbinding.
In een ionrooster wisselen positieve en negatieve ionen elkaar af. Elk positief ion is omringd door negatieve ionen, en elk negatief ion is omringd door positieve ionen. Deze afwisseling zorgt voor een sterke aantrekking tussen de tegengesteld geladen ionen door elektrostatische interactie. Deze aantrekkingskracht vormt de ionbinding, die de ionen stevig bij elkaar houdt in het rooster. Een zoutkristal, zoals een korrel keukenzout, is op microniveau op deze manier opgebouwd.

De laatste categorie zijn de moleculaire stoffen, zoals water of suiker.

•Moleculaire stoffen bestaan uitsluitend uit niet-metaalelementen.
•Ze bestaan uit ongeladen moleculen.
•Moleculaire stoffen geleiden nooit stroom, omdat ze geen geladen deeltjes bevatten.
•In de vaste fase zijn de moleculen gerangschikt in een molecuulrooster.
•De moleculen trekken elkaar aan door vanderwaalsbindingen.
•Binnen een molecuul worden de atomen bij elkaar gehouden door atoombindingen.
In de vaste fase zijn de ongeladen moleculen van een moleculaire stof gerangschikt in een molecuulrooster. Wanneer de stof vloeibaar wordt, kunnen de moleculen vrijer bewegen. In de gasfase bewegen ze volledig vrij en raken ze elkaar nauwelijks meer aan.
De aantrekkingskracht tussen de moleculen onderling wordt de vanderwaalsbinding genoemd. Hoe groter de massa van een molecuul, hoe sterker de vanderwaalsbinding en hoe hoger het kookpunt van de stof.
Naast de vanderwaalsbinding kan er bij sommige moleculen een extra sterke aantrekkingskracht zijn: de waterstofbrug. Deze treedt op wanneer een molecuul OH- en/of NH-groepen bevat, zoals bij water (H₂O). Door kleine partiële ladingen op de atomen ontstaat er een extra aantrekking tussen moleculen.
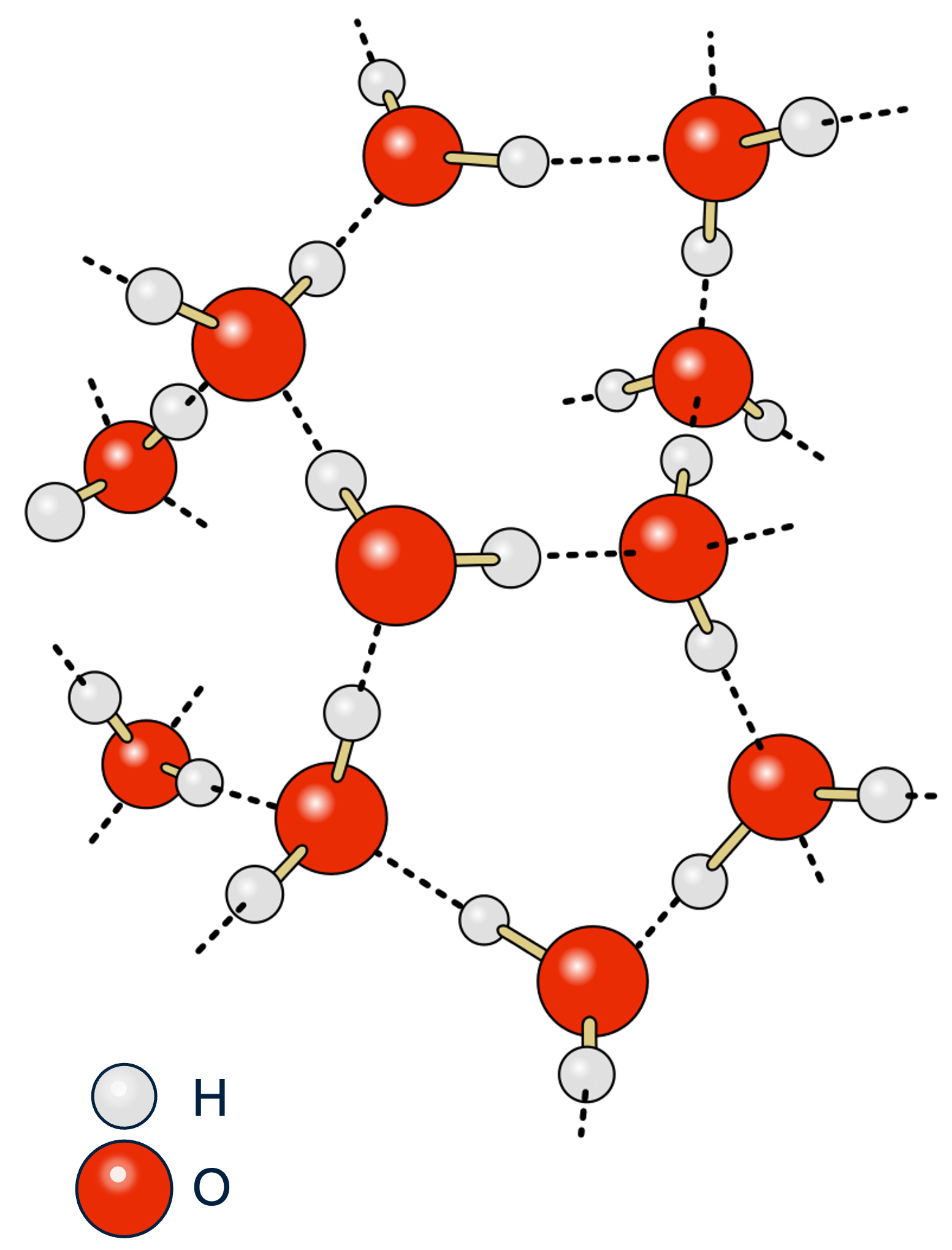
Puur water (gedestilleerd water) is een moleculaire stof en geleidt geen stroom, omdat het geen geladen deeltjes bevat. Het is echter gevaarlijk om in een zwembad te zijn tijdens onweer. Dit komt niet door het water zelf, maar door de opgeloste ionen (zouten) die in zwembadwater aanwezig zijn. Deze ionen kunnen vrij bewegen en zorgen ervoor dat het water geleidend wordt.
Moleculaire stoffen zoals ijs (H₂O) bestaan dus geheel uit niet-metalen en zijn slechte geleiders. Water geleidt niet in zuivere vorm. De atomen waterstof (H) en zuurstof (O) zijn namelijk beiden niet-metalen.
Een voorbeeld hiervan is de combinatie van een afbeelding van een elektrische kabel (vaak van koper) met een tekening van een nikkelrooster. Hoewel beide metalen zijn, is het belangrijk om te beseffen dat het specifieke voorbeeld (nikkel) niet direct overeenkomt met de algemene afbeelding (koperkabel). Blijf altijd scherp en controleer of de gepresenteerde informatie en beelden logisch bij elkaar passen.


Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







