Wat is een van de belangrijkste conclusies van Rutherford over de bouw van een atoom?
Leerdoelen
•Je kunt het atoommodel van Dalton, Rutherford en Bohr beschrijven en uitleggen
•Je kunt de bouw van een atoom weergeven met behulp van het atoomnummer
•Je kunt het begrip ‘massagetal’ en ‘isotoop’ uitleggen
•Je kunt uitleggen waarom er wordt gewerkt met gemiddelde atoommassa's
Atoommodel van Dalton
Het atoommodel van Dalton stelt dat atomen kleine, ondeelbare bolletjes zijn. Elk atoom heeft een andere diameter, afhankelijk van het atoomnummer. Dalton gebruikte kleuren om verschillende elementen te vertegenwoordigen, zoals rood voor zuurstof en zwart voor koolstof. In deze fase werd de structuur van atomen nog niet verder onderzocht.

Atoommodel van Rutherford
Later kwam Rutherford met een nieuw model na zijn experiment met heliumkernen die hij op een gouden folie afvuurde. Hij ontdekte dat de meeste heliumkernen door het folie heen gingen, wat hem leidde tot de conclusie dat atomen voor het grootste deel uit lege ruimte bestaan.
In Rutherford zijn model bevinden de protonen en neutronen zich in een dichte kern, terwijl de elektronen zich in een “leefruimte” eromheen bevinden. Dit model benadrukt dat atomen grotendeels leeg zijn en dat elektronen niet op gestructureerde wijze om de kern bewegen.
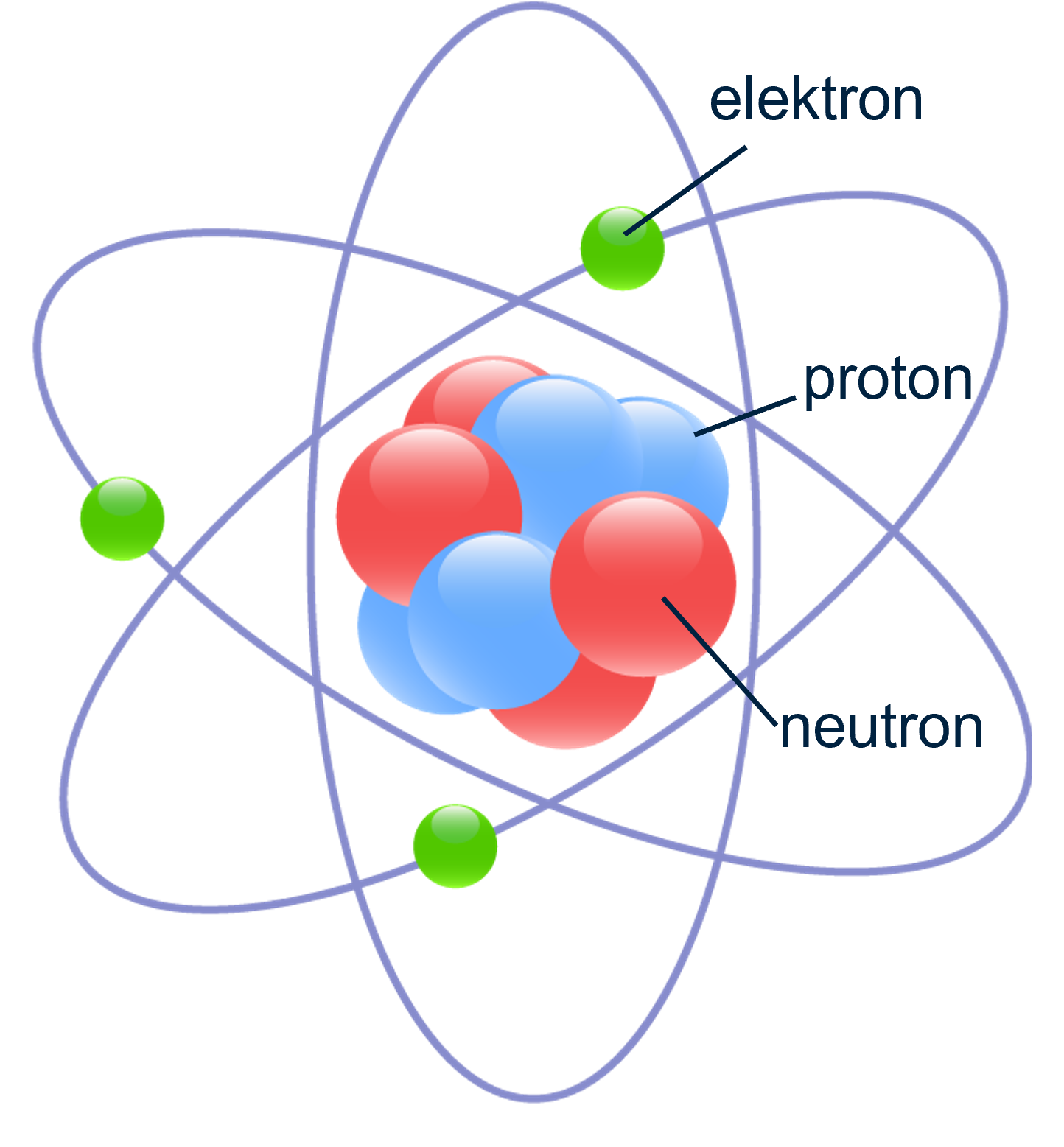
Atoommodel van Bohr
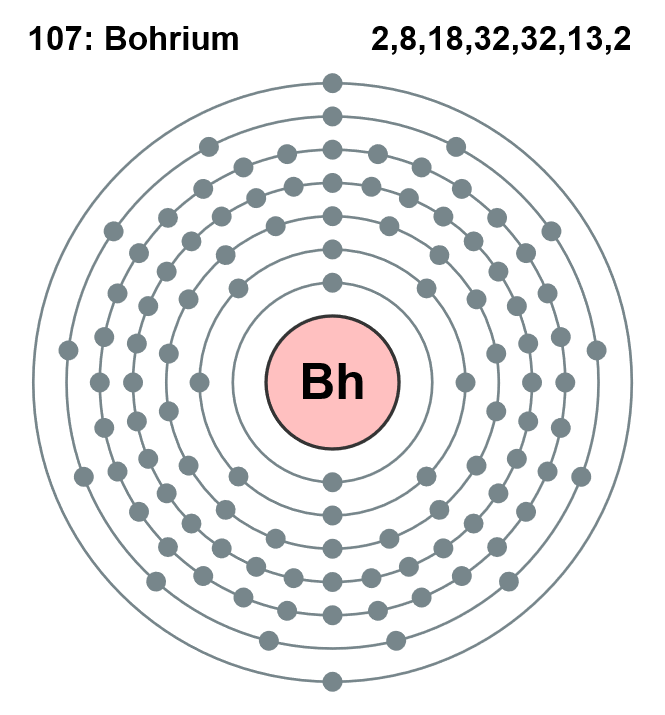
Bohr paste het atoommodel van Rutherford aan door te stellen dat elektronen zich in vaste banen, ook wel schillen genoemd, rondom de kern bewegen. Deze schillen zijn genummerd:
K-schil: max. 2 elektronen
L-schil: max. 8 elektronen
M-schil: max. 18 elektronen
In Bohr zijn model was het belangrijk dat de elektronen niet willekeurig rond de kern bewegen, maar in specifieke schillen blijven.
Kenmerken van atomen
Atoomnummer
Het atoomnummer is gelijk aan het aantal protonen in de kern van een atoom. Dit nummer bepaalt de identiteit van een element.
Massagetal
Het massagetal is het totaal aantal protonen en neutronen in de kern. Het aantal elektronen is gelijk aan het aantal protonen in een neutraal atoom.
Trends in het periodiek systeem
Het periodiek systeem toont trends in de eigenschappen van elementen. Elk element heeft een uniek atoomnummer, wat het aantal protonen in de kern vertegenwoordigt. De eigenschappen van een element worden vaak bepaald door de verdeling van elektronen in de schillen.
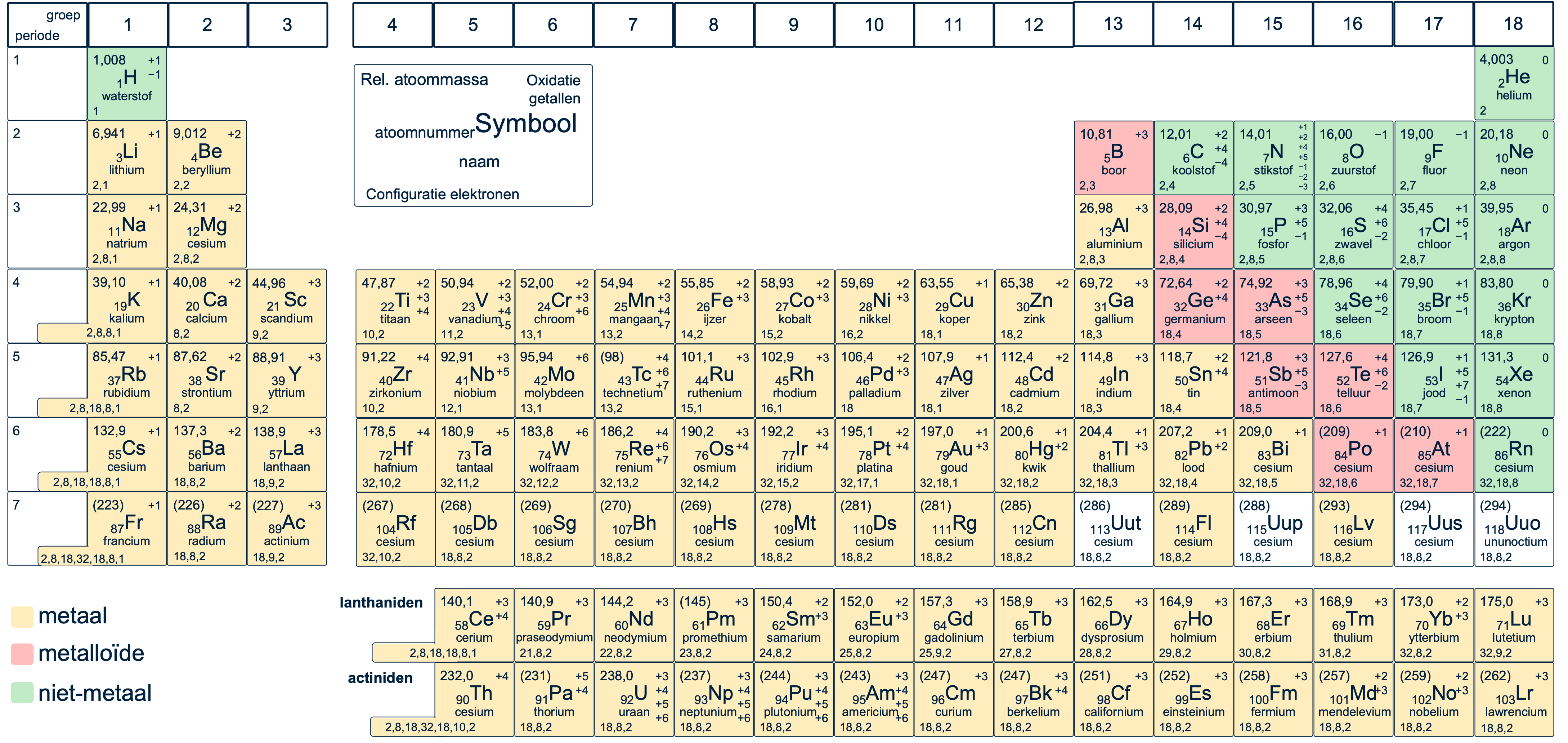
Isotopen
Isotopen zijn atomen van hetzelfde element die een verschillend aantal neutronen hebben. Hierdoor kunnen ze een andere massa hebben. Voorbeeld: Koper-63 (29 protonen, 34 neutronen) en Koper-65 (29 protonen, 36 neutronen).
Gemiddelde atoommassa
In het periodiek systeem worden gemiddelde atoommassa's weergegeven, gebaseerd op de relatieve hoeveelheden van de isotopen die natuurlijk voorkomen. Dit wordt berekend door het gewogen gemiddelde van de isotopen. Bijvoorbeeld, voor koper:
Er komt in de natuur 69,17% Cu-63 met massa getal 63 en 30,83% Cu-65 met massa getal 65 voor.
Dan is de gemiddelde atoommassa gelijk aan=
\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,61\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,6\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,3\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,32\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,324\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{100}=63,3241\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{10}=63,3241\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{1}=63,3241\frac{\left(69{,}17\cdot63+30{,}83\cdot65\right)}{\placeholder{}}=63,3241\left(69{,}17\cdot63+30{,}83\cdot65\right)=63,324169{,}17\cdot63+30{,}83\cdot65)=63,324169{,}17\cdot63+30{,}83\cdot65=63,324169{,}17\cdot63+30{,}8\cdot65=63,324169{,}17\cdot63+30{,}\cdot65=63,324169{,}17\cdot63+30{,}3\cdot65=63,324169{,}17\cdot63+30{,}38\cdot65=63,324169{,}17\cdot63+3038\cdot65=63,324169{,}17\cdot63+338\cdot65=63,324169{,}17\cdot63+38\cdot65=63,324169{,}17\cdot63+038\cdot65=63,324169{,}17\cdot63+0{,}38\cdot65=63,324169{,}17\cdot63+0{,}338\cdot65=63,324169{,}17\cdot63+0{,}3038\cdot65=63,32416917\cdot63+0{,}3038\cdot65=63,3241617\cdot63+0{,}3038\cdot65=63,324117\cdot63+0{,}3038\cdot65=63,3241017\cdot63+0{,}3038\cdot65=63,32410{,}17\cdot63+0{,}3038\cdot65=63,32410{,}617\cdot63+0{,}3038\cdot65=63,32410{,}6917\cdot63+0{,}3038\cdot65=63,32410{,}6917\cdot63+0{,}3038\cdot65=0{,}6917\cdot63+0{,}3038\cdot65=50{,}6917\cdot63+0{,}3038\cdot65=550{,}6917\cdot63+0{,}3038\cdot65={,}550{,}6917\cdot63+0{,}3038\cdot65=3{,}550{,}6917\cdot63+0{,}3038\cdot65=63{,}550{,}6917\cdot63+0{,}3038\cdot65=63{,}50{,}6917\cdot63+0{,}3038\cdot65=63{,}0{,}6917\cdot63+0{,}3038\cdot65=630{,}6917\cdot63+0{,}3038\cdot65=60{,}6917\cdot63+0{,}3038\cdot65=0{,}6917\cdot63+0{,}3038\cdot650{,}6917\cdot63+0{,}3038\cdot65+0{,}6917\cdot63+0{,}3038\cdot650{,}6917\cdot63+0{,}3038\cdot60{,}6917\cdot63+0{,}3038\cdot0{,}6917\cdot63+0{,}30380{,}6917\cdot63+0{,}3030{,}6917\cdot63+0{,}300{,}6917\cdot63+0{,}30{,}6917\cdot63+0{,}0{,}6917\cdot63+00{,}6917\cdot63+0{,}6917\cdot630{,}6917\cdot60{,}6917\cdot0{,}69170{,}6910{,}690{,}60{,}0
Dit geeft een gemiddelde atoommassa van ongeveer 63{,}55u6355u, wat in het periodiek systeem staat.













