Een aangezuurde permanganaatoplossing
Bij een oplossing van methanal wordt een oplossing van aangezuurde kaliumpermanganaat toegevoegd. Hieronder staan meerdere totaalvergelijkingen en kruis de juiste aan.

Totaalreacties zijn heel belangrijk in de scheikunde, vooral wanneer we kijken naar redoxreacties, die plaats kunnen vinden in verschillende omgevingen: zuur, basisch of neutraal. Dit artikel behandelt hoe de omgeving de totaalreacties beïnvloedt en hoe je deze kunt opstellen.
De omgeving waarin een reactie zich afspeelt, speelt een cruciale rol bij het bepalen van de halfreacties:
•Zuur milieu: Hierin is er een aanwezigheid van H+ ionen. Dit betekent dat de reactie plaatsvindt in een omgeving waar zuur (bijvoorbeeld azijnzuur) aanwezig is.
•Basisch milieu: In deze omgeving zijn er OH- ionen. Dit kan bijvoorbeeld betekenen dat de reactie plaatsvindt in een oplossing van natriumhydroxide.
•Neutraal milieu: Dit houdt in dat de oplossing niet zuur of basisch is, maar dat er wel H2O (water) aanwezige is. H2O hoeft niet altijd expliciet in de vergelijking te staan.
Het stappenplan voor het opstellen van totaalreacties blijft consistent, ongeacht de omgeving. Een belangrijk aspect om te onthouden is dat in een zuur milieu H+ betrokken is en in een basisch milieu OH-.

Stel je voor dat je methanal (H2CO) toevoegt aan een aangezuurde waterstofperoxide oplossing.
In een zuur milieu zijn we op zoek naar de halfreactie van waterstofperoxide, die er als volgt uitziet:
H2O2 + 2 e- + 2 H+ ⇄ 2 H2O (l)
In dit geval is het belangrijk om de H+ aanwezig te hebben om de oxidator te kunnen selecteren.
Voor de reductor, in dit geval methanal (H2CO), hebben we een andere halfreactie nodig. Deze moet omgedraaid worden, omdat deze als reductor fungeert.
De redoxreactie die optreedt als je reductor methanal bij een aangezuurde waterstofperoxide oplossing voegt, ziet er als volgt uit: H2CO + H2O (l) ⇄ HCOOH + 2 H+ + 2 e-
Wanneer je de halfreacties optelt, kun je de elektronen wegstrepen. Zorg dat je de reacties goed op orde hebt. Als totaal reactie krijg je dan:
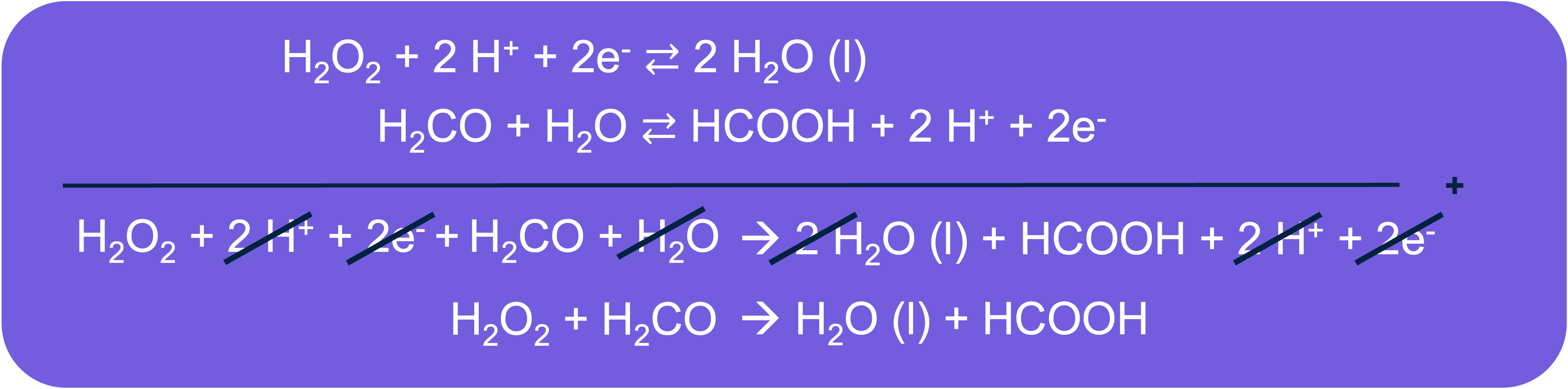
Hieruit volgt dat waterstofperoxide en methanol reageren tot water en mierenzuur (HCOOH).
In een basisch milieu werkt het proces vergelijkbaar, maar dan moeten we rekening houden met de OH- ionen in plaats van H+. De aanpak en het stappenplan blijven hetzelfde, maar de betrokken ionen veranderen afhankelijk van het milieu.


 Thijs Brouwer
Thijs BrouwerBij een oplossing van methanal wordt een oplossing van aangezuurde kaliumpermanganaat toegevoegd. Hieronder staan meerdere totaalvergelijkingen en kruis de juiste aan.
Totaalreactie in zure of basische omgeving: uitleg, samenvatting en oefenen
Krijg de beste uitleg over basisch milieu, binas tabel 48, halfreactie oxidator, halfreactie reductor, neutraal milieu, redox, totaalreactie en zuur milieu. Op deze pagina vind je:
Ondersteund door Ainstein, onze AI-hulp die je vragen stap voor stap beantwoordt.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







