Sterk naar zwak
Sorteer de volgende stoffen van meest sterke naar minst sterke reductor. Gebruik hiervoor je BiNaS tabel 48.


 Thijs Brouwer
Thijs BrouwerSorteer de volgende stoffen van meest sterke naar minst sterke reductor. Gebruik hiervoor je BiNaS tabel 48.
•Wat oxidators en reductors zijn
•Wat ‘edelheid’ betekent
•Waar je halfreacties vindt in de BiNaS
Bij scheikunde spelen oxidatoren en reductoren een cruciale rol in redoxreacties. Deze reacties zijn belangrijk voor diverse processen in de natuur en industrie. Om deze reacties goed te begrijpen en toe te passen, hebben we BiNaS tabel 48.
Een reductor is een deeltje dat elektronen af kan staan. Een goed voorbeeld hiervan is koper (Cu), dat verandert in koperionen (Cu²⁺) door twee elektronen af te staan. Aan de andere kant heb je oxidatoren: deeltjes die elektronen opnemen. Voor een redoxreactie heb je dus een reductor en een oxidator nodig. De reductor staat elektronen af aan de oxidator, waardoor er een chemische verandering plaatsvindt.
De edelheid van metalen beschrijft hoe gemakkelijk metalen reageren met hun omgeving. Metalen kunnen worden ingedeeld in verschillende categorieën op basis van hun edelheid:
•Edele metalen (bijv. goud, zilver, platina): reageren niet met zuurstof en water (bijv. sieraden)
•Halfedele metalen (bijv. koper, ijzer): reageren matig met zuurstof en water (bijv. roest op een fiets)
•Zeer onedele metalen (bijv. natrium, kalium): reageren heftig met zuurstof en water (bijv. natrium in water)
Om een redoxreactie volledig te begrijpen, moet je weten dat deze bestaat uit twee halfreacties:
•De reductorhalfreactie - beschrijft hoe de reductor elektronen afstaat.
•De oxidatorhalfreactie - beschrijft hoe de oxidator elektronen opneemt.
In BiNaS tabel 48 zie je dat halfreacties altijd elektronen bevatten, aan de linkerkant of de rechterkant van de pijl. De positie van elektronen in een halfreactie helpt je te begrijpen hoe elektronen verplaatst worden tijdens de chemische reactie.
Tabel 48 is cruciaal voor het begrijpen van redoxreacties. Hier zie je dat:
•Sterke oxidatoren linksboven in de tabel staan.
•Sterke reductoren rechtsonder in de tabel staan.
Een sterk oxidator betekent automatisch dat het corresponderende deeltje een zwakke reductor is en vice versa.
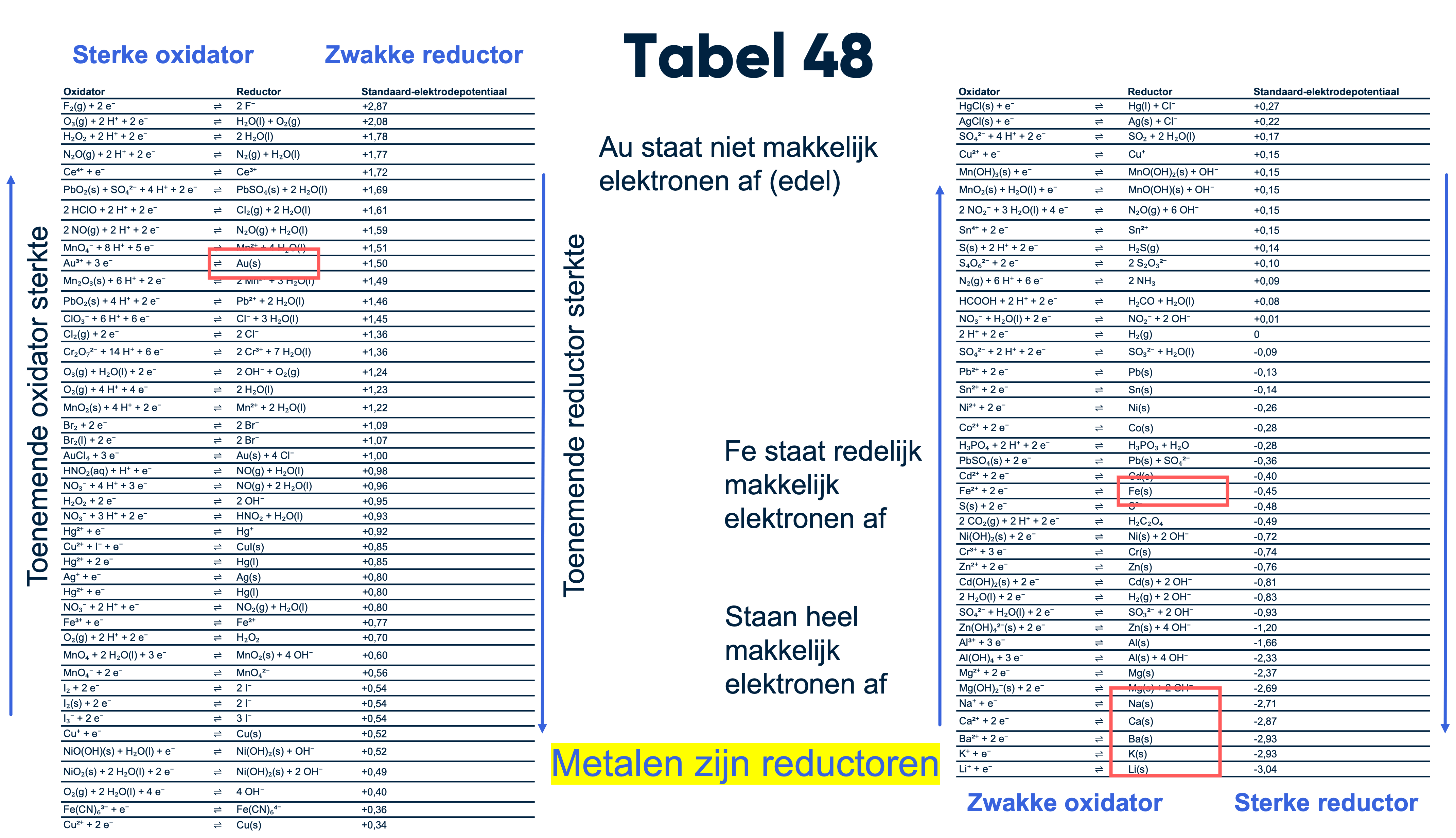
Een voorbeeld uit de tabel is fluor (F₂), een sterke oxidator die elektronen opneemt en verandert in fluoride-ionen (2 F⁻). Dit toont een halfreactie waarbij fluor aan de linkerkant van de pijl elektronen opneemt:
F_2+e^{-}\to2F^{-}F_2+e^{-}\to2FF_2+e^{-}\to2F_2+e^{-}\toF_2+e^{-}-F_2+e^{-}F_2+eF_2+F_2F
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







