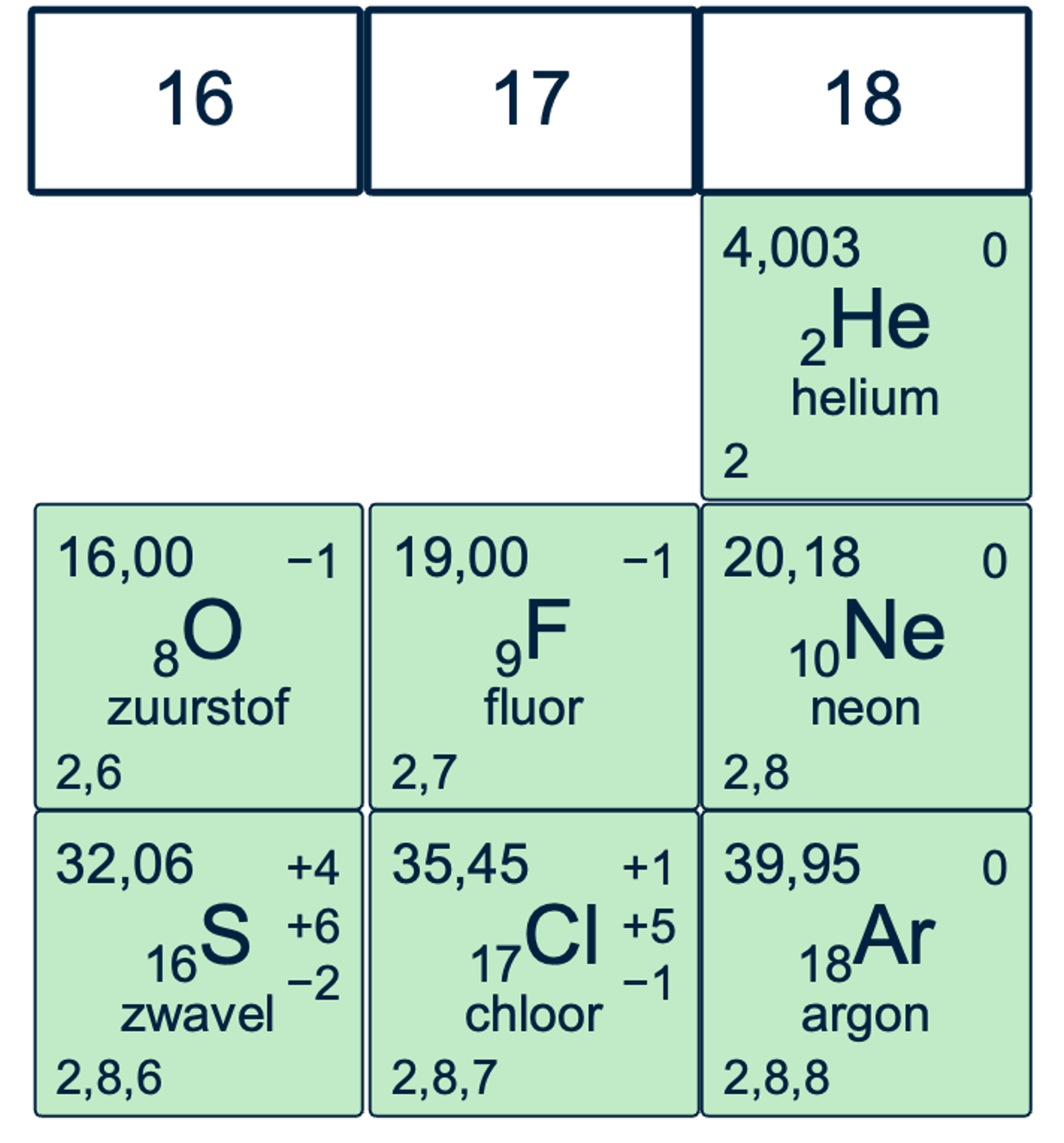
Waarom kan covalentie 6 wel bij zwavel en niet bij zuurstof voorkomen?
Leerdoelen
•Je kunt uitleggen wat een lewisstructuur is.
•Je kunt het nut van lewisstructuren benoemen.
•Je kunt een stappenplan voor het opstellen van een lewisstructuur toepassen.
•Je kunt de formele lading van een deeltje bepalen.
De kapstok van de scheikunde
De kapstok van de scheikunde deelt stoffen in drie categorieën in:
1.Metalen - als het deeltje alleen uit metalen bestaat.
2.Zouten - als het deeltje een combinatie is van metalen en niet-metalen.
3.Moleculaire stoffen - als het deeltje enkel uit niet-metalen bestaat.
Lewisstructuren hebben betrekking op moleculaire stoffen en een belangrijke voorkennis hierbij is het streven van atomen naar een edelgasconfiguratie of de octetregel.
Edelgasconfiguratie en de octetregel
Atomen streven naar een configuratie met volledig gevulde elektronenschillen, zoals de edelgassen die hebben. De eerste drie schillen bevatten 2, 8 en 8 elektronen wanneer ze volledig gevuld zijn. Dit streven wordt de octetregel genoemd. Dit principe verklaart waarom bijvoorbeeld zuurstofatomen geneigd zijn twee elektronen te delen, om zo tot acht valentie-elektronen te komen.
Hoe teken je een lewisstructuur?
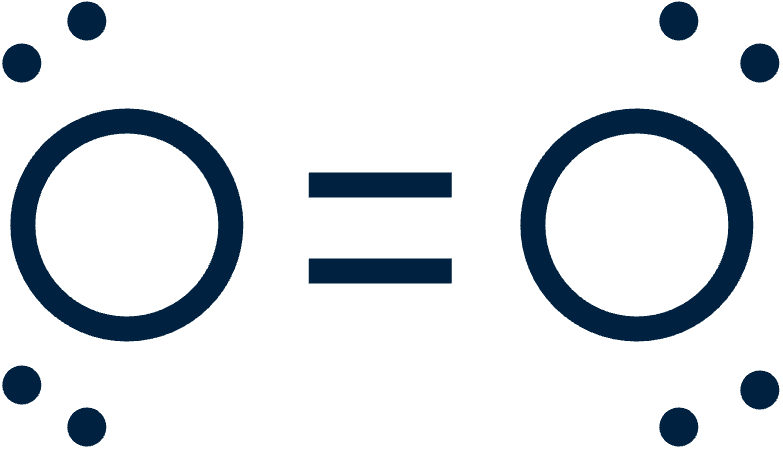
In een lewisstructuur teken je niet alleen de covalente bindingen, maar ook de ongebonden elektronenparen en eventuele formele ladingen. Zo zie je precies hoe de elektronen in een molecuul verdeeld zijn.
Voorbeeld: de lewisstructuur van water
1.Teken de structuurformule, rekening houdend met de covalenties van de atomen (O=2, H=1).
2.Tel het totaal aantal valentie-elektronen. Zoek dit op in Binas en tel ze op. Zuurstof heeft 6 valentie-elektronen en waterstof heeft er 1. Het totaal is .
3.Bepaal hoeveel elektronen nodig zijn om aan de octetregel te voldoen. Voor zuurstof zijn 8 elektronen nodig en voor elk waterstofatoom 2. Het totaal is .
4.Bereken het tekort aan elektronen. Dat zijn de bindingselektronen (12-8=4).
5.Bepaal het aantal bindingen. Deel het aantal bindingselektronen door twee (\frac{4}{2}=2 bindingen).
6.Bepaal de ongebonden elektronen. Trek het aantal bindingselektronen (stap 4) af van het totaal aantal valentie-elektronen (stap 2), 8-4=4, dus 2 vrije paren.

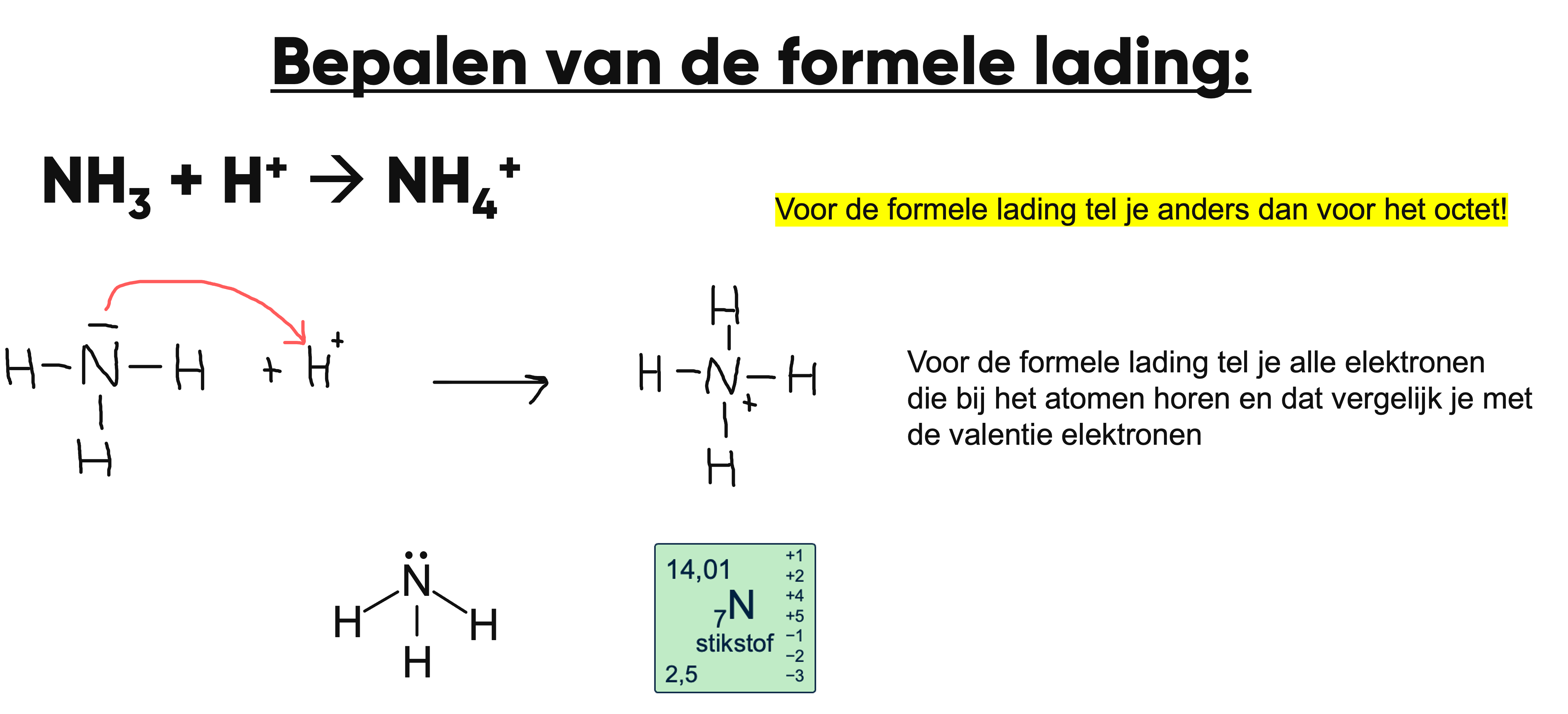
De formele lading bepalen
Het bepalen van de formele lading van een deeltje vereist een specifieke telwijze, waarbij het aantal elektronen dat bij het atoom hoort (ongebonden elektronen + de helft van de gebonden elektronen) wordt vergeleken met het aantal valentie-elektronen van het atoom.
Het ammoniumion als voorbeeld
Het oorspronkelijke vraagstuk over het ammoniumion kan worden verklaard door de lewisstructuur van ammoniak te onderzoeken en te zien hoe het toevoegen van een proton (H+) het ongebonden paar elektronen op het stikstofatoom laat reageren, resulterend in een vierde covalente binding en een positieve formele lading op stikstof.