Is er in de structuurformule sprake van cis-trans-isomerie? Leg je antwoord uit.
Leerdoelen
•Je kunt het verschil tussen structuurisomerie en stereoisomerie uitleggen.
•Je kunt uitleggen wat cis-trans-isomerie is.
•Je kunt cis-trans-isomerie herkennen.
Structuurisomerie versus stereoisomerie
Isomerie betekent dat stoffen dezelfde molecuulformule hebben, maar een andere structuur. Dit kan op twee manieren: als structuurisomerie of als stereoisomerie.
Structuurisomerie
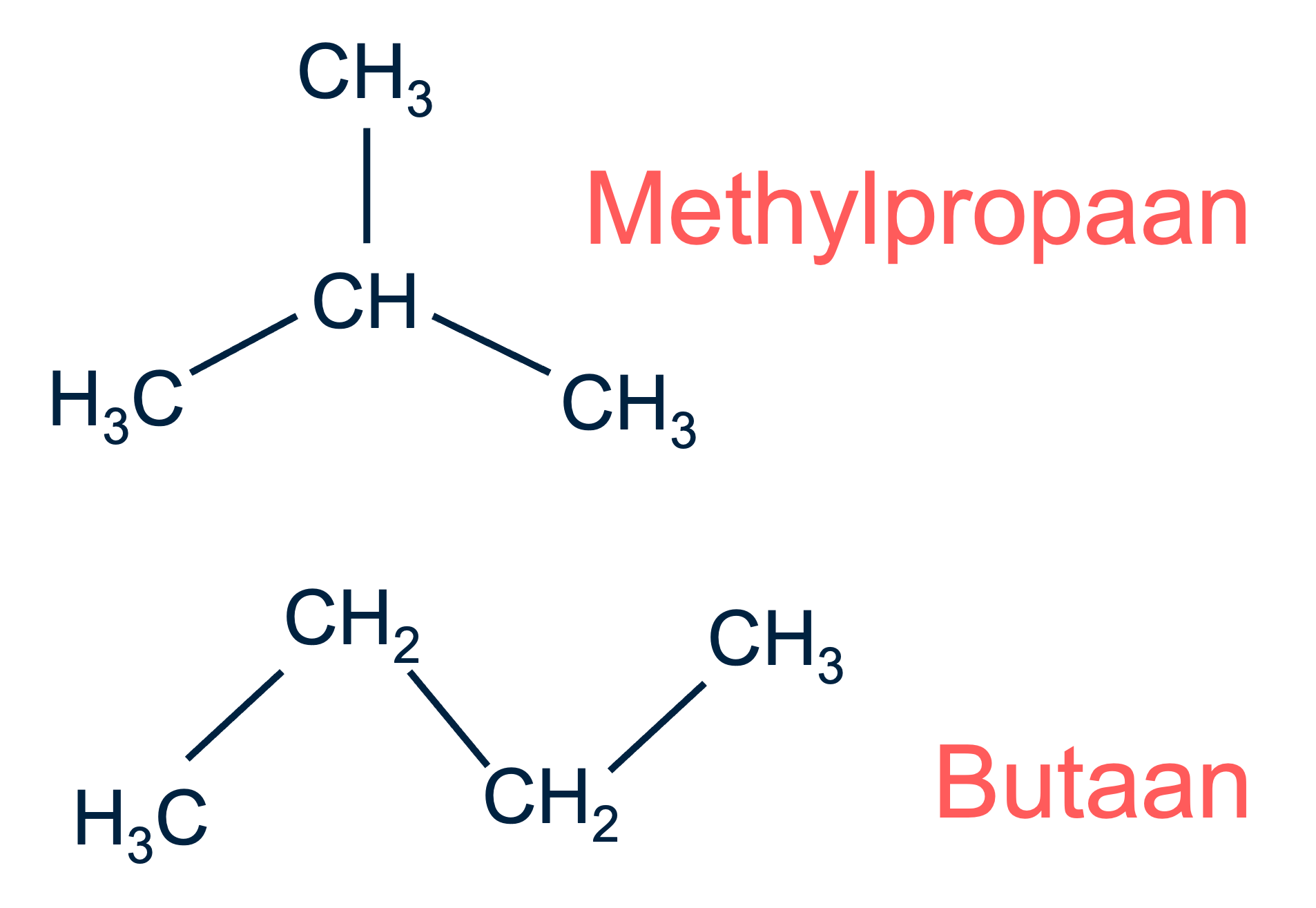
Structuurisomerie gaat over verbindingen die dezelfde atomen hebben, maar waarbij de atomen op een andere manier met elkaar verbonden zijn. Bijvoorbeeld, methylpropaan en butaan hebben beide de formule , maar hun structuren verschillen. Dit is een duidelijk voorbeeld van structuurisomerie.
Een ander voorbeeld van structuurisomerie wordt duidelijk bij het vergelijken van 1,1-dichloorethaan met 1,2-dichloorethaan. Beide hebben dezelfde molecuulformule , maar de plaatsing van de chlooratomen varieert, wat resulteert in twee structureel verschillende verbindingen.
Stereoisomerie
Stereoisomerie beschrijft moleculen die dezelfde bindingen tussen atomen hebben, maar waarbij de ruimtelijke oriëntatie van de atomen verschilt. Dit type isomerie splitst zich op in cis-trans-isomerie en spiegelbeeldisomerie.
Cis-trans-isomerie
Bij cis-trans-isomerie komen de verschillen tot stand door de ruimtelijke oriëntatie van de atomen rondom een starre structuur in het molecuul, vaak veroorzaakt door een dubbele binding of een cyclische structuur.
Vrije draaibaarheid versus starre structuur
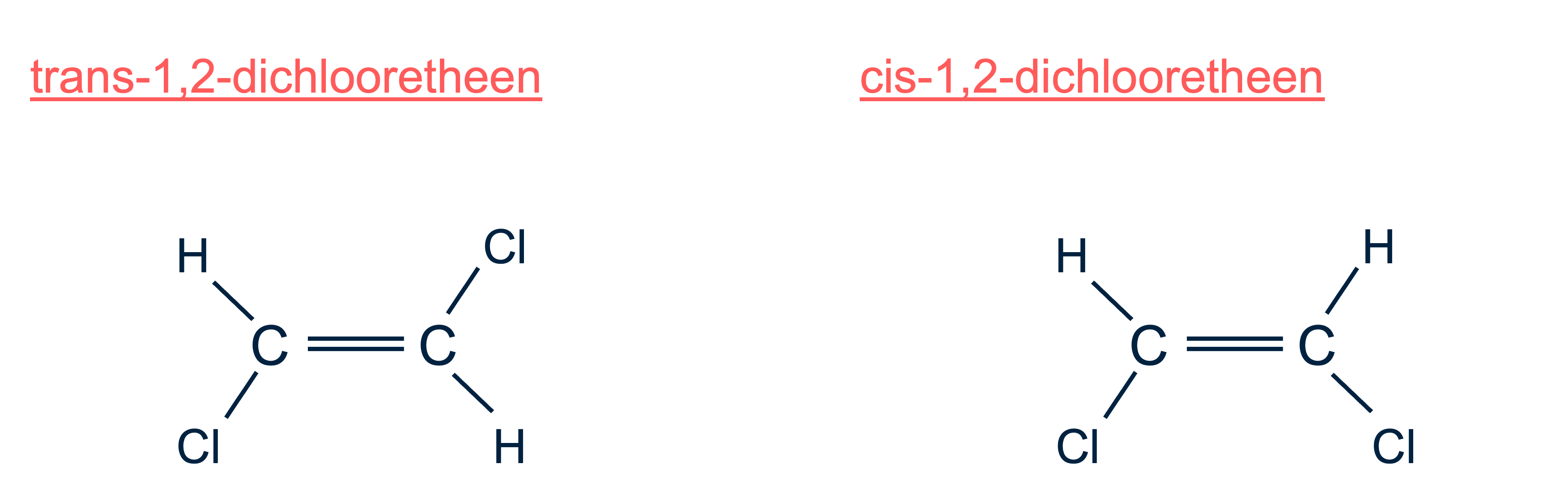
Door de vrije draaibaarheid rond enkelvoudige bindingen, zoals bij chloorethaan, gaan verschillende ruimtelijke rangschikkingen continu in elkaar over. Hierdoor worden ze als één en dezelfde stof beschouwd. Dubbele bindingen, zoals bij 1,2-dichlooretheen, beperken deze draaibaarheid. Hierdoor worden specifieke ruimtelijke oriëntaties vastgelegd; dit leidt tot twee vormen:
•cis-isomeren (waarbij de groepen aan dezelfde kant van de binding zitten).
•trans-isomeren (waarbij ze aan tegenovergestelde kanten zitten).
Voorwaarden voor cis-trans-isomerie
Om cis-trans-isomerie te hebben, moet er aan enkele criteria worden voldaan:
•Er moet sprake zijn van een starre binding, bijvoorbeeld door een dubbele binding of een cyclische structuur, waardoor vrije draaiing niet mogelijk is.
•Aan beide koolstofatomen van deze starre structuur moeten twee verschillende groepen verbonden zijn. Als een koolstofatoom twee dezelfde groepen heeft, is cis-trans-isomerie niet mogelijk.
Cis-trans-isomerie kan ook voorkomen in cyclische verbindingen. In een ringstructuur zitten de atomen in een vast vlak, waardoor ze niet vrij kunnen draaien.
Een voorbeeld is 1,2-dimethylcyclopropaan. In dit molecuul vormen drie koolstofatomen een ring. Aan twee van deze koolstofatomen zit een methylgroep (). Als beide methylgroepen aan dezelfde kant van de ring zitten, is het de cis-vorm. Zitten ze aan tegenovergestelde kanten, dan is het de trans-vorm. Omdat de ring niet kan draaien, blijven deze verschillen bestaan en zijn het twee verschillende stoffen.
Effecten van cis-trans-isomerie
Hoewel cis- en trans-isomeren dezelfde molecuulformule delen, kunnen hun chemische en fysische eigenschappen, zoals kook- en smeltpunt, behoorlijk verschillen. Bovendien kunnen enzymen ook specifiek reageren op één isomeer, maar niet op het andere, vanwege hun structurele verschillen.














