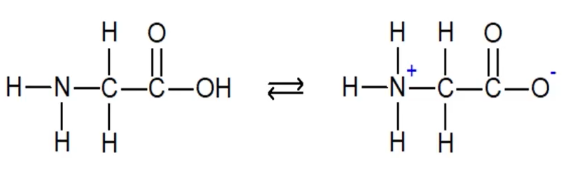Welke stof kan zowel een H+ afstaan als opnemen?
Leerdoelen
•je kunt uitleggen wat amfolieten zijn.
•je kunt bepalen of een amfoliet zich als zuur of base gedraagt.
•je kunt de rol van aminozuren als amfolieten beschrijven.
Wat zijn amfolieten?
Amfolieten zijn deeltjes die zowel als zuur als base kunnen reageren. Een voorbeeld van een amfoliet is natriumwaterstofcarbonaat (NaHCO₃). In water splitst het in natriumionen en waterstofcarbonationen. Het waterstofcarbonation kan als zuur reageren door een H+ af te staan, of als base door een H+ op te nemen.
Gedrag in water
Wanneer natriumwaterstofcarbonaat in water oplost, treden er twee evenwichten op:
Als zuur:
HCO₃⁻ + H₂O ⇌ CO₃²⁻ + H₃O⁺
Kz = 4,7\times10^{-11}4,7\times10^{-1}4,7\times10^{-}4,7\times10^{-}1
Als base:
HCO₃⁻ + H₂O ⇌ H₂CO₃ + OH⁻
Kb = 2,2\times10^{-8}2,2\times10^{-}
De Kz en Kb-waarden bepalen of de oplossing zuur of basisch is. In dit geval is Kb groter dan Kz, wat betekent dat de oplossing basisch is.
Amfolieten in zure en basische oplossingen
Een amfoliet reageert afhankelijk van zijn omgeving:
In een zure oplossing gedraagt het zich als een base en neemt het een H+ op.
In een basische oplossing gedraagt het zich als een zuur en staat het een H+ af.
Voorbeeld: H_2PO_4-H_{\placeholder{}}PO_4-HPO_4-H2PO_4-H2PO_4H2PO_{\placeholder{}}H2POH2PO^{\placeholder{}}H2POH2PO4 reageert als base in een zure oplossing en als zuur in een basische oplossing.
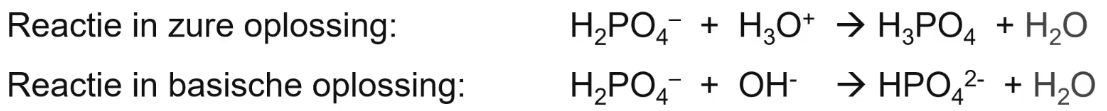
Aminozuren als amfolieten
Aminozuren zijn moleculaire stoffen die als amfolieten fungeren. Ze bestaan uit een NH₂-groep en een C=OOH-groep. In water kunnen aminozuren protonen opnemen of afstaan, waardoor ze dubbelionen vormen. Dit zorgt voor extra elektrostatische aantrekkingskrachten tussen de moleculen, wat resulteert in relatief hoge smeltpunten.
Dankzij hun amfolytische eigenschappen kunnen aminozuren zich aanpassen aan verschillende pH-omstandigheden, wat essentieel is voor hun rol in biologische systemen.