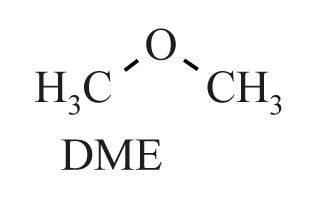
De stof methoxymethaan (DME, zie de figuur) staat in de belangstelling als brandstof. DME kan namelijk worden gemaakt op basis van uitsluitend koolstofdioxide en waterstof.
In een onderzoek is een voorstel voor een productieproces onderzocht.
Dit proces is opgebouwd uit twee opeenvolgende reacties, die hieronder zijn weergegeven.
\begin{array}{ll} \mathrm{CO}_{2}(\mathrm{~g})+3 \mathrm{H}_{2}(\mathrm{~g}) \rightleftharpoons \mathrm{CH}_{3} \mathrm{OH}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O}(\mathrm{~g}) & (\text { reactie 1) } \\ 2 \mathrm{CH}_{3} \mathrm{OH}(\mathrm{~g}) \rightleftharpoons \mathrm{CH}_{3}-\mathrm{O}-\mathrm{CH}_{3}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O}(\mathrm{~g}) & (\text { reactie 2) } \end{array}
De vormingswarmte van DME bedraagt$-1{,}84 \cdot 10^{5} \mathrm{~J} \mathrm{~mol}^{-1}.
