De meeste auto's met een brandstofcel gebruiken waterstof als brandstof.
Om een 'volle' tank waterstof te krijgen, moet waterstof onder zeer hoge druk worden opgeslagen. Dit opslaan onder hoge druk is niet nodig als waterstof met stikstof uit de lucht eerst wordt omgezet tot ammoniak.
$\mathrm{N}_{2}+3 \mathrm{H}_{2} \rightarrow 2 \mathrm{NH}_{3}(reactie 1)
Ammoniak is ook geschikt als brandstof in een brandstofcel en kan gemakkelijker vloeibaar gemaakt worden dan waterstof. In figuur 1 is een ammoniak-brandstofcel schematisch weergegeven.
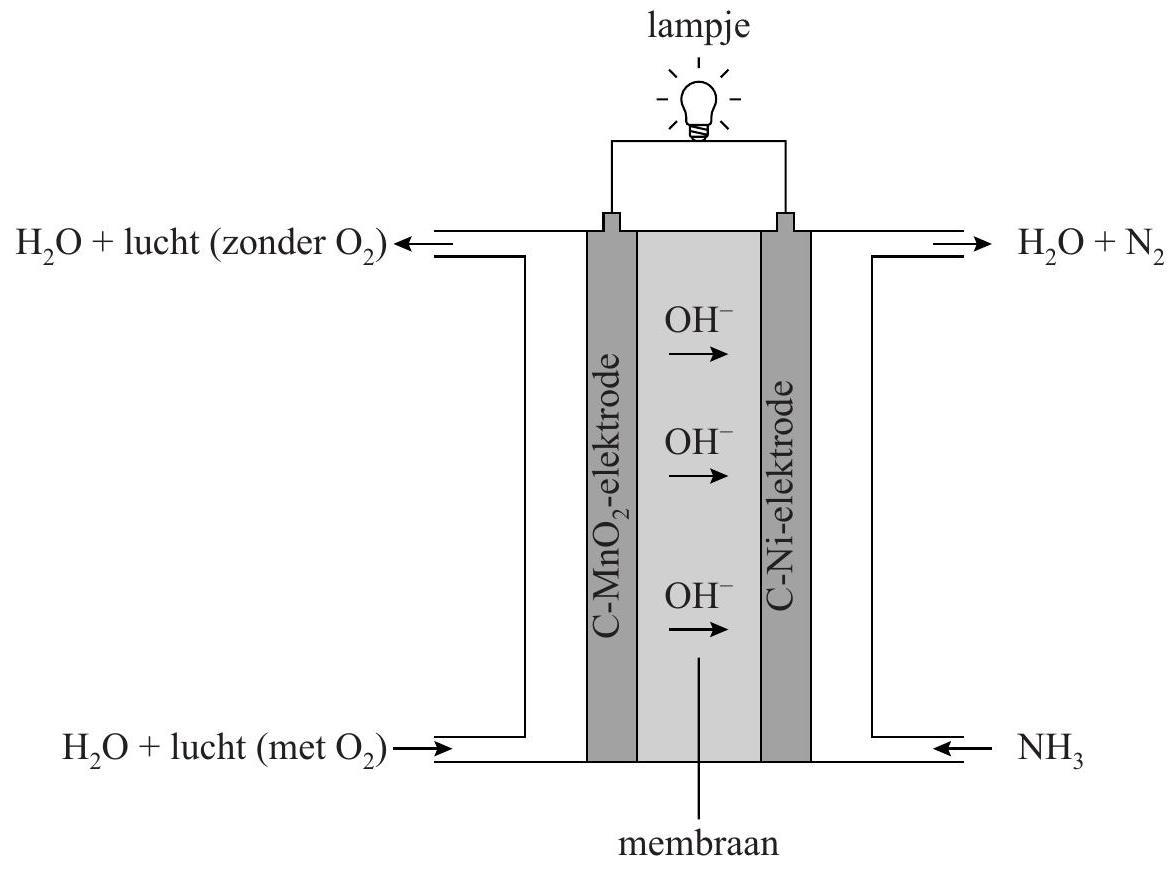
In deze brandstofcel reageert zuurstof aan de\mathrm{C}-\mathrm{MnO}_2\mathrm{CMnO}_2$\mathrm{C}-\mathrm{MnO}_{2}-elektrode volgens halfreactie a:
$\mathrm{O}_{2}+2 \mathrm{H}_{2} \mathrm{O}+4 \mathrm{e}^{-} \rightarrow 4 \mathrm{OH}^{-}(halfreactie a)
Aan de\mathrm{C}-\mathrm{Ni}\mathrm{C}-\mathrm{Nin}\mathrm{C}-\mathrm{NinO}\mathrm{C}-\mathrm{NinO}_{}\mathrm{C}-\mathrm{NinO}_2\mathrm{C}-\mathrm{MNinO}_2\mathrm{C}-\mathrm{MNnO}_2\mathrm{C}-\mathrm{MnO}_2-elektrode reageert ammoniak volgens halfreactie b. Halfreactie b is hieronder onvolledig weergegeven: de coëfficiënten ontbreken.
$\mathrm{NH}_{3}+\mathrm{OH}^{-} \rightarrow \mathrm{N}_{2}+\mathrm{H}_{2} \mathrm{O}+\mathrm{e}^{-}(halfreactie b)
