Oude spaarlampen en oude tl-buizen bevatten stoffen die worden aangeduid met de afkorting HALO. HALO geeft de gewenste kleur aan het licht. De kleur wordt onder andere bepaald door een klein percentage antimoonionen ($\mathrm{Sb}^{3+}) in HALO. Het aantal elektronen (en de verdeling ervan over de schillen) in de$\mathrm{Sb}^{3+}-ionen zijn daarbij van belang.
- Oefen examens van de afgelopen 5 jaar met extra uitleg door docenten bij examenvragen
- Extra uitleg en oefenen voor elk onderwerp uit je examen
- Stel vragen en krijg direct antwoord

De ontwikkelde methode verloopt in een aantal stappen.
stap 1: Aan HALO wordt een overmaat zoutzuur gevoegd. Daarbij ontstaat een waterige oplossing. De$\mathrm{Sb}^{3+}-ionen uit HALO worden omgezet tot$\mathrm{SbCl}_{4}{ }^{-}-ionen.
stap 2: Aan de oplossing uit stap 1 wordt de eerdergenoemde ionische vloeistof toegevoegd. De ionische vloeistof mengt niet met de oplossing die in stap 1 is ontstaan. Er ontstaat een twee-lagensysteem. Tussen de twee vloeistoffen worden de$\mathrm{Cl}^{-}-ionen uit de ionische vloeistof met de$\mathrm{SbCl}_{4}{ }^{-}-ionen van stap 1 uitgewisseld (zie figuur 3). Na enige tijd worden de twee vloeistoflagen A en B van elkaar gescheiden.
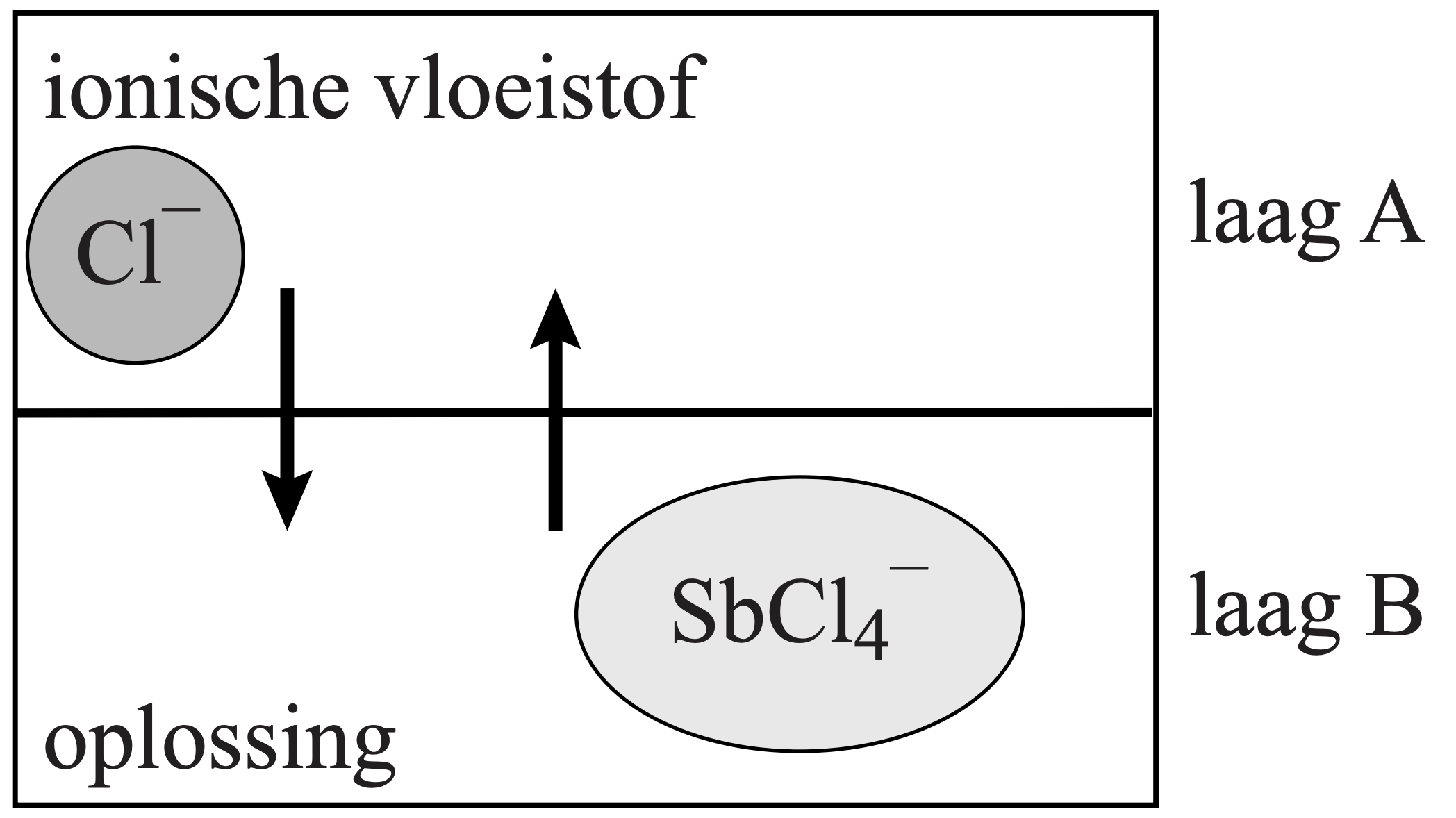
stap 3: Aan laag A wordt een natriumhydroxide-oplossing toegevoegd.
De twee vloeistoffen worden flink door elkaar geschud. De volgende reactie treedt op:
2 \mathrm{SbCl}_{4}^{-}+6 \mathrm{OH}^{-} \rightarrow \mathrm{Sb}_{2} \mathrm{O}_{3}(\mathrm{~s})+3 \mathrm{H}_{2} \mathrm{O}+8 \mathrm{Cl}^{-}
$\mathrm{Sb}_{2} \mathrm{O}_{3}wordt afgescheiden van de twee vloeistoffen.
Leg uit welke scheidingsmethode geschikt is om$\mathrm{Sb}_{2} \mathrm{O}_{3}te scheiden van de twee vloeistoffen.
Op deze pagina behandelen we vraag 28 van het centraal examen scheikunde havo 2019 – tijdvak 1. Deze vraag is onderdeel van Grondstoffen uit spaarlampen, en is 2 punten waard.
Je kunt hier zelf het antwoord invullen en vervolgens direct de uitwerking en uitleg bekijken.
Daarnaast kun je:
- Oude antwoorden terugzien
- Extra uitleg vragen aan onze AI-hulp via de knop "Stel je vraag"
- Klikken op de bijbehorende onderwerpen uit de examenroute om verdieping te vinden