Oude spaarlampen en oude tl-buizen bevatten stoffen die worden aangeduid met de afkorting HALO. HALO geeft de gewenste kleur aan het licht. De kleur wordt onder andere bepaald door een klein percentage antimoonionen ($\mathrm{Sb}^{3+}) in HALO. Het aantal elektronen (en de verdeling ervan over de schillen) in de$\mathrm{Sb}^{3+}-ionen zijn daarbij van belang.
- Oefen examens van de afgelopen 5 jaar met extra uitleg door docenten bij examenvragen
- Extra uitleg en oefenen voor elk onderwerp uit je examen
- Stel vragen en krijg direct antwoord

Aangezien antimoon hoog staat op de lijst van elementen die schaars dreigen te worden, is men op zoek naar methoden om$\mathrm{Sb}^{3+}-ionen uit HALO terug te winnen.
Behalve$\mathrm{Sb}^{3+}-ionen bevat HALO fosfaationen en calciumionen die kunnen worden gebruikt om hydroxy apatiet te maken. Hydroxy-apatiet is een grondstof voor kunstmest.
Onderzoekers hebben daarom een methode ontwikkeld waarbij uit HALO twee producten worden verkregen: antimoonoxide en hydroxy-apatiet.

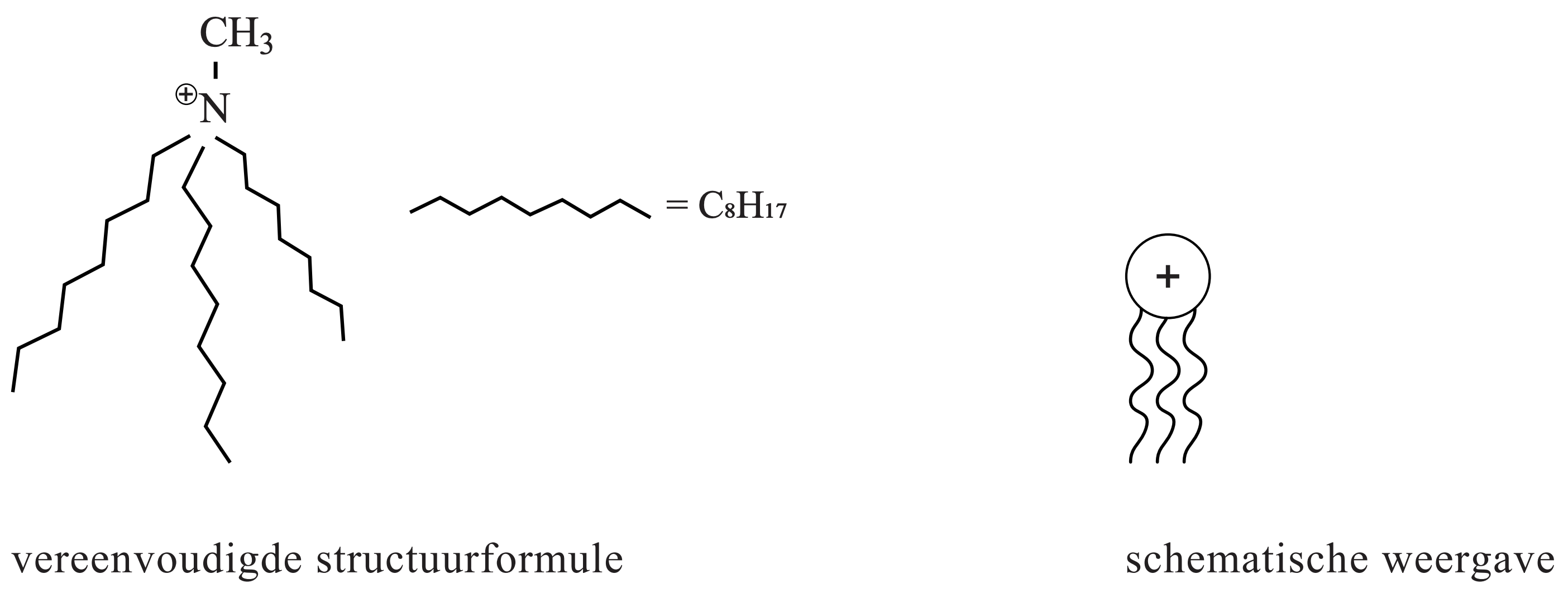
In deze methode wordt een ionische vloeistof gebruikt. Een ionische vloeistof is een zout dat vloeibaar is bij lage temperaturen, bijvoorbeeld bij kamertemperatuur. De gebruikte ionische vloeistof$((\mathrm{C}_{8} \mathrm{H}_{17})_{3} \mathrm{CH}_{3} \mathrm{NCl})bestaat uit$(\mathrm{C}_{8} \mathrm{H}_{17})_{3} \mathrm{CH}_{3} \mathrm{~N}^{+}-ionen en$\mathrm{Cl}^{-}-ionen. De$(\mathrm{C}_{8} \mathrm{H}_{17})_{3} \mathrm{CH}_{3} \mathrm{~N}^{+}-ionen zijn in figuur 1 met een vereenvoudigde structuurformule en op schematische wijze weergegeven.
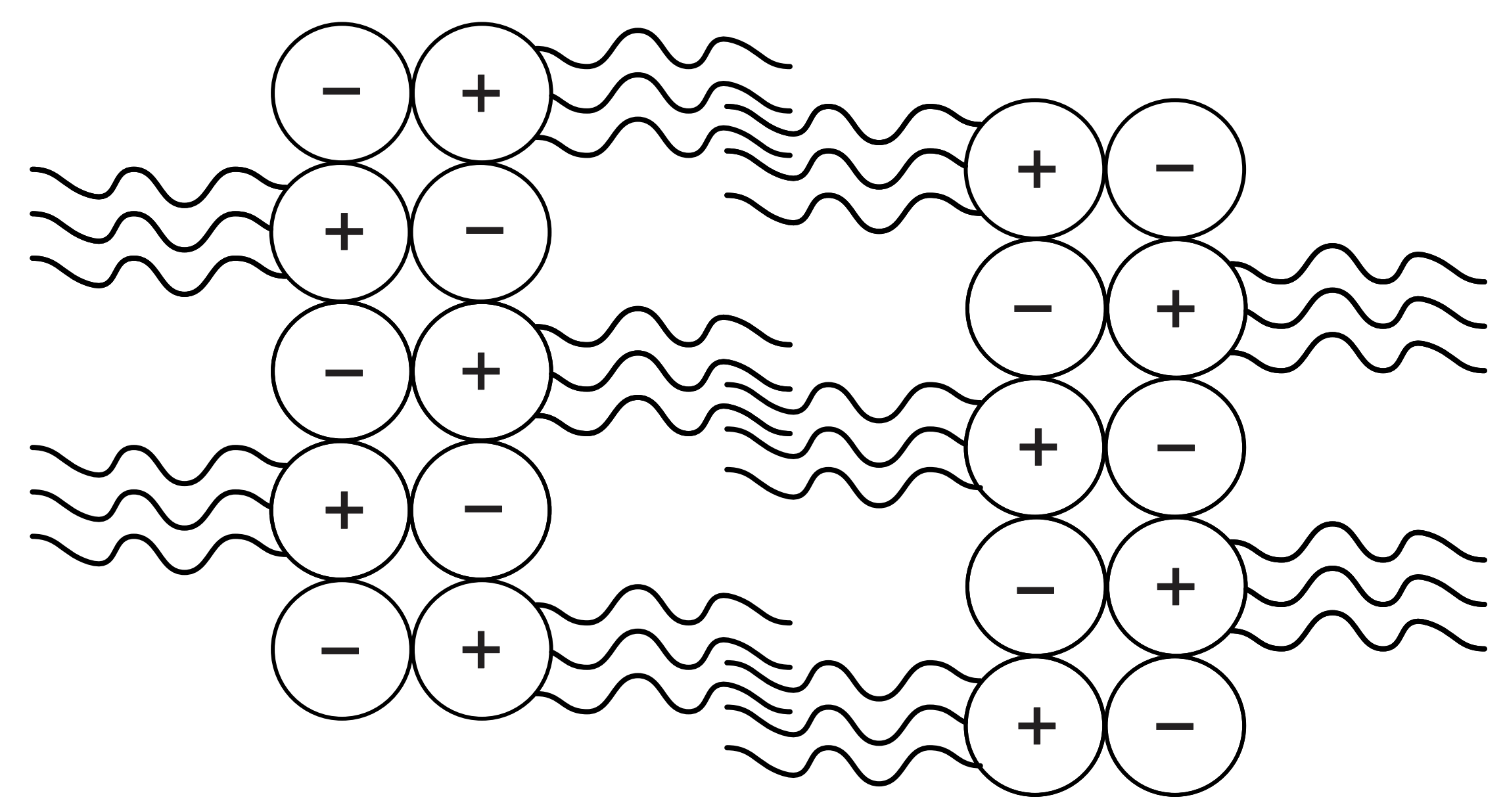
De vaste stof$(\mathrm{C}_{8} \mathrm{H}_{17})_{3} \mathrm{CH}_{3} \mathrm{NCl}heeft een veel lager smeltpunt dan het zout NaCl . Het verschil in smeltpunt kan verklaard worden aan de hand van de roosteropbouw van beide stoffen. Een mogelijke roosteropbouw van$(\mathrm{C}_{8} \mathrm{H}_{17})_{3} \mathrm{CH}_{3} \mathrm{NCl}is vereenvoudigd en schematisch weergegeven in figuur 2.
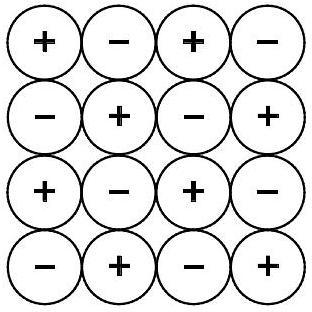
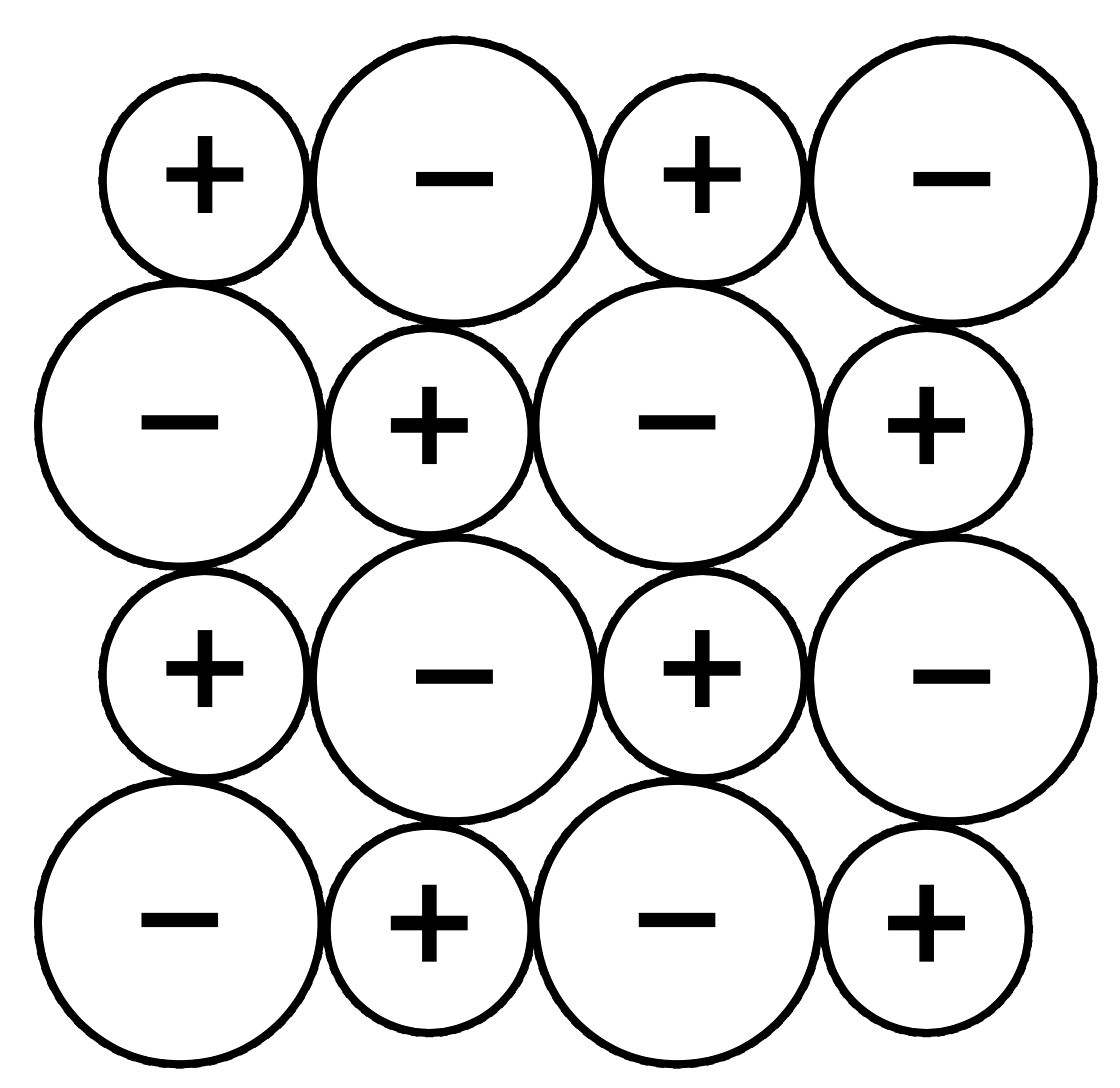
Geef met behulp van een schets de roosteropbouw van NaCl weer.
•Teken acht positieve en acht negatieve ionen.
•Gebruik voor elk positief ionen voor elk negatief ion.
Op deze pagina behandelen we vraag 26 van het centraal examen scheikunde havo 2019 – tijdvak 1. Deze vraag is onderdeel van Grondstoffen uit spaarlampen, en is 1 punt waard.
Je kunt hier zelf het antwoord invullen en vervolgens direct de uitwerking en uitleg bekijken.
Daarnaast kun je:
- Oude antwoorden terugzien
- Extra uitleg vragen aan onze AI-hulp via de knop "Stel je vraag"
- Klikken op de bijbehorende onderwerpen uit de examenroute om verdieping te vinden