Wat is de triviale naam voor natriumchloride?
Leerdoelen
•Je kunt stofeigenschappen van zouten benoemen.
•Je kunt de oplosbaarheidstabel aflezen.
•Je kunt een oplosvergelijking opstellen.
•Je kunt een indampvergelijking opstellen.
Triviale en systematische namen
Veel stoffen hebben net als keukenzout twee namen: een dagelijkse naam (triviale naam) en een scheikundige naam (systematische naam). Natriumchloride is de scheikundige naam voor keukenzout.
Opbouw van een zout
Een zout is altijd opgebouwd uit twee delen: een positief ion en een negatief ion. Vaak is het positieve ion een metaal en het negatieve ion een niet-metaal. Deze geladen deeltjes, de ionen, trekken elkaar aan en vormen zo het zout.
Stofeigenschappen van zouten
Zouten hebben een paar belangrijke eigenschappen. Zouten zijn bij kamertemperatuur altijd een vaste stof. Als zouten in vaste toestand zijn, geleiden ze geen stroom. Als je stroom door een potje zout probeert te sturen, gebeurt er niks.
Dit verandert als je het zout oplost in water. In water komen de ionen los van elkaar en kunnen ze vrij bewegen. Omdat ionen geladen deeltjes zijn, kunnen ze stroom geleiden. Hierdoor kan een lampje gaan branden als je het aansluit op een zoutoplossing.
Faseaanduidingen
Bij scheikundige vergelijkingen geven we de fase van een stof aan met een letter tussen haakjes:
•(s) van solid: vast
•(l) van liquid: vloeibaar
•(g) van gas: gas
Maar wat als een stof is opgelost in water? Dan is het geen vloeistof geworden, maar het zit gemengd in het water. Hiervoor gebruiken we een nieuwe faseaanduiding:
•(aq) van aqua: opgelost in water
De oplosbaarheidstabel
Niet alle zouten lossen even goed op in water. Denk bijvoorbeeld aan:
•Keukenzout: lost goed op (aangeduid met de letter g)
•Gips: lost matig op (aangeduid met de letter m)
•Krijt: lost slecht op (aangeduid met de letter s)
Om te weten hoe goed een zout oplost, gebruiken we de oplosbaarheidstabel. In deze tabel staat per combinatie van ionen aangegeven of het zout goed (g), matig (m) of slecht (s) oplosbaar is. Soms zie je een streepje staan. Dit betekent meestal dat dit zout niet bestaat, of dat de oplosbaarheid niet bekend is.
De oplosbaarheidstabel vind je in de Binas (tabel 35) of in je scheikundeboek. Je zoekt de twee ionen op waaruit het zout is opgebouwd. Waar de rij en kolom van deze ionen elkaar kruisen, staat een letter (g, m, s of een streepje) die de oplosbaarheid aangeeft. In deze tabel kun je ook de ladingen van de ionen vinden.
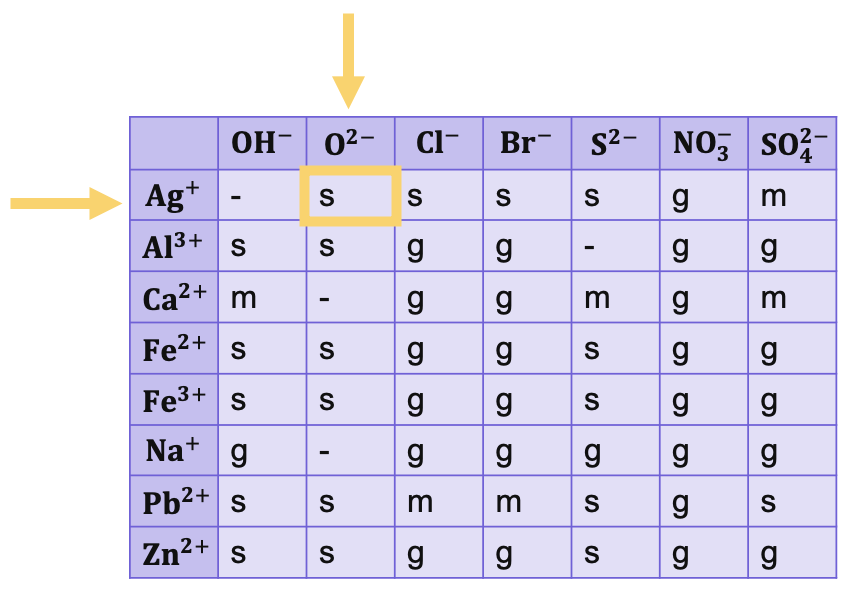
Oefenen met de oplosbaarheidstabel
Om de oplosbaarheid te bepalen van zilveroxide, zoeken we de ionen op waaruit het bestaat:en. Als je deze opzoekt in de oplosbaarheidstabel, zie je dat zilveroxide slecht oplost in water (s).
Oplossen en indampen in vergelijkingen
De oplosvergelijking
Een oplosvergelijking toont aan wat er gebeurt als een zout in water oplost. Dit doen we alleen voor zouten die goed oplossen. De algemene vorm is:
Zout (s) → ion 1 (aq) + ion 2 (aq)
Het zout begint als een vaste stof (s). Als het oplost, komen de ionen vrij in het water (aq).
De indampvergelijking
Een indampvergelijking is precies het tegenovergestelde van een oplosvergelijking. Bij indampen haal je het water weg uit een oplossing, waardoor je het vaste zout weer overhoudt. Dit is een veelgebruikte scheidingsmethode. De algemene vorm ziet er als volgt uit:
ion 1 (aq) + ion 2 (aq) → Zout (s)
Je begint met de opgeloste ionen (aq) en eindigt met het vaste zout (s). Let op: de ionen hebben altijd een lading, maar het zout zelf is ongeladen (neutraal).
Oefenen met de oplosvergelijking: aluminiumsulfaat
1.Verhoudingsformule bepalen:
•Aluminium-ion:
•Sulfaat-ion:(een samengesteld ion) Om de totale lading neutraal te krijgen, zoeken we het kleinste getal dat een veelvoud is van zowel 3 (van) als 2 (van). Dit is 6. Hiervoor hebben we 2 aluminiumionen (totale lading van2\cdot3+=6+23+=6+) en 3 sulfaationen (totale lading van3\cdot2-=6-32-=6-) nodig. De verhoudingsformule is dus. Omdateen samengesteld ion is, zetten we het tussen haakjes met de index erachter.
2.Oplosbaarheid controleren: Nu kijken we in de oplosbaarheidstabel naar de combinatie vanen. Deze geeft aan dat aluminiumsulfaat goed oplost in water, dus we kunnen een oplosvergelijking maken.
3.Oplosvergelijking opstellen: We beginnen met het vaste zout en laten zien dat het uiteenvalt in zijn ionen.
4.Vergelijking kloppend maken: In de verhoudingsformulezien we dat er twee aluminiumionen en drie sulfaationen zijn. Dit moeten we ook aan de rechterkant van de vergelijking aangeven:
Voorbeeld: een slecht oplosbaar zout filtreren
Omdat zinksulfideslecht oplosbaar is, lost maar een heel klein deel ervan op in het water. Het grootste deel blijft als vaste stof in het water zweven. Als je dit mengsel vervolgens filtreert, blijft die vaste stof achter in het filter. Dit vaste stofje noemen we een residu. Het residu zal grotendeels bestaan uit het niet-opgeloste zinksulfide. Het water dat door het filter stroomt (het filtraat) zal bijna geen zinksulfide bevatten, op een heel klein opgelost deel na.













