Op basis van welke stofeigenschap worden mengsels gescheiden bij zowel indampen als destilleren?
Leerdoelen:
•Je kunt uitleggen wat indampen is.
•Je kunt uitleggen wat destilleren is.
Wat zijn scheidingsmethoden?
Een scheidingsmethode is een manier om een mengsel van stoffen te scheiden. Je doet dit op basis van stofeigenschappen. Elke stof heeft zijn eigen unieke eigenschappen, zoals een bepaald kookpunt of deeltjesgrootte. Door gebruik te maken van deze verschillen, kun je verschillende stoffen uit elkaar halen. Er bestaan zes veelgebruikte scheidingsmethoden: bezinken, filtreren, indampen, destilleren, extraheren en adsorberen. In dit artikel leer je meer over indampen en destilleren.
Homogene oplossing
Indampen en destilleren gebruik je allebei bij het scheiden van een speciaal soort mengsel: een homogeen mengsel. Een voorbeeld van een homogeen mengsel is een oplossing. Een oplossing bestaat uit een opgeloste stof (vaak een vaste stof) die helemaal is opgelost in een oplosmiddel (vaak een vloeistof). Denk bijvoorbeeld aan zout dat is opgelost in water. Deze mengsels zijn vaak moeilijk te scheiden. Om ze toch te scheiden kijk je bij indampen en destilleren naar het verschil in kookpunt van de stoffen in het mengsel.
Indampen
Hoe werkt indampen?
Bij indampen ga je een homogeen mengsel, een oplossing, verwarmen. Dit kan bijvoorbeeld met een brander in het practicumlokaal, maar in de natuur gebeurt dit door de zon. Door de warmte zal de stof met het laagste kookpunt verdampen. In een oplossing is dit bijna altijd het oplosmiddel, omdat de opgeloste stof vaak een vaste stof is die pas bij een veel hogere temperatuur smelt of kookt. Het oplosmiddel verandert in damp en verdwijnt in de lucht. Wat er na het verdampen overblijft, is de opgeloste stof. Het indampen is dus een handige methode als je alleen de opgeloste stof wilt opvangen en het oplosmiddel niet nodig hebt.
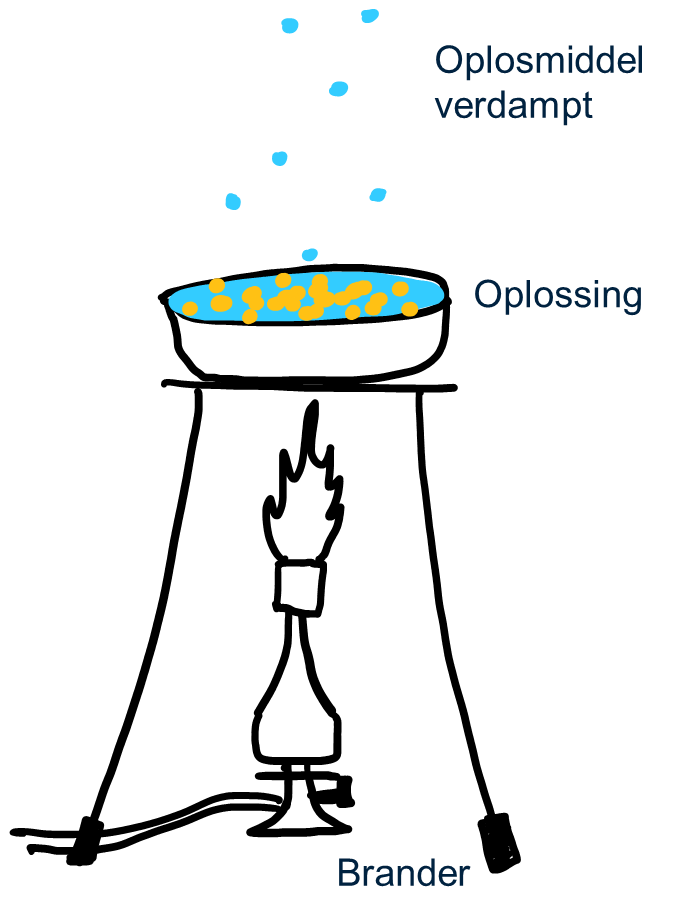
Zout uit zeewater halen
Een bekend voorbeeld van indampen zie je bij het winnen van zout uit de zee. In grote zoutbedden wordt zeewater opgevangen. Na een tijdje blijft daar alleen het zout over. De zon die verwarmt het zeewater in de zoutbedden. Het water verdampt en het zout (de opgeloste stof) blijft over.
Destilleren
Soms wil je niet alleen de opgeloste stof opvangen, maar ook het oplosmiddel. In dat geval gebruik je destilleren. Net als bij indampen, pas je destilleren toe op een homogeen mengsel (een oplossing) en maak je gebruik van het verschil in kookpunt tussen de stoffen. Het grote verschil is dat bij destilleren zowel de opgeloste stof als het oplosmiddel wordt opgevangen. Bij indampen verdwijnt juist het oplosmiddel.
Hoe werkt destilleren?
Voor destilleren heb je een speciale opstelling nodig: een destillatie-opstelling.
1.Je begint met een kolf waarin je het mengsel doet. Deze kolf wordt verwarmd met een brander, net als bij indampen.
2.De stof met het laagste kookpunt zal als eerste verdampen en stijgt op als damp.
3.Deze damp komt in een speciale buis terecht die door een koeler loopt. De koeler is een buitenmantel waardoor koud water stroomt. Dit water mengt zelf niet met de damp. Het gaat er aan de bovenkant in en komt er aan de onderkant weer uit.
4.Het koude water in de koeler zorgt ervoor dat de warme damp afkoelt en weer condenseert (vloeibaar wordt).
5.De afgekoelde vloeistof wordt vervolgens opgevangen in een andere kolf.
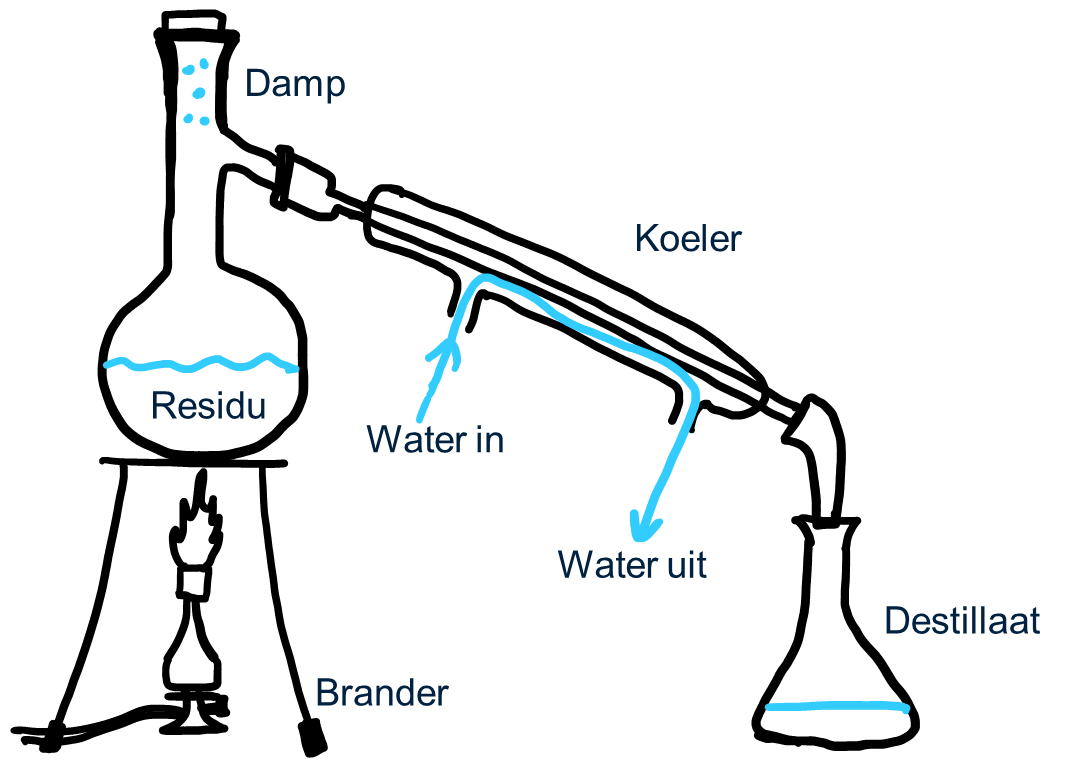
Wat er in de oorspronkelijke kolf (de verwarmde kolf) achterblijft, noemen we het residu. Dit is de stof met het hogere kookpunt. De vloeistof die in de nieuwe kolf is opgevangen na het afkoelen, noemen we het destillaat. Dit is de stof die eerst verdampt is en vervolgens weer vloeibaar is geworden. Een voorbeeld hiervan is gedestilleerd water: puur water zonder opgeloste zouten, waarbij het water het destillaat is.
De stroomrichting van het gekoelde water
Het koelwater stroomt op een specifieke manier door de koeler: het water gaat er aan de bovenkant in en stroomt er aan de onderkant weer uit. De damp stroomt van boven naar beneden door de koeler en is bovenaan het warmst. Als het koude water van boven naar beneden stroomt, komt het steeds in contact met een warmer deel van de koeler. Zo blijft de koeler overal goed koud en kan de damp efficiënt afkoelen. Als het water andersom zou stromen (van onder naar boven), zou het water onderin al opwarmen en minder goed koelen als het bovenin bij de warmste damp aankomt.













